Evolocumab: snížení hodnot LDL cholesterolu i kardiovaskulárního rizika
Souhrn:
Přibližně před deseti lety byl objeven nový protein označený jako proprotein konvertáza subtilisin/kexin 9 – PCSK9, který významně ovlivňuje sérové koncentrace LDL cholesterolu. Ve velmi krátké době výzkum vyústil v přípravu specifických monoklonálních protilátek blokujících tento protein. Evolo-cumab je jednou z prvních dostupných humánních monoklonálních protilátek proti PCSK9. V důsledku blokády se zvyšuje počet recirkulujících LDL receptorů na povrchu hepatocytu, což vede k poklesu hodnot LDL cholesterolu (i dalších aterogenních lipidů) v séru o 50–70 % nad rámec dosažitelný ostatními dostupnými způsoby léčby. Bezpečnost a účinnost evolocumabu je testována v rozsáhlém výzkumném programu PROFICIO. Tato nová tera-peutická možnost představuje naději pro obtížně léčitelné nemocné s familiární hypercholesterolemií nebo s intolerancí statinů a do budoucna možná i pro další pacienty s velmi vysokým a vysokým kardiovaskulárním rizikem, kteří nedosahují cílových hodnot LDL cholesterolu běžnými postupy.
Key words: cardiovascular risk – LDL cholesterol – hypolipidemics – PCSK9 – monoclonal antibodies – evolocumab.
Summary:
Some 10 years ago, a novel protein called proprotein convertase subtilisin/kexin type 9, PCSK9, was described, profoundly affecting the serum concentrations of LDL cholesterol. Within a very short time, this knowledge has led to the preparation of specific monoclonal antibodies blocking this protein. Evolocumab is one of the first available human monoclonal antibodies against PCSK9. As a result of the blockade, the number of re circulating LDL receptors on the surface of hepatocytes increases, leading to the drop in the serum concentrations of LDL cholesterol (and other atherogenic lipids) by 50–70%, i.e. to an effect not achievable by any other known treatment modalities. The effectiveness and safety of evolocumab is being tested in a large scientific program called PROFICIO. This novel therapeutic option brings hope to hard to treat patients with familial hypercholesterolemia or statin intolerance and, in future, possibly to other patients with very high or high cardiovascular risk not achieving their LDL cholesterol targets with more common therapy.
Léčba dyslipidemií, jednoho z nejdůležitějších rizikových faktorů aterosklerózy, představuje jednu z hlavních možností snížení kardiovaskulárního rizika. Snížení sérové koncentrace LDL cholesterolu je primárním léčebným cílem. Jak ukázaly početné studie se statiny i jejich následné metaanalýzy, účinnost a bezpečnost této léčby patří k nejlepším nejen v kardiologii, ale i ve srovnání s dalšími medicínskými odvětvími. Studie také přinesly data potřebná pro stanovení doporučených cílových hodnot LDL cholesterolu; ty se postupně snižovaly až na současnou úroveň a víme, že jejich dosahování není zdaleka optimální. Výsledky opakovaných průzkumů jasně ukazují, že dosahování cílových hodnot se u velmi vysoce a vysoce rizikových osob pohybuje na úrovni maximálně 50 % [1,2]. Proto chápeme, že vývoj zaměřený na hledání způsobů, jak snížit koncentrace LDL cholesterolu nad rámec dosažitelný současnými možnostmi, nadále pokračuje. Nové směry hypolipidemické léčby se primárně zaměřují právě na snižování hodnot LDL cholesterolu. Nejslibnější se zdá vývoj v oblasti monoklonálních protilátek proti proprotein konvertáze subtilisin/kexin 9
(PCSK9).
PCSK9 – od objevu proteinu k terapeutickému využití za deset let
Proprotein konvertáza subtilisin/kexin 9 byla objevena teprve v roce 2003, ale určitě bychom si název tohoto proteinu (nebo alespoň jeho zkratku) měli zapamatovat. Jde o serinovou proteázu s maximem exprese v buňkách jaterní a střevní tkáně. Francouzští autoři popsali nový genový lokus pro PCSK9 u rodin s autosomálně dominantní formou familiární hypercholesterolemie [3]. Jeho zatím jedinou poznanou funkcí je regulace exprese receptoru pro LDL cholesterol. Proprotein konvertáza subtilisin/kexin 9 tvoří komplex s LDL receptorem a ten je následně internalizován do cytoplazmy. Vazba PCSK9 na LDL receptor znemožní uvolnění LDL částice z receptoru a celý komplex LDL receptor + LDL částice + PCSK9 je následně degradován v lysosomu. Tímto mechanismem PCSK9 brání normálnímu průběhu recyklace LDL receptoru a jeho zpětnému vystavení na plazmatické membráně. Bez přítomnosti PCSK9 může LDL‑receptorový protein za dobu své životnosti takto recirkulovat až 150krát.
Aktivita PCSK9 tedy reguluje počet LDL receptorů na povrchu buněk [4]; je‑li aktivita PCSK9 zvýšená, počet receptorů klesá a koncentrace LDL cholesterolu stoupá, v případě snížení aktivity PCSK9 nastává děj přesně opačný a osoby s geneticky podmíněným poklesem funkce PCSK9 jsou charakterizovány hypocholesterolemií. V epidemiologických studiích sledujících osoby s hypocholesterolemií (hypobetalipoproteinemií) zachytili výzkumníci nositele mutací v genu pro PCSK9 snižujících jeho funkci, kteří byli charakterizováni velmi nízkými koncentracemi LDL cholesterolu. Za ilustrativní lze považovat příběh čtyřicetileté vysokoškolsky vzdělané ženy, matky dvou dětí, která se živila jako cvičitelka aerobiku. Pozornost vzbudila zjištěná koncentrace jejího LDL cholesterolu, která byla 0,36 mmol/l. Genetické vyšetření u ní odhalilo dvě různé mutace snižující funkci PCSK9 – byla tedy složeným heterozygotem s prakticky nedetekovatelnými koncentracemi PCSK9 v séru. Oba její rodiče i někteří sourozenci byli heterozygoty pro mutace v genu pro PCSK9 a jejich sérové koncentrace LDL cholesterolu se pohybovaly pod 1. percentilem populačních rozmezí [5].
Přitom i stručná charakteristika popsané osoby ukazuje na několik důležitých aspektů praktické absence PCSK9 a představuje důležitou informaci o bezpečnosti jak nízké aktivity PCSK9, tak i velmi nízkých hodnot LDL cholesterolu. Ty bývají často dávány do souvislosti s různými riziky, mezi nimiž pravidelně dominují myopatie, poruchy kognitivních funkcí a také riziko snížení produkce steroidních hormonů včetně pohlavních. Fakt, že popsaná žena s celoživotně nízkou sérovou koncentrací LDL cholesterolu intenzivně cvičila, měla vysokoškolské vzdělání a dvě zdravé děti, ilustruje, že nízké koncentrace LDL cholesterolu v séru samy o sobě žádnou z těchto funkcí zásadně neporušují.
Následovala další pozorování, která dokumentovala podobný efekt geneticky podmíněného snížení funkce PCSK9 nejen na sérové koncentrace lipidů, ale také na riziko ischemické choroby srdeční. Výsledky 15letého sledování kohorty více než 3 300 Afroameričanů zařazených do studie ARIC vyvolaly velký ohlas – mezi sledovanými bylo identifikováno 85 nositelů mutace v genu pro PCSK9 se snížením funkce tohoto proteinu. Tito probandi měli o 28 % nižší průměrné hodnoty LDL cholesterolu. Tento nevelký, ale celoživotní rozdíl mezi „běžnou populační“ úrovní LDL cholesterolemie vyústil v dramatický pokles rizika vzniku ischemické choroby srdeční o 88 % [6]. To potvrdili i autoři souhrnné práce sledující vliv genetické variability v několika genových lokusech na hodnoty LDL cholesterolu a míru kardiovaskulárního rizika [7].
Blokáda PCSK9 v léčbě hypercholesterolemie
Pochopení zásad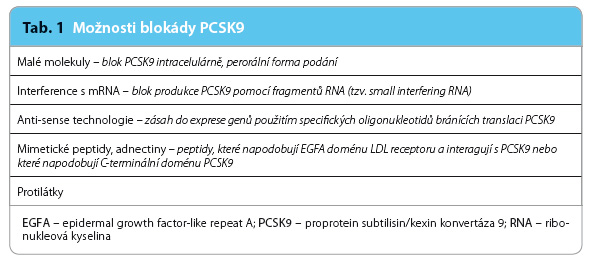 ní úlohy PCSK9 pro metabolismus LDL receptoru, a tedy i LDL částic, vedly rychle k úvaze o možnosti využití inhibice PCSK9 v léčbě hypercholesterolemie a při snižování rizika aterotrombotických cévních příhod. Testuje se více možností ovlivnění PCSK9 (tab. 1), ale nejpokročilejší je výzkum monoklonálních protilátek blokujících vazebné místo PCSK9 pro doménu v proteinu LDL receptoru.
ní úlohy PCSK9 pro metabolismus LDL receptoru, a tedy i LDL částic, vedly rychle k úvaze o možnosti využití inhibice PCSK9 v léčbě hypercholesterolemie a při snižování rizika aterotrombotických cévních příhod. Testuje se více možností ovlivnění PCSK9 (tab. 1), ale nejpokročilejší je výzkum monoklonálních protilátek blokujících vazebné místo PCSK9 pro doménu v proteinu LDL receptoru.
Monoklonální protilátky proti PCSK9, dnes také často označované za PCSK9 inhibitory, představují nejpokročilejší koncept terapeutického využití inhibice PCSK9 v léčbě pacientů s hypercholesterolemií a při snižování kardiovaskulárního rizika. Už dnes můžeme říci, že jde o největší výzkumný farmaceutický program v současné kardiologii, na němž se podílí řada farmaceutických společností. Tři nejpokročilejší zástupci inhibitorů PCSK9 – alirocumab, bococizumab a evolocumab – procházejí klinickým hodnocením v rozsáhlých programech již 3. fáze testujících jejich podávání u různých skupin nemocných [8].
Evolocumab: plně humánní protilátka proti PCSK9
Evolocumab je plně humánní monoklonální imunoglobulin G2 produkovaný buňkami ovarií čínských křečků pomocí technologie rekombinantní DNA s vysokou afinitou k vazebné doméně LDL receptoru pro PCSK9.
Evolocumab se podává subkutánně a má nelineární farmakokinetiku, což znamená, že plazmatická koncentrace léčiva nestoupá spojitě v závislosti na dávce. Opakovaná podání evolocumabu v dávkách nad 140 mg aplikovaných jednou za 14 dnů ale již vykazují farmakokinetiku lineární s dosažením vrcholové koncentrace léčiva 72 hodin po podání. Je odhadováno, že efektivní biologický poločas evolocumabu je 11–17 dní [9].
Evolocumab prochází hodnocením v rozsáhlém programu klinických studií známém pod souhrnným názvem PROFICIO, který testuje tuto účinnou látku v různých režimech u odlišných pacientských populací.
Prvními kandidáty pro léčbu inhibitory PCSK9 jsou nemocní s familiární hypercholesterolemií, kteří představují typickou populaci, u níž současné možnosti hypolipidemické léčby nestačí a potřeba dalších možností ke snížení hodnot LDL cholesterolu je zvláště naléhavá.
Ve studii RUTHEFORD bylo 168 pacientů s heterozygotní familiární hypercholesterolemií randomizováno k léčbě evolocumabem, který byl přidán ke standardní léčbě a podáván v dávkách 350 mg nebo 420 mg každé 4 týdny a 56 pacientů s familiární hypercholesterolemií k podávání placeba po 12 týdnů [10]. Snížení koncentrace LDL cholesterolu dosáhlo ve větvi s pacienty léčenými nižší dávkou evolocumabu (350 mg) 43 % a u pacientů léčených vyšší dávkou (420 mg) 1krát za 4 týdny dokonce 55 % ve srovnání s placebovou skupinou. Tyto změny opět provázelo významné snížení sérových koncentrací triglyceridů o 15–20 %, lipoproteinu (a) o 23–32 % a vzestup koncentrace HDL cholesterolu o 7 %.
Zvláštní pozornost zasluhují klinické studie u pacientů s homozygotní familiární hypercholesterolemií, u nichž současné možnosti farmakoterapie nepřinášejí dostatečný účinek, a proto jsou tito nemocní častými kandidáty lipoproteinové aferézy. Ve studii TESLA byl při sledování 50 pacientů s homozygotní formou familiární hypercholesterolemie zjištěn průměrný pokles koncentrace LDL cholesterolu při podávání evolocumabu o 30,9 % [11]. U většiny nemocných s homozygotní familiární hypercholesterolemií je prokázána kauzální mutace způsobující snížení vazebné afinity nebo jiné z funkcí LDL receptoru, nemocní mají různě velkou zbytkovou receptorovou aktivitu. Tu lze využít pro zprostředkování efektu inhibice PCSK9 a vysvětlit tak i významný účinek evolocumabu u těchto vzácných a těžce postižených pacientů.
Studie TAUSS![Graf 1 Změny lipidových parametrů a koncentrace PCSK9 ve studii TAUSSIG; podle [12] – Bruckert, et al., 2012. HDL cholesterol – cholesterol s lipoproteiny o vysoké hustotě (high-density lipoprotein); PCSK9 – proprotein konvertáza subtilisin/kexin 9](https://www.remedia.cz/photo-a-30403---.jpg) IG testovala význam přidání evolocumabu k léčbě pacientů s homozygotní (n = 34) nebo s těžkou heterozygotní (n = 18) familiární hypercholesterolemií, kteří jsou léčeni LDL‑aferézou. Evolocumab snížil koncentrace LDL cholesterolu u homozygotních pacientů o 17 %, a u heterozygotních dokonce o 65 %; 15 % pacientů s homozygotní familiární hypercholesterolemií a 31 % s heterozygotní formou ve studii snížilo frekvenci nebo zcela ukončilo léčbu LDL‑aferézou [12]. Studie ukázala další směr využití inhibice PCSK9 u nejzávažněji postižených nemocných s hypercholesterolemií (graf 1).
IG testovala význam přidání evolocumabu k léčbě pacientů s homozygotní (n = 34) nebo s těžkou heterozygotní (n = 18) familiární hypercholesterolemií, kteří jsou léčeni LDL‑aferézou. Evolocumab snížil koncentrace LDL cholesterolu u homozygotních pacientů o 17 %, a u heterozygotních dokonce o 65 %; 15 % pacientů s homozygotní familiární hypercholesterolemií a 31 % s heterozygotní formou ve studii snížilo frekvenci nebo zcela ukončilo léčbu LDL‑aferézou [12]. Studie ukázala další směr využití inhibice PCSK9 u nejzávažněji postižených nemocných s hypercholesterolemií (graf 1).
Program PROFICIO samozřejmě hodnotí i běžnější populace nemocných: pacienti s hypercholesterolemií a s vysokým![Graf 2 Pokles hodnot LDL cholesterolu ve srovnání se vstupní hodnotou v závislosti na dávce evolocumabu ve studii MENDEL; podle [13] – Dias, et al., 2012.](https://www.remedia.cz/photo-a-30404---.jpg) kardiovaskulárním rizikem léčení monoterapií evolocumabem byli sledováni ve studii MENDEL, evolocumab v kombinaci s dalšími hypolipidemiky hodnotila u podobné populace studie LAPLACE. Ve studii MENDEL hledala optimální dávku evolocumabu a hodnotila jej v širokém dávkovém rozmezí od 70 mg do 140 mg podávaných každých 14 dnů nebo v rozmezí dávek 280–420 mg podávaných každé 4 týdny [13] (graf 2).
kardiovaskulárním rizikem léčení monoterapií evolocumabem byli sledováni ve studii MENDEL, evolocumab v kombinaci s dalšími hypolipidemiky hodnotila u podobné populace studie LAPLACE. Ve studii MENDEL hledala optimální dávku evolocumabu a hodnotila jej v širokém dávkovém rozmezí od 70 mg do 140 mg podávaných každých 14 dnů nebo v rozmezí dávek 280–420 mg podávaných každé 4 týdny [13] (graf 2).
Účinnost evolocumabu byla závislá na dávce a maxima dosahovala při podávání 140 mg ve dvoutýdenních intervalech nebo 420 mg jedenkrát měsíčně – v obou případech dosahovalo snížení koncentrace LDL cholesterolu přibližně 50 % vstupních hodnot. Koncentrace lipoproteinu (a) klesly v závislosti na dávce o 18–32,3 %. Tento účinek opakovaně demonstrovaly nejen další studie s evolocumabem, ale i s ostatními monoklonálními protilátkami proti PCSK9 – jedná se o žádoucí efekt celé třídy těchto nových léčiv.
Evolocumab u pacientů s intolerancí statinů
Při rozšiřujících se indikacích léčby statiny absolutně narůstá počet pacientů neschopných tolerovat statiny nebo jejich dávku dostatečně vysokou k dosažení léčebných cílů. Pro takové nemocné představují nové modality léčby naději na zlepšení lipidogramu a také celkové prognózy. Studie GAUSS a GAUSS II testovaly pacienty neschopné tolerovat alespoň dva různé statiny v účinných dávkách [14,15]. Výsledky obou studií ukázaly obdobné vlivy na lipidogram jako výše komentované projekty, především pokles koncentrací LDL cholesterolu o více než 50 %.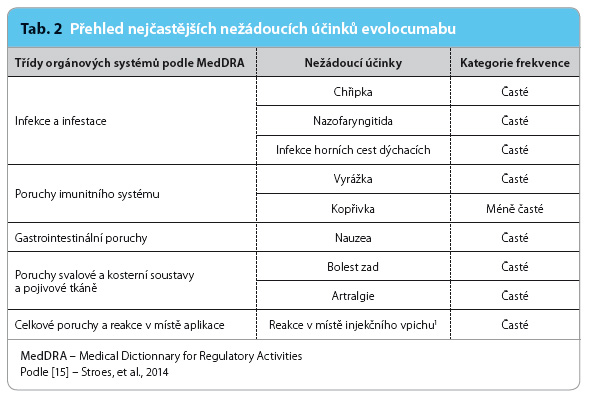
Tolerance léčby byla u pacientů zařazených do studií velmi dobrá (srovnatelná s placebem) a opět se potvrdilo, že nežádoucí účinky nepůsobí snižování sérové koncentrace cholesterolu, ale jsou vázány na konkrétní způsob, kterým jej dosahujeme. Obecně jsou nežádoucí účinky při léčbě evolocumabem (i ostatními inhibitory PCSK9) nečetné a mírné. Přehled těch nejčastěji se vyskytujících uvádí tab. 2 [15].
Účinnost a bezpečnost evolocumabu v delších sledováních
Většina úvodních studií programu PROFICIO s evolocumabem trvala tři měsíce. Proto bylo nutné zjistit účinnost a toleranci léčby v delším časovém období. Téměř roční sledování nemocných s nedostatečně kontrolovanou hypercholesterolemií ve studii DESCARTES, do jejichž léčby byl přidán evolocumab v dávce 420 mg 1krát měsíčně, ukázalo, že nová léčba přináší další přibližně 50% snížení hodnot LDL cholesterolu všem, bez závislosti na typu a dávce souběžně podávané medikace.
Ve studii DESCARTES dosáhlo cílových hodnot LDL cholesterolu < 1,8 mmol/l celkem 82,3 % pacientů [17]. Studie OSLER byly navrženy jako dlouhodobé pokračování studií fáze II (OSLER 1) a fáze III (OSLER 2) se zaměřením na sledování dlouhodobé účinnosti a bezpečnosti léčby evolocumabem. Výsledky souhrnného sledování 4 465 pacientů hodnocených po mediánu sledování 11,1 měsíce byly publikovány v letošním roce [18].
Studie se primárně věnují sledování bezpečnostního![Graf 3 Snížení kardiovaskulárního rizika ve studiích OSLER; podle [18] – Sabatine, et al., 2015. Složeným cílovým ukazatelem byly kardiovaskulární události spojené s následnou hospitalizací, které zahrnovaly infarkt myokardu, koronární revaskularizace, cévní mozkovou příhodu, tranzitorní ischemickou ataku, nestabilní anginu pectoris nebo úmrtí. CI – interval spolehlivosti; HR – poměr rizik](https://www.remedia.cz/photo-a-30406---.jpg) profilu léčby, a nikoli hodnocení vlivu na výskyt cévních příhod. Ten je sledován jako bezpečnostní ukazatel. A přesto představuje jeden z nejdůležitějších „vzkazů“ celého výzkumného programu PROFICIO a náznak toho, že inhibice PCSK9 je tím správným směrem. Ve studiích OSLER autoři zaznamenali podstatné snížení výskytu kardiovaskulárních příhod dosahující více než 50 % nad rámec dosažitelný při jinak dobře vedené standardní léčbě (graf 3).
profilu léčby, a nikoli hodnocení vlivu na výskyt cévních příhod. Ten je sledován jako bezpečnostní ukazatel. A přesto představuje jeden z nejdůležitějších „vzkazů“ celého výzkumného programu PROFICIO a náznak toho, že inhibice PCSK9 je tím správným směrem. Ve studiích OSLER autoři zaznamenali podstatné snížení výskytu kardiovaskulárních příhod dosahující více než 50 % nad rámec dosažitelný při jinak dobře vedené standardní léčbě (graf 3).
Tento výsledek je jistě slibný, ale připomeňme si, že jde o explorativní analýzu dat primárně bezpečnostní studie OSLER, a že jej tedy nesmíme považovat za jednoznačný průkaz účinnosti. Ten je očekáván až od studie FOURIER, která na souboru 22 500 pacientů s kardiovaskulárním onemocněním testuje vliv evolocumabu na výskyt kardiovaskulárních příhod. Studie probíhá od roku 2013 s předpokládaným ukončením v roce 2018 [19].
Závěr
Výsledky probíhajících i uzavřených projektů sledujících podávání inhibitorů PCSK9 vypadají velmi nadějně. Evolocumab shromáždil během výzkumného programu PROFICIO pozoruhodné množství dat, která dokládají, že pacienti léčbu dobře tolerují a hypolipidemický účinek je pronikavý i ve skupinách nejobtížněji ovlivnitelných pacientů s familiární hypercholesterolemií i v homozygotní konstituci. Evolocumab má tedy jistě „právo“ na indikaci v léčbě hypercholesterolemie u pacientů s intolerancí statinů a shromažďuje údaje pro další indikaci, kterou bude snižování kardiovaskulárního rizika u pacientů s nedostatečnou kontrolou dyslipidemie ostatními léčebnými možnostmi. Naplní‑li se očekávání a budou‑li výsledky dlouhodobých mortalitních studií v souladu s těmi dosud publikovanými, otevře se další nová perspektiva léčby a prevence vzniku aterotrombotických cévních komplikací i širší populaci osob s vysokým cévním rizikem.
Podpořeno částečně grantem IGA MZ ČR 14186.
Seznam použité literatury
- [1] Vrablík M, Freiberger T, Lánská V, et al. Projekt Atractiv: zlepšení kardiovaskulární prevence v podmínkách primární péče v České republice. Vnitr Lek 2008, 54: 1131–1139.
- [2] Češka R, Štulc T. Implementation of cardiovascular disease prevention guidelines into clinical practice: an unmet challenge? Curr Pharm Des 2015; 21: 1180–1184.
- [3] Abifadel M, Varret M, Rabes JP, et al. Mutations in PCSK9 cause autosomal dominant hypercholesterolemia. Nat Genet 2003; 34: 154e6.
- [4] Seidah NG. PCSK9 as a therapeutic target of dyslipidemia. Expert Opin Ther Targets 2009; 13: 19e28.
- [5] Zhao Z, Tuakli Wosornu Y, Lagace TA, et al. Molecular characterization of loss of function mutations in PCSK9 and identification of a compound heterozygote. Am J Hum Genet 2006; 79: 514e23.
- [6] Cohen JC, Boerwinkle E, Mosley Jr TH, Hobbs HH. Sequence variations in PCSK9, low LDL, and protection against coronary heart disease. N Engl J Med 2006; 354: 1264e72.
- [7] Ference B, Yoo W, Alesh I, at al. Effect of long term exposure to lower low density lipoprotein cholesterol beginning early in life on the risk of coronary heart disease. J Am Coll Cardiol 2012, 60: 2631–2639.
- [8] Dadu RT, Ballantyne CM. Lipid lowering with PCSK9 inhibitors. Nat Rev Cardiol 2014, 11: 563–575.
- [9] Cicero AFG, Colletti A, Borghi C. Profile of evolocumab and its potential in the treatment of hyperlipidemia. Drug Des Devel Ther 2015; 9: 3073–3082.
- [10] Raal F, Scott R, Somaratne R, et al. Low density lipoprotein cholesterol lowering effects of AMG 145, a monoclonal antibody to proprotein convertase subtilisin/kexin type 9 serine protease in patients with heterozygous familial hypercholesterolemia: the Reduction of LDL C with PCSK9 Inhibition in Heterozygous Familial Hypercholes-terolemia Disorder (RUTHERFORD) randomized trial. Circulation 2012; 126: 2408–2417.
- [11] Raal FJ, Honarpour N, Blom DJ, et al; for the TESLA Investigators. Inhibition of PCSK9 with evolocumab in homozygous familial hypercholesterolemia (TESLA Part B): a randomised, double blind, placebo controlled trial. Lancet 2014; 385: 341–350.
- [12] Bruckert E, Bláha V, Stein E, et al. Trial assessing long term use of PCSK9 inhibition in patients with genetic LDL disorders (TAUSSIG). Efficacy and safety in patients with familial hypercholesterolemia receiving lipid apheresis. Poster sessions, AHA Scientific Sessions, Chicago, 15 19 November 2014.
- [13] Dias CS, Shaywitz AJ, Wasserman SM, et al. Effects of AMG145 on low monoclonal antibody to proprotein convertase subtilisin/kexin type 9 as monotherapy in patients with hypercholesterolaemia (MENDEL): a randomised, double blind, placebo controlled, phase 2 study. Lancet 2012; 380: 1995–2006.
- [14] Sullivan D, Olsson AG, Scott R, et al. Effect of a monoclonal antibody to PCSK9 on low density lipoprotein cholesterol levels in statin intolerant patients. The GAUSS Randomized Trial. JAMA 2012; 308: 2497–2506.
- [15] Stroes E, Colquhoun D, Sullivan D, et al. Anti PCSK9 antibody effectively lowers cholesterol in patients with statin intolerance: the GAUSS 2 randomized, place-bo controlled phase 3 clinical trial of evolocumab. J Am Coll Cardiol 2014; 63: 2541–2548.
- [16] Repatha. Souhrn údajů o přípravku (SPC). Dostupné na http://www.sukl.cz/modules/medication/detail.php?code=0210922&tab=texts
- [17] Blom DJ, Hala T, Bolognese M, et al. A 52 week placebo controlled trial of evolocumab in hyperlipidemia. N Engl J Med 2014; 370: 1809–1819.
- [18] Sabatine MS, Giugliano RP, Wiviott SD, et al. Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med 2015, 372: 1500–1509.
- [19] Further cardiovascular outcomes research with PCSK9 inhibition in subjects with elevated risk (FOURIER). Available from: http://clinicaltrials.gov/show/NCT01764633.