Nitrofurantoin a ovlivnění jeho účinnosti
Souhrn:
Nitrofurantoin je do České republiky dodáván v rámci specifického léčebného programu, v současné době jsou ale dodávky přerušeny. Retardované tablety jsou nahrazovány magistraliter připravovanými tobolkami. V textu je rozebrán rozdíl farmakokinetiky při použití makrokrystalů nitrofurantoinu. Pro správ-nou účinnost je nezbytná edukace pacienta o správném užití stejně jako ověření formy používaného nitrofurantoinu.
Key words: nitrofurantoin – drug form – macrocrystalline – pharmacokinetics.
Summary:
Nitrofurantoin is being imported within delivered on a specific therapeutic program to the Czech Republic. Currently, the deliveries are its import is interrupted. The retarded capsules are being replaced by magistraliter prepared capsules produced in magistral pharmacies. The differences in pharmacokinetics of macrocrystalline and other forms of nitrofurantoin areis discussed. Patient´s education on proper use and the verification of the nitrofurantoin drug form used for magistraliter preparation are essential for efficacious therapy.
Nitrofurantoin (obr. 1), antibiotikum dnes prakticky využívané pouze v léčbě infekcí močových cest a pro dlouhodobou profylaxi uroinfekcí, je do České republiky dodáván v rámci specifického léčebného programu. V současné době ale tento léčivý přípravek není na trhu dostupný a je nahraz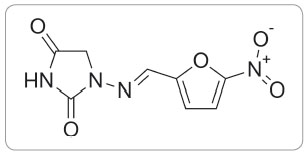 ován magistraliter připravovanými tobolkami s obsahem nitrofurantoinu.
ován magistraliter připravovanými tobolkami s obsahem nitrofurantoinu.
Léková forma hromadně vyráběného léčivého přípravku Nitrofurantoin – Ratiopharm 100 mg® je popsána jako tobolka s prodlouženým uvolňováním [1]. Ovšem v pravém slova smyslu je retardace dosaženo použitím makrokrystalů nitrofurantoinu. Rychlost absorpce je závislá na velikosti krystalů. V zahraničí jsou dostupné přípravky obsahující buď pouze makrokrystaly nitrofurantoinu, nebo kombinaci makrokrystalické a mikrokrystalické formy [2].
Makrokrystalická forma zajistí pomalejší rozpouštění a absorpci oproti mikrokrystalické formě [1–4]. Nedochází tak k vysokým vrcholovým plazmatickým koncentracím a k projevům nežádoucích účinků. Je třeba zdůraznit, že plazmatická koncentrace nitrofurantoinu je nedostatečná pro baktericidní účinek, dostatečných koncentrací převyšujících minimální inhibiční koncentrace (MIC) je dosaženo až v moči [3]. Do moči se nitrofurantoin dostává v menší míře glomerulární filtrací, ve větší míře tubulární sekrecí, tubulární reabsorpce nebyla prokázána [1,2]. Při renální insuficienci se vylučování nitrofurantoinu snižuje, zvyšují se tedy plazmatické koncentrace a zároveň není dosaženo baktericidních koncentrací v moči. Účinnost nitrofurantoinu je rovněž ovlivněna pH moči, je méně účinný v alkalickém prostředí [1,3]. Nitrofurantoin zařazujeme s ohledem na farmakokineticko‑farmakodynamické parametry do skupiny antibiotik s účinkem závislým na čase, tedy cílem je maximální prodloužení doby, kdy koncentrace antibiotika převyšuje MIC.
Nitrofurantoin jako parentní látka nemá antimikrobiální aktivitu, aktivován je až redukcí bakteriálními flavoproteiny. Takto vzniklá redukovaná forma léku se nespecificky váže na různé makromolekuly přítomné v bakteriální buňce, včetně ribozomů, DNA i různých proteinů. Důsledkem je inhibice biochemických procesů typu proteosyntézy, aerobního energetického metabolismu, syntézy DNA, RNA a syntézy buněčné stěny [2]. Protože reakce mezi antibiotikem a buněčnými makromolekulami je nespecifická, nemůže se bakterie před účinkem antibiotika bránit změnou cílového místa, využitím jiné metabolické dráhy nebo zapojením efluxové pumpy. Vznik rezistence na toto antibiotikum u primárně citlivých druhů bakterií je proto velmi vzácný.
Incidence nežádoucích účinků se po podání nitrofurantoinu pohybuje kolem 10 %, incidence plicních postižení představuje asi 0,001 %, neurotoxicita je ještě vzácnější (0,0007 %) [3]. Gastrointestinální nežádoucí účinky jsou na dávce závislé, nejčastěji se vyskytuje nauzea a zvracení, méně časté jsou u makrokrystalických forem a/nebo při užití s jídlem [3,4]. Nitrofurantoin vykazuje hepatotoxické účinky, může způsobit akutní hepatitidy (cholestatické, granulomatózní), podobně jako jeho strukturální analog phenytoin. Pro tyto nežádoucí účinky se jeví být kritická doba léčby 10 dní [5]. Neméně významné jsou také alergické reakce.
Syntézou výše uvedeného je zřejmé, že méně nežádoucích účinků je asociováno s makrokrystalickou formou, jež uvolňuje léčivo pomaleji, nedochází k tak významným vzestupům plazmatické koncentrace, a nežádoucí účinky jsou tudíž méně vyjádřeny. Vliv na pomalejší uvolňování, ale i na celkový rozsah absorpce má současný příjem stravy [4].
Významu tedy nabývá správné dispenzační minimum v lékárně a edukace pacienta. Je vhodné užít nitrofurantoin s jídlem, nebo bezprostředně po jídle, nebo jej užít s mlékem. Díky zpomalení a současnému navýšení absorpce je dosaženo prodlouženého intervalu přítomnosti dostatečných koncentrací antibiotika v moči a je podpořena jeho účinnost.
V lékárnické praxi je pak neméně důležité ověřit si u dodavatele suroviny pro magistraliter přípravu, v jaké formě je nitrofurantoin dodáván s ohledem na rozdíly ve farmakokinetice spojené s velikostí krystalů. Preferována by měla být forma makrokrystalická. Ta odpovídá velikosti krystalu přibližně 90−200 µm [4]. Pro úplnost, v literatuře jsou uváděny velikosti mikrokrystalů od 4 µm do 15 µm, za střední velikost jsou považovány rozměry 50−80 µm [4].
Seznam použité literatury
- [1] Souhrn údajů o přípravku Nitrofurantoin – Ratiopharm 100 mg. Státní ústav pro kontrolu léčiv. [online]. ©2010 [cit. 015 10 23]. Dostupné z: http://www.sukl.cz/modules/medication/detail.php?code=0154748&tab=texts
- [2] Nitrofurantoin. Drugs.com: Know more. Be sure. [online]. ©2010 2015 [cit. 2015 10 23]. Dostupné z: http://www.drugs.com/monograph/nitrofurantoin.html.
- [3] Martindale: The Complete Drug Reference, 36th edition. London: Pharmaceutical Press, 2009.
- [4] Männistö P. The effect of crystal size, gastric content and emptying rate on the absorption of nitrofurantoin in healthy human volunteers. Int J Clin Pharmacol 1978; 16: 223−228.
- [5] Dvořák J. Antimikrobiální látky v léčbě komplikací jaterních onemocnění. Remedia 2011; 21: 372−375.