Naltrexon/bupropion
Souhrn:
Naltrexon/bupropion (Mysimba) je nové centrálně působící antiobezitikum. Tato fixní kombinace (v tabletě s prodlouženým uvolňováním) je v léčbě obezity velmi účinná, neboť obě její složky se v terapeutickém efektu vzájemně doplňují. Bupropion je inhibitor zpětného vychytávání dopaminu a noradrenalinu a naltrexon antagonista opioidních receptorů. Bupropion uvolňuje hormon stimulující alfa melanocyty (alpha‑melanocyte stimulating hormone, α‑MSH), který působí anorekticky, a beta endorfiny, jež vytvářejí zpětnou inhibiční vazbu a tlumí anorektický efekt. Úbytek tělesné hmotnosti je zapříčiněn α‑MSH, jehož působení zesiluje naltrexon, který blokuje inhibiční účinek beta endorfinů. Právě kombinace léčiv má výrazný efekt na hmotnost a další složky metabolického syndromu. Proběhla už rovněž studie s velmi zajímavým pozitivním kardiovaskulárním účinkem v prvních měsících léčby kombinací naltrexon/bu-propion. Do české obezitologie a diabetologie tak vstupuje nová účinná fixní kombinace, která ukončuje téměř desetileté období s omezeným přístupem k podávání centrálně působících antiobezitik.
Key words: anti‑obesity drugs – bupropion – naltrexone – obesity – diabetes – metabolic syndrome – cardiovascular effect.
Summary:
Naltrexone/bupropion (Mysimba) is a new centrally acting anti‑obesity medication. It is a fixed combination of two drugs (in prolonged release tablet) that is higly effective in obesity treatment because of synergistic therapeutic effect of both its components. Bupropion acts as both dopamine, and norepinephrine reuptake inhibitor. Naltrexone is an opioid receptor antagonist. Bupropion releases alpha‑melanocyte stimulating hormone (α‑MSH) causing loss of appetite, while at the same time stimulates the release of beta‑endorphins creating negative feedback to supress anorexic effect. Weight loss is caused by α‑MSH supported in its action by naltrexone which blocks inhibitory effect of beta endorphins. It is the combination of the two drugs that has a significant effect on body weight and other components of the metabolic syndrome. Very interesting beneficial cardiovascular effect in the first few months of naltrexone/bupropion treatment has been shown by clinical trial. Introduction of this new effective fixed drug combination into the Czech obesitology and diabetology community announces the end of almost ten years lasting period of limited access to centrally acting anti‑obesity drugs.
Farmakologická skupina
Přípravek patří do farmakoterapeutické skupiny A08AA, centrálně působící léčiva k terapii obezity, ATC kód: A081162 (bupropion a naltrexon). Základní informace o přípravku uvádíme podle Souhrnu údajů o přípravku [1].
Léková forma
Naltrexon/bupropion (Mysimba) je k dispozici ve formě tablety s prodlouženým uvolňováním (8 mg/90 mg). Jedna tableta obsahuje naltrexoni hydrochloridum 8 mg, což odpovídá naltrexonum 7,2 mg, a bupropioni hydrochloridum 90 mg, což odpovídá bupropionum 78 mg. Jedná se o modrou, bikonvexní, kulatou tabletu o průměru 11,9 mm s vyraženým nápisem „NB 890“ na jedné straně.
Mechanismus účinku‚ farmakodynamika
Přesné neurochemické vlivy kom![OBR. 1 Mechanismus účinku kombinace naltrexon/bupropion na snížení tělesné hmotnosti; podle [2] – Christou, et al., 2015. α‑Msh – hormon stimulující alfa melanocyty, alpha-melanocyte stimulating hormone; MC4r – receptor pro melanokortin 4, melanocortin- 4 receptor; Mop‑r – μ-opioidní receptor, μ-opioid receptor; poMC – proopiomelanokortin, proopiomelanocortin](https://www.remedia.cz/photo-a-31077---.jpg) binace
naltrexon/bupropion potlačující chuť k jídlu nebyly
do detailu objasněny, její předpokládaný mechanismus účinku
ilustruje obrázek 1.
Léčivý přípravek má dvě složky: naltrexon, μ opioidního
antagonistu, a bupropion, slabý inhibitor neuronálního
zpětného vychytávání noradrenalinu a dopaminu. Uvedené
složky ovlivňují dvě hlavní oblasti mozku, konkrétně nucleus
arcuatus hypothalami
a dopaminergní mezolimbický systém odměny. Bupropion řídí
v nucleus arcuatus
hypothalami neurony proopiomelanokortinu
(proopiomelanocortin, POMC), které uvolňují hormon stimulující
alfa melanocyty (alpha melanocyte stimulating hormone, α MSH)
působící na receptory melanokortinu 4. Pokud se vyplaví
α MSH, neurony POMC zároveň uvolňují beta endorfin,
endogenního agonistu μ opioidních receptorů. Vazba beta
endorfinu na μ opioidní receptory v neuronech POMC
zprostředkovává negativní zpětnovazební smyčku k těmto
neuronům, což vede k poklesu vyplavování α MSH.
Blokování uvedené inhibiční zpětnovazební smyčky naltrexonem
je navrženo k usnadnění silnější a déletrvající
aktivace neuronů POMC a tím ke zvýšení účinku
bupropionu na energetickou rovnováhu. Předklinické údaje
naznačují, že naltrexon a bupropion mohou mít při souběžném
podání v této oblasti více než aditivní účinky
na snížení příjmu potravy.
binace
naltrexon/bupropion potlačující chuť k jídlu nebyly
do detailu objasněny, její předpokládaný mechanismus účinku
ilustruje obrázek 1.
Léčivý přípravek má dvě složky: naltrexon, μ opioidního
antagonistu, a bupropion, slabý inhibitor neuronálního
zpětného vychytávání noradrenalinu a dopaminu. Uvedené
složky ovlivňují dvě hlavní oblasti mozku, konkrétně nucleus
arcuatus hypothalami
a dopaminergní mezolimbický systém odměny. Bupropion řídí
v nucleus arcuatus
hypothalami neurony proopiomelanokortinu
(proopiomelanocortin, POMC), které uvolňují hormon stimulující
alfa melanocyty (alpha melanocyte stimulating hormone, α MSH)
působící na receptory melanokortinu 4. Pokud se vyplaví
α MSH, neurony POMC zároveň uvolňují beta endorfin,
endogenního agonistu μ opioidních receptorů. Vazba beta
endorfinu na μ opioidní receptory v neuronech POMC
zprostředkovává negativní zpětnovazební smyčku k těmto
neuronům, což vede k poklesu vyplavování α MSH.
Blokování uvedené inhibiční zpětnovazební smyčky naltrexonem
je navrženo k usnadnění silnější a déletrvající
aktivace neuronů POMC a tím ke zvýšení účinku
bupropionu na energetickou rovnováhu. Předklinické údaje
naznačují, že naltrexon a bupropion mohou mít při souběžném
podání v této oblasti více než aditivní účinky
na snížení příjmu potravy.
Farmakokinetické vlastnosti
Výsledky studie relativní biologické dostupnosti s jednorázovou dávkou přípravku u zdravých jedinců prokázaly, že kombinované tablety jsou bioekvivalentní tabletám naltrexonu s okamžitým uvolňováním (IR) nebo bupropionu s prodlouženým uvolňováním (ER) podávaným jako samostatné látky.
V návaznosti na jednorázové perorální užití kombinovaných tablet naltrexon/bupropion zdravými osobami bylo dosaženo vrcholové koncentrace (cmax) naltrexonu a bupropionu přibližně dvě, resp. tři hodiny po podání. Na základě měření plochy pod křivkou sérové koncentrace (AUC) nebyly zjištěny žádné rozdíly v biologické dostupnosti naltrexonu nebo bupropionu při podání v kombinaci ve srovnání se samostatným podáním obou látek. Avšak vzhledem k prodlouženému charakteru uvolňování léčiva v případě kombinace byla výrazně snížena hodnota maximální plazmatické koncentrace pro naltrexon ve srovnání s 50 mg naltrexon hydrochloridu IR podávaného samostatně (přibližně dvojnásobný rozdíl po úpravě dávky). Hodnota cmax bupropionu v kombinaci naltrexon/bupropion (180 mg bupropion hydrochloridu) byla ekvivalentní hodnotě cmax bupropionu ER (150 mg bupropion hydrochloridu), což ukazuje, že hodnota cmax bupropionu dosažená léčbou kombinací naltrexon/bupropion (360 mg bupropion hydrochloridu denně) je srovnatelná s hodnotou dosaženou za použití komerčně dostupného bupropionu ER (300 mg bupropion hydrochloridu denně) podaného samostatně.
Naltrexon a bupropion jsou dobře absorbovány z gastrointestinálního traktu (z více než 90 %), avšak naltrexon má významný efekt prvního průchodu játry, a tedy omezenou systémovou biologickou dostupnost s pouze 5–6 % dosahujícími systémové cirkulace. Pokud byla kombinace naltrexon/bupropion podávána s vysoce tučným jídlem, hodnoty AUC a cmax pro naltrexon se zvýšily 2,1násobně, resp. 3,7násobně, a hodnoty AUC a cmax pro bupropion 1,4násobně, resp. 1,8násobně.
Vazba na plazmatické bílkoviny není u naltrexonu (21 %) ani u bupropionu (84 %) rozsáhlá, což ukazuje nízký potenciál pro lékové interakce při vytěsňování. V návaznosti na jednorázové perorální podání kombinovaných tablet naltrexon/bupropion zdravým jedincům byl průměrný eliminační poločas (t½) přibližně 5 hodin pro naltrexon a 21 hodin pro bupropion.
Hlavní metabolit naltrexonu představuje 6 beta naltrexol. Ačkoliv je méně účinný než naltrexon, eliminuje se pomaleji, a proto cirkuluje v mnohem vyšších koncentracích. Naltrexon a 6 beta naltrexol nejsou metabolizovány enzymy cytochromu P450 a studie in vitro neukazují na existenci možné inhibice nebo indukce důležitých izoenzymů. Naltrexon je primárně metabolizován na 6 beta naltrexol pomocí dihydrodiol dehydrogenáz.
Naltrexon a jeho metabolity jsou vylučovány především ledvinami (37‒60 % dávky). Odvozená hodnota pro renální exkreci naltrexonu po perorálním podání upravená pro vazbu plazmatické bílkoviny je 89 ml/min. Enzym odpovědný za hlavní cestu eliminace není znám. Vylučování stolicí je vedlejší eliminační cestou.
Bupropion je z velké části metabolizován na tři aktivní metabolity: hydroxybupropion, treohydroxybupropion a erytrohydroxybupropion. Tyto metabolity mají delší eliminační poločasy než bupropion a akumulují se ve větší míře. Nálezy in vitro naznačují, že CYP2B6 je hlavním izoenzymem podílejícím se na tvorbě hydroxybupropionu, zatímco podíl CYP1A2, 2A6, 2C9, 3A4 a 2E1 je výrazně nižší. Naproti tomu tvorba treohydroxybupropionu byla v odborné literatuře popsána jako zprostředkovaná 11 beta hydroxysteroid dehydrogenázou.
V případě cirhózy je
systémová expozice významně vyšší u bupropionu a jeho
metabolitů (dvoj až trojnásobně) a naltrexonu (až
10násobně) u pacientů vykazujících středně těžké až
těžké poškození jater. Naltrexon/bupropion je proto
kontraindikován u nemocných s těžkou poruchou funkce
jater a jeho podávání se nedoporučuje u osob s mírnou
až středně těžkou poruchou funkce jater. Na základě
informací z publikované literatury je systémová expozice
rovněž významně vyšší u obou složek kombinace a jejich
metabolitů u pacientů se středně těžkým až těžkým
poškozením ledvin. Naltrexon/bupropion je kontraindikován
u nemocných s terminálním selháním ledvin nebo
s těžkou poruchou funkce ledvin a jeho podávání není
doporučeno u osob se středně těžkým poškozením ledvin.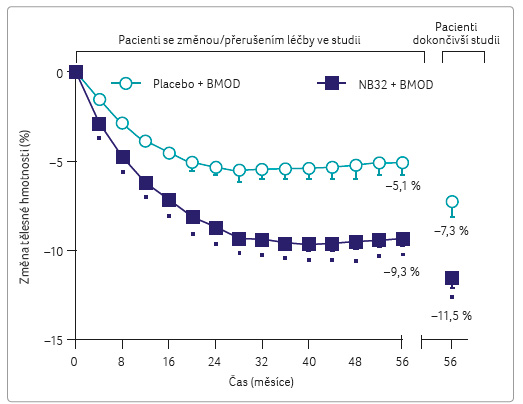
Klinická účinnost a bezpečnost
Účinky kombinace naltrexon/bupropion
na pokles tělesné hmotnosti, její udržení, obvod pasu,
stavbu těla, na markery kardiovaskulárních a metabolických
parametrů souvisejících s obezitou a na pacientem
hlášená hodnocení byly zkoumány ve dvojitě zaslepených
studiích kontrolovaných placebem (rozmezí BMI 27–45 kg/m2).
Z množství provedených sledování, jež shrnuje graf 1
a tabulka 1,
ukazuje například studie Waddena a kol. [3] až 9% pokles
hodnoty glykovaného hemoglobinu (HbA1c) v průběhu
ročního podávání kombinace naltrexon/bupropion. Pokles tělesné
hmotnosti byl zaznamenán v průměrné hodnotě 5 % za rok.
Randomizovaná zaslep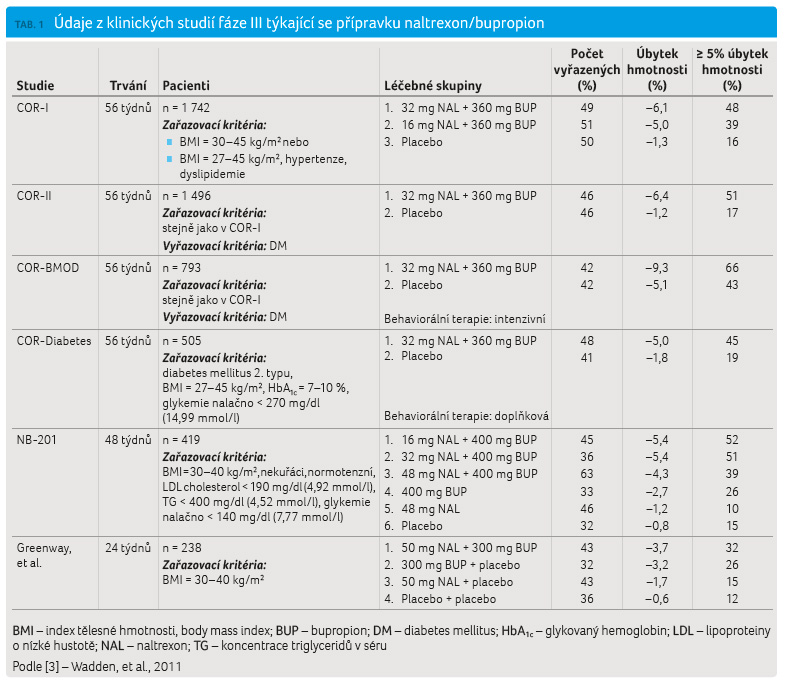 ená kardiovaskulární studie [4] zahrnovala
4 544 pacientů, jimž bylo podáváno placebo, a 4 456
pacientů, kteří dostávali naltrexon v dávce 32 mg denně
a bupropion v dávce 360 mg denně. Poměrně vysoký byl průměrný věk pacientů (61 let), 32,1 % mělo anamnézu
kardiovaskulárního onemocnění, 85 % bylo diabetiků, průměrný
BMI byl 36,6 kg/m2. Zjištěná redukce rizika byla
v průběhu léčby antiobezitikem signifikantní ‒ HR (hazard
ratio, poměr rizik) = 0,59, resp. 0,89 po dosažení
25 %, resp. 50 % předpokládaného počtu kardiovaskulárních
příhod. Autoři uzavírají tím, že bude třeba upřesnění
prostřednictvím dalších sledování, protože ve studii
nebylo dosaženo původně uvažovaného počtu příhod.
ená kardiovaskulární studie [4] zahrnovala
4 544 pacientů, jimž bylo podáváno placebo, a 4 456
pacientů, kteří dostávali naltrexon v dávce 32 mg denně
a bupropion v dávce 360 mg denně. Poměrně vysoký byl průměrný věk pacientů (61 let), 32,1 % mělo anamnézu
kardiovaskulárního onemocnění, 85 % bylo diabetiků, průměrný
BMI byl 36,6 kg/m2. Zjištěná redukce rizika byla
v průběhu léčby antiobezitikem signifikantní ‒ HR (hazard
ratio, poměr rizik) = 0,59, resp. 0,89 po dosažení
25 %, resp. 50 % předpokládaného počtu kardiovaskulárních
příhod. Autoři uzavírají tím, že bude třeba upřesnění
prostřednictvím dalších sledování, protože ve studii
nebylo dosaženo původně uvažovaného počtu příhod.
Účinek u pacientů s diabetem
Hollanderova studie, která byla publikovaná v časopise Diabetes Care [5], hodnotila podání 32 mg naltrexonu IR a 360 mg bupropionu ER u obézních pacientů a pacientů s nadváhou trpících diabetem 2. typu s podáním i bez podání perorálních antidiabetik. Během 56 týdnů v zaslepené, placebem kontrolované studii zahrnující 505 pacientů klesla tělesná hmotnost v průměru o 5 % a hodnota HbA1c o 0,6 %.
Účinek u pacientů s metabolickým syndromem
V další studii [6] byl podrobně
zkoumán vliv na složky metabolického syndromu a další
rizikové faktory aterosklerózy. Ve sledování došlo
k poklesu hmotnosti až o 8 % a byl zaznamenán
velmi komplexní účinek v případě metabolického syndromu
i aterosklerózy: BMI, obvod pasu, koncentrace triglyceridů,
koncentrace HDL i LDL cholesterolu, hodnota C reaktivního
proteinu, výše inzulinemie, citlivost na inzulin hodnocená
indexem HOMA a krevní tlak. V tabulce 2 shrnujeme signifikantní vliv na tyto faktory
u nediabetiků a diabetiků [5,6]. Výrazný efekt je
přítomen u obou skupin pacientů, přičemž u diabetiků
převažuje účinek na kompenzaci diabetu, koncentraci
triglyceridů a HDL cholesterolu, u nediabetiků pak účinek
na krevní tlak, lipidy a inzulinovou senzitivitu.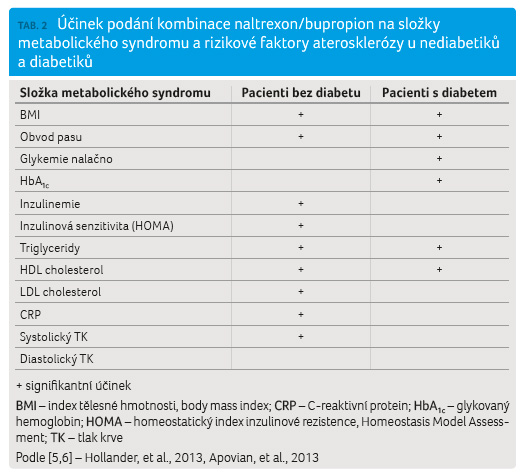
Kontraindikace podání
Léčivý přípravek má oproti jiným antiobezitikům odlišné kontraindikace:
- hypersenzitivita na léčivé látky nebo na kteroukoliv pomocnou látku;
- pacienti s nekontrolovanou hypertenzí;
- pacienti s aktuálním záchvatovitým onemocněním nebo s epileptickými záchvaty v anamnéze;
- pacienti se známým nádorem centrální nervové soustavy;
- pacienti podstupující akutní ukončení konzumace alkoholu nebo ukončení podávání benzodiazepinů;
- pacienti s anamnézou bipolární poruchy;
- pacienti užívající souběžnou léčbu obsahující bupropion nebo naltrexon;
- pacienti se současnou nebo předchozí diagnózou bulimie nebo mentální anorexie;
- pacienti aktuálně závislí na chronicky podávaných opioidech, opioidních agonistech (např. metadonu) nebo pacienti s akutním ukončením podávání opioidů;
- pacienti současně užívající inhibitory monoaminooxidázy (IMAO) ‒ mezi ukončením podávání IMAO a zahájením léčby kombinací naltrexon/bupropion by mělo uplynout minimálně 14 dnů;
- pacienti s těžkou poruchou funkce jater;
- pacienti s terminálním selháním ledvin nebo s těžkou poruchou funkce ledvin.
Závěr
V současné době se významně rozšiřuje spektrum podávaných antiobezitik o kombinaci naltrexon/bupropion. Obě léčiva se vzájemně potencují a jejich podání signifikantně snižuje tělesnou hmotnost i hodnotu HbA1c u diabetiků. Dostává se nám tak k terapeutickému použití nové antiobezitikum, které svým účinkem výrazně překonává všechna dříve podávaná centrální antiobezitika [7]. Zůstává otázkou, zda tento léčivý přípravek zaznamená stejné úspěchy jako antiobezitika užívaná ve Spojených státech amerických, ale v Evropě zatím nepovolená [8].
Seznam použité literatury
- [1] SPC Mysimba, Státní ústav pro kontrolu léčiv: Databáze léků [online]. Dostupné na: http://www.sukl.cz/modules/medication/detail.php?kod=0210388
- [2] Christou GA, Kiortsis DN. The efficacy and safety of the naltrexone/bupropion combination for the treatment of obesity: an update. Hormones (Athens) 2015; 14: 370–375.
- [3] Wadden TA, Foreyt JP, Foster GD, et al. Weight loss with naltrexone SR/bupropion SR combination therapy as an adjunct to behavior modification: the COR‑BMOD trial. Obesity (Silver Spring) 2011; 19: 110–120.
- [4] Nissen SE, Wolski KE, Prcela L, et al. Effect of Naltrexone‑Bupropion on Major Adverse Cardiovascular Events in Overweight and Obese Patients With Cardiovascular Risk Factors: A Randomized Clinical Trial. JAMA 2016; 315: 990–1004. doi:10.1001/jama.2016.1558
- [5] Hollander P, Gupta AK, Plodkowski R, et al.; COR‑Diabetes Study Group. Effects of naltrexone sustained‑release/bupropion sustained‑release combination therapy on body weight and glycemic parameters in overweight and obese patients with type 2 diabetes. Diabetes Care 2013; 36: 4022–4029.
- [6] Apovian CM, Aronne L, Rubino D, et al.; COR‑II Study Group. A randomized, phase 3 trial of naltrexone SR/bupropion SR on weight and obesity‑related risk factors (COR‑II). Obesity (Silver Spring) 2013; 21: 935–943.
- [7] Svačina Š. Minulost a současnost centrálně působících antiobezitik. Medicína po promoci 2016; 17: 265–268.
- [8] Svačina Š. Antidiabetika. Praha: Axonite, 2016.