Mobilní aplikace v revmatologické praxi a co vše hodnotit u psoriatické artritidy
Na letošních Zimních revmatologických dnech zazněla v rámci sympozia společnosti Novartis přednáška MUDr. Heřmana Manna cílená na význam mobilních aplikací v praxi revmatologů. Využití nových technologií zahrnula do následující prezentace také MUDr. Leona Procházková, která účastníky seznámila s tím, co vše by měl revmatolog hodnotit u pacientů postižených psoriatickou artritidou a z jakých důvodů. Předsednictví odborného sympozia se ujali prof. MUDr. Pavel Horák, CSc., a MUDr. Procházková.
Mobilní aplikace v revmatologické praxi
V úvodu své přednášky zavzpomínal MUDr. Heřman Mann, Ph.D., (Revmatologický ústav, Praha) na devadesátá léta minulého století, v jejichž závěru byla pro lékaře dostupná aplikace Epocrates s databází léčiv a přehledem lékových interakcí. Dnes je k dispozici řada typů mobilních aplikací, které fungují v operačním systému Android i iOS. Tyto aplikace mohou sloužit pro edukaci pacientů (např. Arthritis ID) nebo pro revmatology jako klinické nástroje, jež zahrnují referenční informace, diagnostické nástroje nebo nástroje pro hodnocení aktivity onemocnění. Právě na tyto aplikace se zaměřila prezentace primáře Manna.
Kromě nich se lze setkat rovněž s aplikacemi cílenými na selfmanagement pacientů, kteří s jejich pomocí zaznamenávají bolest, aktivitu onemocnění, kvalitu spánku, náladu, užívání léků atp. Jedná se o aplikace, které generují velké množství obtížně zpracovatelných dat, a pacienti proto s nimi obvykle po čase přestanou pracovat. Dále existují aplikace určené k pasivní monitoraci (např. GPS, akcelerometr atd.), aplikace pro monitoraci různých nemocí, pro revmatická onemocnění však zatím nejsou k dispozici. Využívat je možné tzv. gamifikace, které zahrnují pravidla hry, soutěže o body aj. a pomáhají dozvědět se víc informací o nemoci nebo s ní lépe bojovat (opět prozatím nezahrnují revmatické choroby). Velmi populární stále zůstává telemedicína, která umožňuje pacientům komunikovat se zdravotníky a lékaři, je zde ale velký problém s ochranou osobních dat [1].
Aplikace jako klinické nástroje pro revmatology
První aplikací, kterou mohou využívat revmatologové, je EULAR (European Alliance of Associations for Rheumatology). Tato aplikace v angličtině obsahuje pouze texty – všechna doporučení EULAR, jejich zjednodušené verze pro pacienty, databáze ultrazvukových snímků, přehled nemocí. „Nástroj není příliš interaktivní, je to spíš knihovnička do kapsy. Výhodou aplikace je její automatická aktualizace,“ doplnil primář Mann.
Aplikace ACR (American College of Rheumatology), opět v angličtině, obsahuje doporučené postupy, klasifikační, diagnostická a terapeutická kritéria a samostatnou složku informací týkajících se onemocnění covid‑19. Doporučené postupy zde jsou dostupné nejen jako text, ale také jako algoritmy, je tedy možné hledat např. postup pro řešení konkrétní situace u revmatologických pacientů. Aplikace je zaměřena pouze na standardy ACR, které se odlišují od doporučených postupů EULAR i od českých guidelines České revmatologické společnosti.
 V České republice společnost Mediately nabízí dvě aplikace. Jednou z nich je RheumaHelper, bezplatná aplikace pro podporu rozhodování s více než 30 nástroji pro revmatology, vyvinutá ve spolupráci s mezinárodním týmem odborníků. Ve 120 zemích ji používá více než 2 000 revmatologů a má více než 90 000 užití měsíčně. RheumaHelper zahrnuje 23 sad klasifikačních kritérií (pro některá onemocnění je sad větší počet) a 13 skórovacích nástrojů (tab. 1). Aplikace je interaktivní, v českém jazyce. V ČR aplikaci podporuje společnost Novartis čtvrtým rokem, průměrný počet použití je 3 250 měsíčně, počet aktivních revmatologů je 180 za měsíc.
V České republice společnost Mediately nabízí dvě aplikace. Jednou z nich je RheumaHelper, bezplatná aplikace pro podporu rozhodování s více než 30 nástroji pro revmatology, vyvinutá ve spolupráci s mezinárodním týmem odborníků. Ve 120 zemích ji používá více než 2 000 revmatologů a má více než 90 000 užití měsíčně. RheumaHelper zahrnuje 23 sad klasifikačních kritérií (pro některá onemocnění je sad větší počet) a 13 skórovacích nástrojů (tab. 1). Aplikace je interaktivní, v českém jazyce. V ČR aplikaci podporuje společnost Novartis čtvrtým rokem, průměrný počet použití je 3 250 měsíčně, počet aktivních revmatologů je 180 za měsíc.
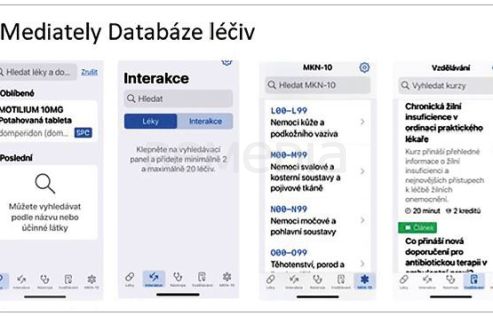 Dále je dostupná aplikace Mediately Databáze léčiv (obr. 1), kterou přednášející považuje za velmi užitečnou. Jejím obsahem jsou informace o všech léčivech, která jsou registrována v ČR, navíc má funkci lékových interakcí, kde lze zadat současně až 20 léků pro zjištění jejich vzájemného ovlivnění. Tato funkce je jedinou zpoplatněnou. Databáze léčiv obsahuje i důležitou databázi Mezinárodní klasifikace nemocí, která s výhodou umožňuje fulltextové vyhledávání. Aplikace zahrnuje rovněž určité vzdělávací moduly.
Dále je dostupná aplikace Mediately Databáze léčiv (obr. 1), kterou přednášející považuje za velmi užitečnou. Jejím obsahem jsou informace o všech léčivech, která jsou registrována v ČR, navíc má funkci lékových interakcí, kde lze zadat současně až 20 léků pro zjištění jejich vzájemného ovlivnění. Tato funkce je jedinou zpoplatněnou. Databáze léčiv obsahuje i důležitou databázi Mezinárodní klasifikace nemocí, která s výhodou umožňuje fulltextové vyhledávání. Aplikace zahrnuje rovněž určité vzdělávací moduly.
Jak mohou aplikace pomoci v praxi
Praktické využití mobilních aplikací ukázal primář Mann na kazuistice 37leté pacientky. Žena pracuje jako sekretářka, má nevýznamnou rodinnou anamnézu. Poslední čtyři roky trpí bolestmi kloubů, bolestmi zad, únavou, ranní ztuhlostí v trvání 45 minut. Nikdy u ní nebyla zjištěna psoriáza, uveitida ani střevní zánět, nemá artritidu, distance je v normě, byla u ní zaznamenána entezitida pravé Achillovy šlachy. Revmatoidní faktor (RF) a protilátky proti citrulinovaným peptidům (ACPA) byly u pacientky v normě, lidský leukocytární antigen B27 (HLA‑B27) pozitivní a hodnota C‑reaktivního proteinu (CRP) 3,2 mg/l. Na RTG zobrazení sakroiliakálního (SI) skloubení bylo zachyceno rozšíření kortikalis více vlevo, při vyšetření magnetickou rezonancí (MR) byla zjištěna pruhovitá sklerotická přestavba kyčelní kosti bilaterálně.
„Pokud využijeme jako pomocníka mobilní aplikaci, bude nás nejprve zajímat, zda jsou bolesti zad zánětlivé. Začaly před 40. rokem života plíživě, zmírňují se při pohybu, neustupují v klidu, přetrvávají v noci. To znamená, že si můžeme odpovědět kladně. Víme dále, že bolesti začaly ve věku před 35. rokem a jsou chronické, pacientka tedy splňuje kritéria pro axiální spondyloartritidu,“ vysvětlil přednášející. I když pomineme nález na MR, nemocná při pozitivitě HLA‑B27 splní klasifikační kritéria pro axiální spondyloartritidu (axSpA). Pacientka měla skóre BASDAI (Bath Ankylosing Spondylitis Disease Activity Index) 5,7, tedy vysoce aktivní chorobu, kdy je nutné zahájit razantní léčbu. Užívání nesteroidních antirevmatik (NSA) bylo u nemocné bez většího efektu. V té době bylo možno pacientku zařadit do klinického hodnocení s inhibitorem tumor nekrotizujícího faktoru (TNFi). V průběhu léčby došlo k odeznění entezitidy, ale pacientka hodnotila celkovou účinnost jako nedostatečnou a po šesti měsících léčbu ukončila. Po odslepení studie bylo zjištěno, že pacientka dostávala aktivní léčbu.
Žena pravidelně cvičí, hodnotu CRP má dlouhodobě v normě, na RTG páteře nebyla odhalena žádná progrese. Stále však trpí bolestmi zad a kloubů, únavou, navíc chronickou bolestí v podbřišku, která byla extenzivně vyšetřena, avšak bez zjištění příčiny. „Po delším kontaktu s nemocnou jsme konstatovali podezření na fibromyalgii (FM). Pacientka skutečně splňuje kritéria pro toto onemocnění, jehož výskyt při axSpA není nic vzácného,“ uvedl primář Mann. Pacienti, kteří mají axSpA s FM/bez FM, se neliší podle věku, zánětlivých markerů ani podle výskytu mimokloubních projevů, nicméně jsou to častěji ženy (v poměru s FM 3 : 2, bez FM 1 : 3) a jsou častěji HLA‑B27 negativní (přítomnost FM pozitivity 45,1 %, absence FM pozitivity 65,6 %). Nemocní s FM mají významně vyšší skóre BASDAI, BASFI (Bath Ankylosing Spondylitis Functional Index) a ASQoL (Ankylosing Spondylitis Quality of Life). Metaanalýza z roku 2022 uvádí, že prevalence FM u axSpA se podle toho, která kritéria jsou pro FM užita, pohybuje mezi 15–30 % [2]. Jiná metaanalýza (2020) sledovala pacienty s axSpA a FM podle toho, která splňují kritéria – u nemocných s axSpA byla prevalence relativně nízká [3]. Tato analýza mimo jiné ukázala, že prevalence FM je vyšší u pacientů, kteří splňují kritéria pro radiografickou axSpA, mají nález na MR nebo RTG, a že pozitivita HLA‑B27 je spojena s nižší prevalencí FM.
Přednášející se v závěru vrátil k případu pacientky, u níž byla navíc odhalena hypotyreóza a úzkostná porucha a zahájena medikace levotyroxinem a venlafaxinem. Nemocná dál pravidelně cvičí, zkouší psychoterapii, cítí se o něco lépe, ale nemá zájem o žádné revmatologické léky, protože jí „stejně nepomáhají“. Hodnota CRP je u ní dlouhodobě v normě, RTG páteře bez patologických změn. V rámci poslední kontroly byla u pacientky diagnostikována onychomykóza a byla jí dermatologem doporučena léčba terbinafinem, který je spojen s rizikem hepatotoxicity. I zde bylo možné využít mobilní aplikaci, podle níž byla zjištěna potenciální léková interakce mezi terbinafinem a venlafaxinem, a léčbu terbinafinem tedy revmatolog pacientce nedoporučil.
Shrnutí
- Aplikace EULAR a ACR – užitečné, avšak omezené tím, co poskytují (přístup k aktuálním klasifikačním kritériím a doporučeným postupům), dostupné v angličtině.
- RheumaHelper – praktický nástroj pro diagnostiku a hodnocení aktivity onemocnění, v češtině.
- Mediately Databáze léčiv – seznam registrovaných přípravků včetně indikací a dávkování, kontrola lékových interakcí, Mezinárodní klasifikace nemocí s možností fulltextového vyhledávání, nástroje pro další klinické obory včetně vzdělávacího modulu.
Co vše hodnotit u pacientů s psoriatickou artritidou
„Psoriatická artritida představuje heterogenní onemocnění, je tedy nutné, aby se hodnocení týkalo všech projevů, které se u pacienta objevují,“ uvedla svoji prezentaci MUDr. Leona Procházková, Ph.D., (II. interní klinika FN u sv. Anny, Brno). Lékař by měl tedy hodnotit přítomnost konkrétních projevů nemoci u konkrétního pacienta v konkrétním čase a také přítomnost kombinace projevů. Otázka je, jak hodnotit, pokud je projevů více a je postiženo více domén. Máme k dispozici nástroje, které jsou schopny zhodnotit všechny projevy pacienta? Nebo máme hodnotit pouze to, co je důležitější? Potřebujeme vědět, čím konkrétně pacient trpí, abychom vybrali správnou léčbu. „Terapeutické přístupy mají větší či menší vliv na konkrétní projevy onemocnění a v neposlední řadě bychom měli cílit i na to, co je důležité z pohledu pacienta,“ zdůraznila přednášející. Další z faktorů, které hodnotíme, je aktivita nemoci. Pokud je choroba aktivní, vede k výraznější strukturální progresi, zhoršuje kvalitu života pacienta a přetrvávající aktivita onemocnění je důvodem pro úpravu či změnu terapie.
 Uvedené postupy jsou součástí managementu terapie psoriatické artritidy (PsA) a byly prezentovány v loňském roce na kongresu EULAR (tab. 2) [4]. Z doporučení vyplývá nutnost sdíleného rozhodování o terapii mezi revmatologem a pacientem, respekt k preferencím nemocného, hodnocení klinicky významných muskuloskeletálních a rovněž extraskeletálních projevů asociovaných s PsA. Je třeba věnovat pozornost jednotlivým nejvýznamnějším projevům onemocnění.
Uvedené postupy jsou součástí managementu terapie psoriatické artritidy (PsA) a byly prezentovány v loňském roce na kongresu EULAR (tab. 2) [4]. Z doporučení vyplývá nutnost sdíleného rozhodování o terapii mezi revmatologem a pacientem, respekt k preferencím nemocného, hodnocení klinicky významných muskuloskeletálních a rovněž extraskeletálních projevů asociovaných s PsA. Je třeba věnovat pozornost jednotlivým nejvýznamnějším projevům onemocnění.
Kazuistika – první část
Také MUDr. Procházková demonstrovala uvedené postupy na konkrétním případu. Pětatřicetiletý muž s PsA pracuje jako prodejce nábytku, má typické projevy onemocnění, je obézní, má metabolický syndrom, trpí depresemi a dlouhodobě vertebrogenním algickým syndromem, který pravděpodobně souvisí s mírnou skoliózou páteře. Psoriáza se u muže projevila v jeho 25 letech, postižení je zjevné všude na těle včetně nehtů. Na bolesti kolen a kotníků si pacient poprvé stěžoval v roce 2018, kdy byl vyšetřen na revmatologii, nebyla u něj zjištěna artritida. Pacient reportoval i bolesti zad, podstoupil RTG a MR SI skloubení, avšak nebylo potvrzeno, že bolesti jsou způsobeny PsA.
Nemocný je léčen topickou léčbou od roku 2013 dosud, dvakrát absolvoval terapii ultrafialovým zářením (PUVA), metotrexát v perorální formě (v maximální dávce do 15 mg) předepsaný dermatologem užíval v letech 2018–2019, ale příliš dobře jej netoleroval. Poté mu byla dermatology nabídnuta účast v klinické studii s biologickou léčbou. V prvním roce byla studie zaslepená, pacienti dostávali buď secukinumab, nebo inhibitor interleukinu (IL) 23, po roce terapie byli všichni účastníci převedeni do otevřené fáze s podáváním inhibitoru IL‑23. Zpětný popis efektu terapie v rámci klinického hodnocení doložil, že u pacienta došlo na počátku sledování velmi rychle ke zmírnění kožního nálezu, popisoval i pozvolný ústup kloubních bolestí. Po přechodu do otevřené fáze se u něj během čtyř měsíců objevily bolesti a otoky kloubů, mírně se zhoršila psoriáza a byl odeslán na revmatologii.
V této době – leden 2021 – už byla diagnóza PsA potvrzena, muž trpěl artritidou kotníků a metatarzofalangeálních (MTP) skloubení, daktylitidou na dolních končetinách, entezitidou plantární fascie. Měl čtyři oteklé a pět bolestivých kloubů, mírnou elevaci hodnot zánětlivých parametrů, HLA‑B27 antigen byl negativní, bolest nemocný hodnotil na škále do deseti číslem 7, hodnocení celkové aktivity onemocnění bylo 6 z 10, se svým stavem byl velmi nespokojen. Skóre DAS 28 (Disease Activity Score‑28) ukazovalo nízkou aktivitu onemocnění, zatímco dle skóre DAPSA (Disease Activity in Psoriatic Arthritis), jehož použití je preferováno u nemocných s PsA, měl pacient střední aktivitu onemocnění. Kožní psoriáza byla dle skóre postižení plochy těla mírná – BSA (Body Surface Area) < 3 %.
Co hodnotíme použitými skórovacími systémy
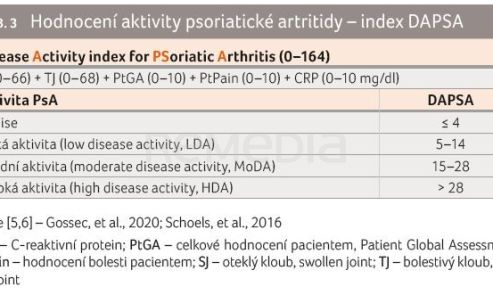 DAPSA představuje index použitelný v hodnocení PsA, sestává z počtu bolestivých a oteklých kloubů, hodnocení bolesti na desetibodové škále (Visual Analogue Scale, VAS), celkového hodnocení aktivity onemocnění pacientem a hodnoty CRP (v mg/dl), tabulka 3. Zjištěné hodnoty se sčítají dohromady [5,6]. Pro toto skórování lze použít aplikaci RheumaHelper, v níž se hodnota CRP zadává v běžnějších mg/l.
DAPSA představuje index použitelný v hodnocení PsA, sestává z počtu bolestivých a oteklých kloubů, hodnocení bolesti na desetibodové škále (Visual Analogue Scale, VAS), celkového hodnocení aktivity onemocnění pacientem a hodnoty CRP (v mg/dl), tabulka 3. Zjištěné hodnoty se sčítají dohromady [5,6]. Pro toto skórování lze použít aplikaci RheumaHelper, v níž se hodnota CRP zadává v běžnějších mg/l.
Proč je skóre DAPSA u pacientů s PsA vhodnější než DAS 28? „Představme si fiktivního pacienta v revmatologické ordinaci, který má distální interfalangeální (DIP) formu PsA – artritidu tří DIP kloubů na rukou, kotníků, čtyř MTP kloubů, dvou proximálních interfalangeálních (PIP) kloubů. Jedná se tedy zjevně o aktivní onemocnění, ale skóre potřebujeme jako doklad např. u pacientů léčených cílenou léčbou. Pokud bychom v tomto případě použili skóre DAS 28, bude podle výsledku pacient v remisi, pokud použijeme DAPSA, má pacient vysoce aktivní onemocnění. Index DAS 28 není v těchto případech vhodný, neboť nezahrnuje DIP klouby u PsA často postižené (obzvlášť v kombinaci s postižením nehtů) a nehodnotí klouby na dolních končetinách,“ vysvětlila MUDr. Procházková.
Mezi další možnosti hodnocení patří dosažení minimální aktivity onemocnění – skóre MDA (Minimal Disease Activity). Oproti DAPSA hodnotí index rovněž přítomnost postižení ostatních domén, jako jsou entezitidy, postižení kůže, a navíc obsahuje funkční dotazník HAQ (Health Assessment Questionnaire). Pro dosažení minimální aktivity onemocnění je třeba minimálně 5 z celkem 7 bodů. Pacient nesmí mít víc než jeden oteklý kloub, jeden bolestivý kloub, více než jedno postižení entezitidou, bolest hodnocená pomocí VAS musí mít hodnotu ≤ 1,5, celkové hodnocení aktivity nemoci pacientem ≤ 2, postižení kůže (BSA) ≤ 3 % a HAQ skóre ≤ 0,5 [5,6].
Je důležité vysvětlit, proč by měl revmatolog hodnotit také kožní postižení. Ve většině případů je to především kvůli indikačním kritériím, neboť určitá léčba může být u pacienta zahájena, jen pokud má středně těžkou nebo těžkou psoriázu. Při odeslání nemocného na příslušné vyšetření k dermatologovi by mohlo dojít k nežádoucímu zdržení. Určitou možností v rukou revmatologa je index BSA, podle něhož je mírná psoriáza hodnocena jako postižení plochy těla < 3 %, středně těžká psoriáza 3–10 %, těžká psoriáza > 10 %. Jedno procento plochy těla odpovídá ploše dlaně, avšak vždy hodnotíme podle plochy ruky pacienta, aby nedošlo ke zkreslení [7].
Index plochy a závažnosti postižení psoriázou (Psoriasis Area and Severity Index, PASI) patří skutečně spíše do rukou dermatologa. Hodnotí se nejen plocha těla postižená psoriázou, ale také např. závažnost erytému, zašupení, indurace kůže v konkrétních lokalitách [8].
Kazuistika – druhá část
Po selhání terapie IL‑23 v rámci klinického hodnocení jsme u pacienta zahájili znovu terapii metotrexátem, tentokrát v injekční podobě, kterou toleroval. Na kontrole po třech měsících však nebylo zaznamenáno zlepšení, došlo k další progresi nálezu, tentokrát včetně kožního zhoršení (4/2021) na středně závažnou psoriázu (BSA 5 %), s hodnotou DAPSA 45,6. Podle doporučení EULAR by měla být u takového pacienta zahájena cílená terapie [4], byl mu proto podáván TNFi. Krátce se projevil efekt této terapie, po 16 týdnech vedla k poklesu na nízkou aktivitu choroby (DAPSA 11,6), BSA 3 %. Účinnost však přetrvávala jen necelý rok, znovu byla zaznamenána artritida zápěstí, metakarpofalangeálního skloubení na rukou, kotníků, entezitida plantární fascie, psoriáza progredovala na BSA 6 % (ruce, nehty, kštice) a muže limitovala v zaměstnání. Po selhání terapie TNFi byl pro další léčbu vybrán inhibitor IL‑17A mimo jiné z důvodu mimokloubního postižení. Podle doporučení EULAR, která kladou při výběru terapie důraz na mimokloubní projevy, zvlášť při klinicky relevantním kožním postižení, jsou preferovány inhibitory IL‑17A, IL‑17A/F, IL‑12/23 nebo IL‑23. Klinicky relevantní neznamená pouze rozsah postižení kůže nebo celkové skóre PASI, ale také právě např. stav pacienta, který je viditelným onemocněním omezen v zaměstnání a sociálních kontaktech [4].
Od roku 2022 dosud je pacient léčen inhibitorem IL‑17A a s touto léčbou je velmi spokojen, nemá entezitidy, má vyhojenou pokožku a téměř vyhojené postižení nehtů, skóre DAPSA je 5,62. Pacient léčbu hodnotí jako velmi účinnou, reportoval i odeznění bolestí páteře. Pro secukinumab (inhibitor IL‑17, jímž je pacient léčen) byla potvrzena účinnost v případě periferní artritidy (studie FUTURE 2) a klinická účinnost srovnatelná s adalimumabem (studie EXCEED). Efekt léčby na periferní klouby byl u obou léků identický, při srovnání secukinumabu a adalimumabu u pacientů s psoriázou v rámci PsA byla blokáda IL‑17A účinnější v ovlivnění kožního postižení [9–11].
MAXIMISE byla jedinou randomizovanou klinickou studií, která hodnotila efekt inhibitoru IL‑17A u pacientů s psoriázou a axiálním postižením [12]. „Je tedy možné, že také u našeho pacienta byly bolesti zad součástí axiálního postižení, které nebylo odhaleno,“ doplnila MUDr. Procházková.
Shrnutí
- Psoriatická artritida je komplexní heterogenní onemocnění s velkým množstvím projevů, které se kombinují a mění v čase u konkrétního pacienta.
- Terapeutickou výzvou je kombinace postižení odlišných domén psoriatické nemoci.
- Při změně fenotypu v průběhu onemocnění volíme terapii dle aktuálního postižení.
- Hodnotíme přítomnost aktuálních projevů nemoci.
- Hodnotíme aktivitu všech projevů onemocnění – důležité je brát v úvahu, která z domén je pro pacienta nejvýznamnější.
„V minulosti jsme se jako revmatologové ptali, jak léčit psoriatickou artritidu, v současnosti už se ptáme, o jakou psoriatickou artritidu se jedná a kterou terapeutickou možnost pro pacienta zvolit,“ shrnula závěrem posun v léčbě tohoto komplikovaného onemocnění MUDr. Leona Procházková.
Redakčně zpracovala PhDr. Nikola Homolová Richtrová
Literatura
[1] Mollard E, Michaud K. Mobile apps for rheumatoid arthritis: Opportunities and challenges. Rheum Dis Clin North Am 2019; 45: 197–209.
[2] Son SM, Kim DS, Lee JS. Fibromyalgia in Axial Spondyloarthritis. A Meta‑analysis. J Clin Rheumatol 2022; 28: e222–e227.
[3] Jones GT, Mallawaarachchi B, Shim J, et al. The prevalence of fibromyalgia in axial spondyloarthritis. Rheumatol Int 2020; 40: 1581–1591.
[4] Gossec L. EULAR‑Recommendations on the management of PsA. Presented at: EULAR 2023 Congress; May 31 to June 3, 2023, Milan, Italy.
[5] Gossec L, Baraliakos X, Kerschbaumer A, et al. EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2019 update. Ann Rheum Dis 2020; 79: 700–712.
[6] Schoels MM, Aletaha D, Alasti F, Smolen JS. Disease activity in psoriatic arthritis (PsA): defining remission and treatment success using the DAPSA score. Ann Rheum Dis 2016; 75: 811–818.
[7] Rhodes J, Clay C, Phillips M. The surface area of the hand and the palm for estimating percentage of total body surface area: results of a meta‑analysis. Br J Dermatol 2013; 169: 76–84.
[8] Fredriksson T, Pettersson U. Severe psoriasis – oral therapy with a new retinoid. Dermatologica 1978; 157: 238–244.
[9] McInnes IB, Mease PJ, Kirkham B, et al. Secukinumab, a human anti‑interleukin‑17A monoclonal antibody, in patients with psoriatic arthritis (FUTURE 2): a randomised, double‑blind, placebo‑controlled, phase 3 trial. Lancet 2015; 386: 1137–1146.
[10] Gottlieb AB, Behrens F, Nash P, et al. Comparison of secukinumab versus adalimumab efficacy on skin outcomes in psoriatic arthritis: 52‑week results from the EXCEED study. Ann Rheum Dis 2020; 79: 763–764.
[11] Gottlieb AB, Merola JF, Reich K, et al. Efficacy of secukinumab and adalimumab in patients with psoriatic arthritis and concomitant moderate‑to‑severe plaque psoriasis: results from EXCEED, a randomized, double‑blind head‑to‑head monotherapy study. Br J Dermatol 2021; 185: 1124–1134.
[12] Baraliakos X, et al. Secukinumab in patients with psoriatic arthritis and axial manifestations: results from the double‑blind, randomised, phase 3 MAXIMISE trial. Ann Rheum Dis 2021; 80: 582–590.