Afatinib v klinické praxi Pacient s dobou přežití bez progrese onemocnění 18 měsíců a s vysokou kvalitou života
Souhrn:
Nemalobuněčný karcinom plic lokálně pokročilého a metastatického stadia je standardně, obvykle v závislosti na výkonnostním stavu pacienta a na komorbiditách, léčen systémově chemoterapií přípravky třetí generace spolu s platinovými deriváty. Preferovanou kombinací je v první linii léčby ade-nokarcinomů pemetrexed s cisplatinou s možností udržovací léčby pemetrexedem nebo platinový dublet s bevacizumabem, v pokračovací léčbě je podáván bevacizumab. Pro některé pacienty je možností již v první linii léčby podání tyrosinkinázových inhibitorů v případě pozitivní aktivační mutace genu EGFR (5–10 %) a nově také podání crizotinibu v případě translokace genu ALK (přibližně 5 %). Autor předkládá kasuistiku pacienta léčeného afatinibem v první linii léčby.
Key words: non-small cell lung cancer – EGFR positivity – first-line treatment.
Summary:
Standard therapy of locally advanced or metastatic non-small cell lung cancer consists of systemic chemotherapy using third-generation drugs plus platinum derivatives, depending on the patient’s performance status and comorbidities. In the first line of adenocarcinoma treatment, pemetrexed plus cisplatina are the preferred combination; pemetrexed or platinum doublet with bevacizumab may be used in maintenance therapy, continuation therapy consisting of bevacizumab application. Some patients – those with positive activating mutation of the EGFR gene (5–10%) – can be treated with tyrosine kinase inhibitors in the first line already; the same has recently become true for crizotinib application in cases with ALK gene translocation (about 5%). The author presents a case study of a patient undergoing first-line treatment with afatinib.
Průběh nemoci
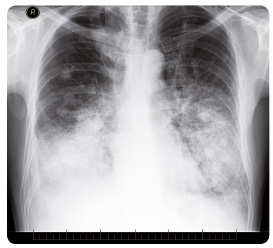 Pacient (ročník 1961) přichází s prvními příznaky nemoci do naší ambulance koncem května 2014 pro hmotnostní úbytek 7 kg za tři měsíce a s pocitem dušnosti provázeným suchým pokašláváním. Muž je jen příležitostným kuřákem, bez komorbidit, pracuje jako operátor na velíně. Na skiagramu hrudníku (obr. 1) nález hodnotíme jako nejspíše pokročilý tumor horního laloku pravé plíce. Na CT (computed tomography, počítačová tomografie) hrudníku a horní části břicha ze dne 22. května 2014 (obr. 2) nacházíme v S1/3 pravé plíce spikulovité ložisko o velikosti 43 mm × 39 mm × 47 mm – nejspíše primární bronchogenní karcinom. V plicích jsou přítomny difuzně oboustranně mnohočetné metastázy v rozsahu 5–30 mm, vpravo zhruba 19 mm, vlevo 30 mm, parahilózně a v dolních lalocích karcinomatózní
Pacient (ročník 1961) přichází s prvními příznaky nemoci do naší ambulance koncem května 2014 pro hmotnostní úbytek 7 kg za tři měsíce a s pocitem dušnosti provázeným suchým pokašláváním. Muž je jen příležitostným kuřákem, bez komorbidit, pracuje jako operátor na velíně. Na skiagramu hrudníku (obr. 1) nález hodnotíme jako nejspíše pokročilý tumor horního laloku pravé plíce. Na CT (computed tomography, počítačová tomografie) hrudníku a horní části břicha ze dne 22. května 2014 (obr. 2) nacházíme v S1/3 pravé plíce spikulovité ložisko o velikosti 43 mm × 39 mm × 47 mm – nejspíše primární bronchogenní karcinom. V plicích jsou přítomny difuzně oboustranně mnohočetné metastázy v rozsahu 5–30 mm, vpravo zhruba 19 mm, vlevo 30 mm, parahilózně a v dolních lalocích karcinomatózní 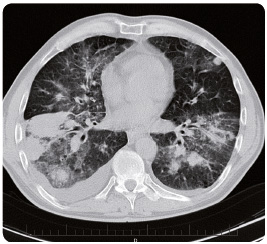 lymfangoitida. Fluidothorax vpravo je v šíři 27 mm, vlevo 4 mm. Dokumentovány jsou zvětšené lymfatické uzliny v okolí trachey a v aortopulmonálním okénku i v hilech bilaterálně. V oblasti jater se nacházejí hypodenzní ložiska o velikosti až 19 mm v největším průměru. Současně je popsáno ložisko metastázy ve štítné žláze, které ověřujeme ultrasonograficky a následně punkčně.
lymfangoitida. Fluidothorax vpravo je v šíři 27 mm, vlevo 4 mm. Dokumentovány jsou zvětšené lymfatické uzliny v okolí trachey a v aortopulmonálním okénku i v hilech bilaterálně. V oblasti jater se nacházejí hypodenzní ložiska o velikosti až 19 mm v největším průměru. Současně je popsáno ložisko metastázy ve štítné žláze, které ověřujeme ultrasonograficky a následně punkčně.
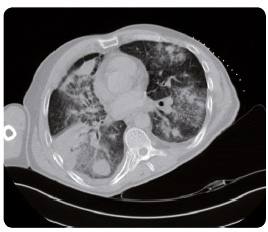 Dne 3. června 2014 byl u nemocného perthorakální punkcí ložiska levé plíce pod kontrolou CT diagnostikován primární plicní adenokarcinom acinárně mikropapilárního typu (obr. 3), dle klasifikace TNM (tumor‑node‑metastasis) je nemoc hodnocena jako T4N3M1b IV. stadia. Patologem jsou porovnány biopsie z plíce i z uzlu štítné žlázy, které se imunohistologicky shodují.
Dne 3. června 2014 byl u nemocného perthorakální punkcí ložiska levé plíce pod kontrolou CT diagnostikován primární plicní adenokarcinom acinárně mikropapilárního typu (obr. 3), dle klasifikace TNM (tumor‑node‑metastasis) je nemoc hodnocena jako T4N3M1b IV. stadia. Patologem jsou porovnány biopsie z plíce i z uzlu štítné žlázy, které se imunohistologicky shodují.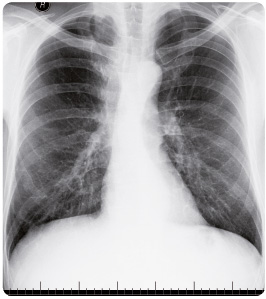
Výkonnostní status v úvodu nemoci byl i přes rozsah nemoci při mírné pozátěžové respirační insuficienci dobrý, na škále ECOG (Eastern Cooperative Oncology Group) byl hodnocen stupněm 1. Následným molekulárně genetickým vyšetřením ze dne 20. června 2014 dle konsensu byla zjištěna aktivační mutace kaskády receptoru pro epidermální růstový faktor (epidermal growth factor receptor, EGFR) v exonu 21 L858R, byla zjištěna i amplifikace genu EGFR, nebyla nalezena přestavba genu ALK ani ROS1. Diagnostický proces trval od 22. května 2014 do 17. června 2014. Léčba afatinibem v časném přístupu 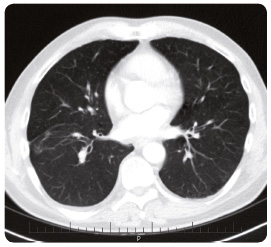 byla zahájena dne 20. června 2014, tedy méně než měsíc od odběru tkáně, a to dávkou 40 mg/den. Měsíc po zahájení léčby je nemocný bez kožních toxických reakcí a průjmů, dávku nemusíme snižovat. Při kontrole vyjde do 4. patra, je bez potíží, ještě pohublý, subjektivně výrazně zlepšen, což nám hlásil již při první telefonické kontrole po 14 dnech léčby dle protokolu časného přístupu. Pacient je dále pravidelně sledován v měsíčních intervalech laboratorně, klinicky a v šestitýdenních intervalech i CT vyšetřením a echokardiograficky. V dalším průběhu léčby je tedy dokumentována výrazně zlepšená kvalita života, pacient se cítí zdráv, sportuje, jezdí na kole, zřetelný je přírůstek tělesné hmotnosti a při kontrole zadopřední rtg projekcí hrudníku dne 10. června 2015 (obr. 4) a po kontrole pomocí CT dne 20. června 2015 (obr. 5) má dokonce zájem ukončit pracovní neschopnost a vrátit se na příští
byla zahájena dne 20. června 2014, tedy méně než měsíc od odběru tkáně, a to dávkou 40 mg/den. Měsíc po zahájení léčby je nemocný bez kožních toxických reakcí a průjmů, dávku nemusíme snižovat. Při kontrole vyjde do 4. patra, je bez potíží, ještě pohublý, subjektivně výrazně zlepšen, což nám hlásil již při první telefonické kontrole po 14 dnech léčby dle protokolu časného přístupu. Pacient je dále pravidelně sledován v měsíčních intervalech laboratorně, klinicky a v šestitýdenních intervalech i CT vyšetřením a echokardiograficky. V dalším průběhu léčby je tedy dokumentována výrazně zlepšená kvalita života, pacient se cítí zdráv, sportuje, jezdí na kole, zřetelný je přírůstek tělesné hmotnosti a při kontrole zadopřední rtg projekcí hrudníku dne 10. června 2015 (obr. 4) a po kontrole pomocí CT dne 20. června 2015 (obr. 5) má dokonce zájem ukončit pracovní neschopnost a vrátit se na příští 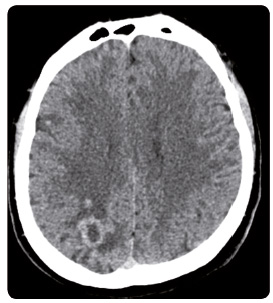 období do zaměstnání (obr. 3, 4). I při dalších hodnoceních pozorujeme dlouhodobou výraznou parciální regresi postižení plic, jater a štítné žlázy při zlepšení výkonnostního stavu na ECOG 0.
období do zaměstnání (obr. 3, 4). I při dalších hodnoceních pozorujeme dlouhodobou výraznou parciální regresi postižení plic, jater a štítné žlázy při zlepšení výkonnostního stavu na ECOG 0.
Bohužel, po 18 měsících léčby dochází dne 12. prosince 2015 k progresi nemoci, kdy na podkladě mnohočetných metastáz do mozku (obr. 6) je pacient přijat po dvou generalizovaných epileptických paroxysmech na neurologickou kliniku, je přítomna levostranná centrální hemiparéza s prevalencí postižení levé dolní končetiny. Po stabilizaci stavu probíhá radioterapie neurokrania od 16. prosince do 22. prosince 2015 v celkové dávce 20 Gy/5 fr. V lednu 2016 je přítomna ještě regredující levostranná centrální hemiparéza a dle kontrolního 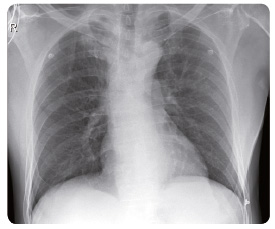 CT vyšetření mozku je popsáno zvýraznění edematózních změn po radioterapii. Nemocný je opět hospitalizován na neurologii, je zvýšeno dávkování antiedematózní léčby a stav se postupně upravuje v neurologicky prakticky normální nález. Vzhledem k výraznému celkovému zlepšení (obr. 7) projednáváme stav pacienta a předchozí léčbu s multidisciplinárním týmem Komplexního onkologického centra Fakultní nemocnice Ostrava a rozhodujeme o systémové léčbě druhé linie pemetrexedem s cisplatinou.
CT vyšetření mozku je popsáno zvýraznění edematózních změn po radioterapii. Nemocný je opět hospitalizován na neurologii, je zvýšeno dávkování antiedematózní léčby a stav se postupně upravuje v neurologicky prakticky normální nález. Vzhledem k výraznému celkovému zlepšení (obr. 7) projednáváme stav pacienta a předchozí léčbu s multidisciplinárním týmem Komplexního onkologického centra Fakultní nemocnice Ostrava a rozhodujeme o systémové léčbě druhé linie pemetrexedem s cisplatinou.
Aktuálně v dubnu 2016 byl pacient ve stabilizovaném stavu, ECOG 0–1 při léčbě druhé linie chemoterapie (nyní po třetím cyklu), i neurologicky stabilizován při podávání nízké dávky dexamethasonu 4 mg (Fortecortin 4) per os, bez dušnosti, bez kašle, bez bolestí, auskultačně dýchání fyziologické, s plánem kontrolního CT po ukončení čtvrtého cyklu chemoterapie na počátku května 2016.
Závěr
U našeho pacienta jsme pozorovali výrazný klinický přínos první linie cílené léčby, kterou představoval afatinib podávaný po dobu přežití bez progrese onemocnění (progression‑free survival, PFS). Samotný pacient i klinický lékař konstatují jako zásadní fakt zvláště významné zlepšení a dlouhodobé udržení kvality života v průběhu léčby první linie s minimálními nežádoucími účinky léčby.
Přes veškerou léčbu je prognóza lokálně pokročilých a metastatických stadií nemalobuněčného karcinomu plic (non‑small lung carcinoma, NSCLC) stále nepříznivá. Změnu v prodloužení celkového přežití a času do progrese onemocnění zaznamenáváme u nemocných, u kterých zjistíme již v době diagnózy nebo při progresi nemoci některou z citlivých mutací vhodných pro tzv. biologickou léčbu. V případě tohoto pacienta šlo o aktivační mutaci genu EGFR v exonu 21 L858R. Během celého průběhu první linie léčby nemoci afatinibem byla pozorována velmi dobrá kvalita života pacienta při výkonnostním stavu ECOG 0.
Fotografie v článku: archiv autora.