Erenumab oproti standardní profylaktické léčbě migrény pohledem aktuálních klinických hodnocení
Migréna patří mezi vysoce invalidizující onemocnění, přesto zůstává nedostatečně léčena. Terapeutické možnosti tohoto neurologického onemocnění se díky pochopení patofyziologických mechanismů v posledních desetiletích výrazně posunuly. K dispozici máme specifickou léčbu pro akutní ataky i preventivní terapii pro pacienty s častými záchvaty a nedostatečnou odpovědí na léčbu.
V případě profylaktické léčby byly dosud standardem sice perorálně (p.o.) podávané přípravky, nicméně s nespecifickým účinkem, které nebyly k ovlivnění migrény primárně určeny. Tyto léky přinášejí určité zlepšení, významný podíl pacientů s migrénou ale na tuto léčbu dostatečně neodpovídá nebo ji netoleruje a léčba bývá spojena s nízkou adherencí. Naději pacientům přineslo zavedení specifické profylaktické antimigrenózní léčby cílící na CGRP (calcitonin gene‑related peptide).
Erenumab je plně humánní monoklonální protilátka namířená proti receptoru pro CGRP, do klinické praxe byl zaveden v roce 2018. Účinnost a bezpečnost erenumabu u pacientů s epizodickou (EM) i chronickou migrénou (CM) demonstrovala klinická hodnocení [6–11]. Recentní studie se zaměřily na: přímé srovnání erenumabu s topiramátem (studie HER‑MES) [7], který představuje dle mezinárodních doporučení jedno z preferovaných léčiv první linie profylaktické terapie; efekt léčby erenumabem u pacientů po selhání 1–2 dosud standardně podávaných preventivních terapií (studie APPRAISE) [8] a účinek erenumabu u obtížně léčitelných pacientů, u nichž předcházelo podávání 2–4 profylaktik (studie LIBERTY) [9,10].
Studie HER‑MES
Studie HER‑MES je prvním head‑to‑head srovnáním léčby cílící na dráhu CGRP a standardní profylaktické antimigrenózní léčby. Jednalo se o 24týdenní randomizovanou, dvojitě zaslepenou kontrolovanou studii, která se uskutečnila na 82 pracovištích v Německu [7]. Do klinického hodnocení mohli být zařazeni pacienti s EM v posledních třech měsících, tj. s počtem dnů s migrénou v měsíci (monthly migraine days, MMD) v rozmezí 4–14. S cílem zahrnout celou populaci migreniků mohli být na základě dodatku k protokolu zařazeni i pacienti s CM. Způsobilí pro zařazení byli pacienti tzv. naivní (bez předchozí preventivní léčby) nebo pacienti se selháním až tří profylakticky podávaných léčiv (metoprolol/propranolol, amitriptylin, flunarizin), a to z důvodu nedostatečné účinnosti nebo nesnášenlivosti.
Pacienti byli randomizováni v poměru 1 : 1 k aplikaci 70 mg nebo 140 mg erenumabu subkutánně (s.c.) 1× měsíčně (a placeba topiramátu) nebo k podávání topiramátu p.o. v individuální dávce (50–100 mg/den) dle účinnosti (a placeba erenumabu). Hodnocení zahrnovalo úvodní šestitýdenní titrační fázi léčby (postupná titrace dávky topiramátu s navýšením o 25 mg/týden či pomaleji dle potřeby pacienta s cílem dosáhnout denní dávky 100 mg) a dále udržovací fázi s kontrolami v týdnech 8, 12, 16, 20 a 24.
Primárním cílovým ukazatelem bylo přerušení léčby pro nežádoucí účinky během dvojitě zaslepené fáze. Důvod přerušení léčby byl u každého pacienta zaznamenán. Sekundárním cílovým ukazatelem byl podíl pacientů, kteří dosáhli alespoň 50% snížení MMD oproti výchozí hodnotě během posledních tří měsíců dvojitě zaslepené fáze.
Do studie bylo zařazeno 777 pacientů, charakteristiky nemocných byly mezi skupinami vyvážené. Sledování dokončilo 95,1 % pacientů. Redukce dávky nebyla v žádné ze skupin povolena.
Na počátku sledování činil průměrný MMD 10,4. Anamnézu preventivní antimigrenózní léčby nemělo 59,4 % pacientů. Léčba 70 mg erenumabu byla zahájena u 73,5 % pacientů, u 42,5 % byla během 24týdenního sledování navýšena na 140 mg. Průměrná dávka topiramátu během sledování byla 92,1 mg/den. Ve skupině s erenumabem vysadilo medikaci z důvodu nežádoucích účinků 10,6 % pacientů ve srovnání s 38,9 % ve skupině s topiramátem (poměr šancí [odds ratio, OR] 0,19; 95% interval spolehlivosti [confidence interval, CI] 0,13–0,27; p < 0,001), graf 1.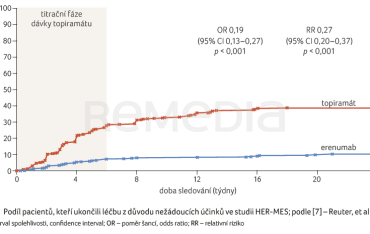
Výrazně více pacientů dosáhlo alespoň 50% snížení MMD oproti výchozímu stavu ve skupině s erenumabem (55,4 % vs. 31,2 %; OR 2,76; 95% CI 2,06–3,71; p < 0,001). U pacientů ve skupině s erenumabem navíc došlo k výraznější změně v hodnocení kvality života pomocí dotazníků HIT‑6 (Headache Impact Test) a SF‑36v2 (Quality of Life Questionnaire), a to jak ve fyzické, tak v psychické komponentě.
Z hlediska bezpečnosti léčby nebyly zaznamenány žádné nové bezpečnostní signály. Více nežádoucích účinků bylo zachyceno ve skupině s topiramátem (81,2 % vs. 55,4 %). Mezi nejčastější nežádoucí účinky ve skupině s topiramátem, které vedly k ukončení léčby, patřily parestezie, poruchy pozornosti, únava a nauzea. Jedná se o typické účinky popisované u topiramátu. Ve skupině s erenumabem to byly únava, nauzea, poruchy pozornosti a závratě s frekvencí výskytu srovnatelnou s placebem [7].
Studie APPRAISE
APPRAISE je prospektivní randomizovaná otevřená studie fáze IV, která probíhala ve 100 centrech 17 zemí [8]. Toto 12měsíční klinické hodnocení si dalo za cíl porovnat setrvalý přínos erenumabu oproti standardní perorální preventivní léčbě u pacientů s EM.
Do studie byli zahrnuti dospělí pacienti od 18 let (n = 621) s EM, u nichž selhala jedna nebo dvě předchozí profylaktické antimigrenózní léčby kvůli nedostatečné účinnosti a/nebo nesnášenlivosti léčby. Pacienti byli randomizováni v poměru 2 : 1 k s.c. aplikaci erenumabu (70 mg nebo 140 mg) 1× měsíčně nebo k dennímu perorálnímu podávání standardní profylaktické léčby. Během sledování byla povolena změna dávky erenumabu nebo změna perorální profylaxe. Primárním složeným cílovým ukazatelem byl podíl pacientů, kteří dokončili přidělenou léčbu a dosáhli ≥ 50% snížení MMD ve 12. měsíci oproti výchozí hodnotě. Sekundárními cílovými ukazateli byly změna kumulativního průměru MMD od výchozí hodnoty u pacientů s původně přidělenou léčbou; podíl pacientů, kteří dokončili studii s původně přidělenou léčbou a hodnocení změny klinického stavu pacientem od výchozí hodnoty měřené pomocí škály PGIC (Patient Global Impression of Change) ve 12. měsíci na původně přidělené léčbě.
Signifikantně vyšší podíl pacientů zůstal na původně přidělené léčbě a dosáhl ≥ 50% snížení MMD ve srovnání s výchozí hodnotou ve skupině s erenumabem oproti skupině s perorální profylaktickou léčbou (56,2 % vs. 16,8 %; p < 0,0001), graf 2. Ve srovnání s perorální preventivní terapií snížila léčba erenumabem významně průměrný počet MMD v každém časovém bodě až do 12. měsíce (p < 0,001; graf 3), což se odrazilo také na retenci pacientů a výsledcích PGIC. Studii dokončilo 86,9 % pacientů ze skupiny s erenumabem a 37,5 % ze skupiny standardní preventivní léčby. Očekávaného klinického zlepšení dosáhlo dle PGIC 76 % pacientů ve skupině s erenumabem a 18,8 % ve skupině standardní perorální profylaxe.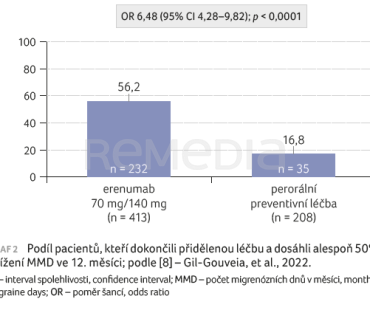
Erenumab prokázal setrvalou vyšší účinnost ve srovnání s perorálními preventivními přípravky u pacientů s EM, u kterých selhala jedna nebo dvě profylaxe proti migréně.
Během sledování nebyly zaznamenány žádné nové bezpečnostní signály. Podíl pacientů, kteří ukončili léčbu z důvodu nežádoucích účinků, byl vyšší ve skupině perorální preventivní léčby (23,3, % vs. 2,9 %) [8].
Studie LIBERTY
Studie LIBERTY se zaměřila na skupinu obtížně léčitelných pacientů s EM. Tato studie fáze IIIb probíhala na 59 místech v 16 zemích Evropy a Austrálie. Zařazeni mohli být pacienti ve věku 18–65 let s anamnézou EM s aurou nebo bez aury v předchozích 12 měsících, kteří měli migrénu 4–14 dní v měsíci během tří měsíců před screeningem a byli neúspěšně léčeni (z hlediska účinnosti nebo snášenlivosti nebo obojího) dvěma až čtyřmi konvenčními preventivními terapiemi (amitriptylin, kandesartan, flunarizin, lisinopril, propranolol nebo metoprolol, topiramát, valproát nebo divalproex, venlafaxin nebo další preventivní léky schválené v dané oblasti).
Úvodní 12týdenní fáze byla dvojitě zaslepená. Celkem 246 pacientů bylo randomizováno v poměru 1 : 1 k aplikaci erenumabu (n = 121) v dávce 140 mg (dvě 70mg injekce) nebo placeba (n = 125) každé 4 týdny s.c. po dobu 12 týdnů. Anamnézu dvou druhů konvenční profylaktické léčby mělo z celkem 246 pacientů 95 (39 %) účastníků, 93 (38 %) účastníků tři a 56 účastníků (23 %) čtyři. Primárním cílovým ukazatelem byl podíl pacientů, kteří dosáhli alespoň 50% snížení MMD během 9.–12. týdne.
Tato dvojitě zaslepená léčebná fáze prokázala účinnost 140 mg erenumabu u pacientů s EM, u kterých selhaly 2–4 předchozí preventivní terapie. V týdnu 12 dosáhlo ≥ 50% snížení MMD oproti výchozí hodnotě 36 (30 %) pacientů léčených erenumabem ve srovnání se 17 (14 %) pacienty ve skupině s placebem (p = 0,002).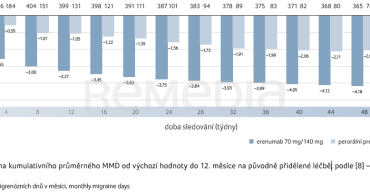
Pacienti, kteří dokončili dvojitě zaslepenou fázi sledování, mohli pokračovat do otevřené extenze s léčbou 140 mg erenumabu aplikovaných měsíčně až po dobu tří let. Publikovány byly výsledky dvouletého a nyní již i tříletého sledování.
Dvouleté otevřené hodnocení demonstrovalo dlouhodobý efekt léčby a vysoký podíl pacientů, kteří si udrželi odpověď na léčbu. Hlavními výstupy interim hodnocení ve 112. týdnu byly: ≥ 50%, ≥ 75% a 100% snížení MMD; změna MMD od výchozí hodnoty; bezpečnost a snášenlivost léčby. Do otevřené extenze vstoupilo 240 pacientů; 118 jich pokračovalo v léčbě erenumabem, 122 pacientů přešlo na terapii erenumabem z placeba. Celkem 181/240 (75,4 %) pacientů dokončilo 112 týdnů léčby. Léčbu přerušilo 24,6 % sledovaných, a sice z důvodu nedostatečné účinnosti (44,0 %), rozhodnutí pacienta (37,0 %) nebo pro nežádoucí příhodu (12,0 %) [9].
Podíl pacientů, kteří v týdnu 112 dosáhli ≥ 50% snížení MMD od výchozí hodnoty, byl 57,2 % (99/173). Snížení MMD o 75 % a více bylo doloženo u 30,6 % (53/173) pacientů a snížení o 100 % u 16,2 % (28/173) pacientů. Změna MMD (standard deviation, SD) od výchozí hodnoty ve 112. týdnu činila –4,2 (5,0) dne.
Léčba erenumabem byla během dvouletého sledování bezpečná a dobře tolerovaná v souladu s bezpečnostním profilem pozorovaným v jiných dlouhodobých studiích s erenumabem a dalšími inhibitory CGRP. Z nejčastějších nežádoucích účinků (≥ 10 %) byly zaznamenány nazofaryngitida, chřipka a bolesti zad. Četnost přerušení léčby z důvodu nežádoucích účinků byla nízká.
Ve 168. týdnu sledování pak bylo hodnoceno: dosažení ≥ 30%, ≥ 50%, ≥ 75% a 100% snížení MMD oproti výchozí hodnotě; změna MMD od výchozí hodnoty; celkové skóre testu dopadu bolesti hlavy (HIT‑6); deník dopadu migrény na fyzické funkce (Migraine Physical Function Impact Diary, MPFID), každodenní aktivity, fyzické postižení a bezpečnost léčby.
Z 240 pacientů vstupujících do otevřené extenze jich dokončilo tříleté sledování 169 (70,4 %) [10]. Mezi důvody předčasného ukončení léčby byly uvedeny nedostatečná účinnost (12,5 %, n = 30), rozhodnutí pacienta (10,8 %, n = 26) a nežádoucí účinky léčby (4,6 %; n = 11). Podíl pacientů s ≥ 30%, ≥ 50%, ≥ 75% a 100% odpovědí na léčbu po tříletém období léčby činil 72,8 %, 52,3 %, 33,1 % a 13,2 %, v tomto pořadí. Průměrná změna MMD (SD) od výchozí hodnoty po třech letech byla –4,4 (3,9). Průměrná změna skóre HIT‑6, MPFID‑EA sledující každodenní aktivity (everyday activities, EA) a MPFID‑PI zaměřeného na fyzické postižení (physical impairment, PI) od výchozího stavu byla –9,7 (8,9), –6,1 (8,2) a –5,1 (7,6). Mezi nežádoucími účinky byly nejčastěji (> 10 %) zaznamenány nazofaryngitida, chřipka a bolesti zad [3].
Závěrem lze shrnout, že účinnost erenumabu byla u pacientů s EM a 2–4 předchozími neúspěšnými preventivními léčbami migrény zachována po dobu tří let. Erenumab byl dobře tolerován a po třech letech expozice nebyly hlášeny žádné nové bezpečnostní signály.
Shrnutí
Protilátky cílící na dráhu CGRP jsou v léčbě migrény dosud rezervovány jako terapeutická možnost pro těžce postižené pacienty s migrénou, u nichž selhaly nebo nebyly vhodné dosud standardní profylaktické terapie. Přímé srovnání účinnosti těchto dvou léčebných modalit, které přinesla studie HER‑MES, dosud chybělo. HER‑MES demonstrovala, že léčba erenumabem je oproti topiramátu provázena lepší snášenlivostí a přináší vyšší pravděpodobnost dosažení klinicky významného snížení frekvence migrén se zlepšením kvality života nemocných.
Při volbě léčby hrají významnou roli charakteristiky pacienta, jeho komorbidity, účinnost léčby a profil nežádoucích účinků. Právě snášenlivost léčby podmiňující spolupráci pacienta je neopomenutelným faktorem účinnosti terapie. Jak doložila další klinická hodnocení, anti‑CGRP terapie představuje efektivní cílenou léčbu pro pacienty s EM i CM s dobrým profilem účinnosti i bezpečnosti.
Literatura
[1] Goadsby PJ, Reuter U, Hallström Y, et al. A controlled trial of Erenumab for episodic migraine. N Engl J Med 2017; 377: 2123–2132.
[2] Goadsby PJ, Reuter U, Hallström Y, et al. One‑Year sustained efficacy of erenumab in episodic migraine: results of the strive study. Neurology 2020; 95: e469–479.
[3] Dodick DW, Ashina M, Brandes JL, et al. Arise: a phase 3 randomized trial of erenumab for episodic migraine. Cephalalgia 2018; 38: 1026–1037.
[4] Tepper S, Ashina M, Reuter U, et al. Safety and efficacy of erenumab for preventive treatment of chronic migraine: a randomised, double‑blind, placebo‑controlled phase 2 trial. Lancet Neurol 2017; 16: 425–434.
[5] Brandes JL, Diener H‑C, Dolezil D, et al. The spectrum of response to erenumab in patients with chronic migraine and subgroup analysis of patients achieving ≥50%, ≥75%, and 100% response. Cephalalgia 2020; 40: 28–38.
[6] Tepper SJ, Ashina M, Reuter U, et al. Long‑Term safety and efficacy of erenumab in patients with chronic migraine: results from a 52‑week, open‑label extension study. Cephalalgia 2020; 40: 543–553.
[7] Reuter U, Ehrlich M, Gendolla A, et al. Erenumab versus topiramate for the prevention of migraine – a randomised, double‑blind, active‑controlled phase 4 trial. Cephalalgia 2022; 42: 108–118.
[8] Gil‑Gouveia R, Dolezil D, Paemeleire K, et al. Sustained benefit of monthly erenumab versus daily oral preventives in episodic migraine patients from APPRAISE study. 8th Congress of the European Academy of Neurology June 25–28 2022: Poster Nr: S11.001.
[9] Ferrari MD, Reuter U, Goadsby PJ, et al. Two‑year efficacy and safety of erenumab in participants with episodic migraine and 2–4 prior preventive treatment failures: results from the LIBERTY study. J Neurol Neurosurg Psychiatry 2022; 93: 254–262.
[10] Reuter U, Goadsby PJ, Ferrari MD, et al. Three‑Year Efficacy and Safety of Erenumab in Participants with Episodic Migraine and 2–4 Prior Preventive Treatment Failures: Results from the LIBERTY Study. Neurology 2022; 98(18 Supplement): 1100. Dostupné na: https://n.neurology.org/content/98/18_Supplement/1100.