Golimumab v léčbě psoriatické artritidy – obtížné případy z klinické praxe
Souhrn:
Psoriatická artritida (PsA) je spondyloartritida s variabilním průběhem v závislosti na klinické formě onemocnění. V léčbě PsA se používají nesteroidní anti-revmatika (NSA), intraartikulárně podávané glukokortikoidy, některé syntetické chorobu modifikující léky (synthetic disease modifying drugs, sDMARDs) a nově též přípravky biologické léčby. Nejčastěji se používají inhibitory tumor nekrotizujícího faktoru alfa, nově jsou též k dispozici inhibitory dalších prozá-nětlivých cytokinů (IL 12, IL 17, IL 23 aj.). Psoriatická artritida probíhá u části nemocných mírně a dobře odpovídá na léčbu NSA, eventuálně na podávání glukokortikoidů nitrokloubními injekcemi; u pacientů s vyšší aktivitou onemocnění a s větším počtem postižených kloubů je nutná léčba pomocí sDMARDs. Existují však i případy těžké PsA, které jsou k léčbě sDMARDs refrakterní, a případy intolerance léčby. Biologická léčba tak může být jediným řešením pro komplikované případy, např. s vysokou aktivitou onemocnění, s nedostatečnou odpovědí na léčbu i s intolerancí standardní terapie.
Key words: psoriasis – psoriatic arthritis – biological therapy – golimumab.
Summary:
Psoriatic arthritis (PsA) is a seronegative spondyloarthritis with variable course depending on the clinical form of the illness. PsA is treated by non steroid antirheumatics (NSA), intra articular glucocorticoids, some synthetic disease modifying drugs (sDMARDs), and – lately – also by biologicals. Tumor necrosis factor alpha inhibitors are being used most often and, more recently, inhibitors of other proinflammatory cytokines (IL 12, IL 17, IL 23, etc) also became available. Psoriatic arthritis has a mild course in part of the patients, responding well to NSA or to intra articular glucocorticoids; patients with higher disease activity and higher number of affected joints require treatment with sDMARDs. However, there are also severe PsA cases with no response to sDMARDs or intolerance of these drugs. Biological therapy can thus be an only solution in complicated cases, e.g. with high disease activity, unsatisfactory response to treatment or with intolerance of standard therapy.
Psoriatická artritida (PsA) je chronické zánětlivé onemocnění kloubů ze skupiny spondyloartritid. Postihuje asi pětinu nemocných s lupénkou a zpravidla se vyvíjí s odstupem měsíců až let po manifestaci psoriázy; může se ale objevit i současně s lupénkou a u malé části nemocných může artritida kožnímu postižení předcházet [1].
Kloubní postižení má nejčastěji charakter asymetrické oligoartritidy. Dále se můžeme setkat s formou polyartikulární, distální interfalangeální, mutilující i s formou, jež predilekčně postihuje klouby páteře (nejčastěji sakroiliakální skloubení a oblast přechodu mezi hrudní a bederní páteří). Typickým klinickým projevem PsA je též daktylitida (zánět všech kloubů jednoho prstu s tendinitidou) nebo entezitida (bolestivé zánětlivé postižení šlachových úponů) [2].
Psoriatická artritida má ve srovnání s revmatoidní artritidou (RA) celkově lepší průběh i prognózu; oproti RA se častěji setkáváme s mírnějšími, oligoartikulárními formami i se spontánními remisemi. U malé části nemocných však může mít PsA devastující vliv na periferní klouby, na kterých nacházíme destruktivní až osteolytické změny či deformity, nebo se mohou vyskytovat teleskopické prsty [1]. Tato tzv. mutilující forma výrazně zhoršuje funkci postižených kloubů. Velmi důležitým aspektem PsA oproti RA je současné postižení kůže, jež je často pro pacienta traumatizující a výrazně zhoršuje psychické složky kvality života [3]. Léčba onemocnění je proto v ideálním případě cílena současně na kloubní i na kožní postižení.
V léčbě PsA používáme u mírnějších forem nesteroidní antirevmatika (NSA) nebo glukokortikoidy ve formě intraartikulárních injekcí, které mohou u části nemocných postačovat. U závažnějších forem je indikována terapie syntetickými chorobu modifikujícími léky (synthetic disease modifying drugs, sDMARDs) – sulfasalazinem, methotrexatem nebo leflunomidem [4]. Antimalarika a soli zlata se v léčbě PsA nepoužívají, neboť nejsou dostatečně účinné, a navíc mohou zhoršovat kožní postižení. Pacientům s aktivní PsA, která je k léčbě sDMARDs refrakterní, je v současné době možné podat biologickou léčbu, resp. biologické DMARDs, jež představují nejúčinnější způsob terapie kloubního i kožního postižení. V posledních letech přibývají příznivé výsledky s léčbou malými molekulami se specifickým účinkem na tvorbu prozánětlivých cytokinů. Příkladem je apremilast, inhibitor fosfodiesterázy 4, jenž inhibuje spontánní produkci tumor nekrotizujícího faktoru alfa (TNFα) a je již v některých zemích pro léčbu PsA registrován.
Léčba psoriatické artritidy
Strategie léčby PsA a volba jednotlivých l éčiv závisí na typu postižení, na aktivitě a rozsahu kožního postižení, na přidružených onemocněních a také na přání pacienta (např. plánování těhotenství). Léčbu navrhuje revmatolog ve spolupráci s dermatologem, jenž současně vede i lokální dermatologickou léčbu. Doporučení pro léčbu PsA v České republice vydala Česká revmatologická společnost ČLS JEP naposledy v roce 2012 [4]. Obsahují i indikační kritéria biologické léčby PsA (tab. 1) V současné době se připravuje jejich aktualizace.
éčiv závisí na typu postižení, na aktivitě a rozsahu kožního postižení, na přidružených onemocněních a také na přání pacienta (např. plánování těhotenství). Léčbu navrhuje revmatolog ve spolupráci s dermatologem, jenž současně vede i lokální dermatologickou léčbu. Doporučení pro léčbu PsA v České republice vydala Česká revmatologická společnost ČLS JEP naposledy v roce 2012 [4]. Obsahují i indikační kritéria biologické léčby PsA (tab. 1) V současné době se připravuje jejich aktualizace.
Biologická léčiva jsou v současné době, jak již bylo řečeno výše, nejúčinnějším farmakologickým prostředkem léčby psoriázy a PsA. Nejvíce zkušeností máme s inhibitory TNFα (s infliximabem, adalimumabem, golimumabem, certolizumabem a etanerceptem); TNFα je klíčový prozánětlivý cytokin, jenž byl detekován v psoriatických placích a v synoviální tkáni kloubů postižených artritidou. Jeho inhibice má mohutný protizánětlivý účinek a příznivě ovlivňuje kloubní i kožní projevy PsA. V posledních letech byly registrovány i další prostředky biologické léčby s odlišným mechanismem účinku, např. ustekinumab (inhibitor IL‑12 a IL‑23) nebo secukinumab (inhibitor IL‑17) [5].
Golimumab je inhibitor TNFα. Jedná se o plně humánní monoklonální protilátku s dlouhým biologickým poločasem (7–20 dní), umožňujícím podávání jednou měsíčně. Podává se subkutánně v dávce 50 mg; v některých zemích je registrována i intravenózní forma [6]. Účinnost golimumabu v léčbě pacientů s PsA byla prokázána v řadě klinických studií, z nichž je zásadní rozsáhlá multicentrická studie GO‑REVEAL. Bylo v ní sledováno celkem 400 pacientů s PsA, kteří byli léčeni ve dvojitě zaslepeném uspořádání placebem nebo golimumabem po dobu 20 týdnů. Klinický účinek golimumabu byl dramatický – přibližně u poloviny pacientů došlo ke zmírnění kloubního postižení (při podávání placeba jen u 9 % pacientů). Ještě výraznější bylo ovlivnění kožního postižení. Ke zlepšení indexu PASI o 75 % došlo u 58 % pacientů léčených golimumabem, zatímco u placeba jen ve 3 % [7]. Výsledky byly vysoce statisticky významné a vedly k prodloužení studie na 3 a 5 let, ve které již byli všichni pacienti léčení golimumabem. Výsledky prokázaly dlouhodobou účinnost léčby i zpomalení rentgenové progrese PsA při léčbě golimumabem [8,9]. Pětiletou studii dokončilo celkem 69 % randomizovaných pacientů. U většiny z nich setrvávala výrazná terapeutická odpověď až do konce studie (odpověď DAS28‑CRP až u 75–85 % pacientů, odpověď PASI75 u 60–72 %). Výskyt protilátek proti golimumabu byl nízký (1,8 %) [9].
Golimumab byl registrován v České republice v roce 2010 pro léčbu revmatoidní artritidy, ankylozující spondylitidy i PsA. V blízké době bude pravděpodobně indikační spektrum léku rozšířeno i na neradiografickou axiální spondyloartritidu. Golimumab představoval vítané rozšíření palety biologických léčiv určených k léčbě PsA; spektrum těchto léčiv je ve srovnání s možnostmi léčby RA podstatně užší. V současné době je golimumab etablovaným lékem RA, ankylozující spondylitidy i psoriatické artritidy, který má oproti ostatním inhibitorům TNFα výhodu komfortního subkutánního podávání v jedné měsíční dávce.
V klinických studiích je zpravidla sledována dobře definovaná populace nemocných z hlediska aktivity onemocnění, typu postižení apod., ze které jsou však vyloučeni pacienti se závažnějšími přidruženými chorobami, senioři apod. Ovšem v klinické praxi se s těmito pacienty setkáváme pravidelně, a proto mohou být zkušenosti s novými léčivy poněkud odlišné. Praktické aspekty léčby proto lépe odrážejí registry pacientů léčených biologickou léčbou nebo kasuistiky pacientů s netypickým či komplikovaným průběhem onemocnění. Ve své praxi jsem se setkala s několika pacienty trpícími těžkou PsA a dalšími problémy; popis tří zajímavých případů je prezentován níže.
Kasuistika 1: těžká mutilující psoriatická artritida s intolerancí léčby konvenčními DMARDs
Pacientka narozená v roce 1978. Její matka, babička a strýcové z matčiny strany mají psoriázu bez kloubního postižení. Sama pacientka lupénku nemá.
Pacientka podstoupila v dětství, ve věku 13 let, neurochirurgický výkon pro nádor mozečku. Nádor byl benigní, nicméně v důsledku dlouhodobého pobytu v nemocnici a řady nepříjemných diagnostických a terapeutických procedur včetně operace, jež zhoršila strabismus, se u pacientky rozvinula úzkostná porucha a fobie ze zdravotnických zařízení. Do současnosti, kdy je jí již 37 let, chodí na ambulantní kontroly vždy v doprovodu rodinného příslušníka, problematicky vnímá např. změnu lékaře, změnu léčby, obává se nežádoucích účinků léčiv apod. Tento problém velmi ztěžuje léčbu nemocné, je však třeba s ním pracovat.
U pacientky se od roku 1999 vyvíjela séronegativní polyartritida s postižením pravého kolenního kloubu, drobných kloubů pravé ruky a kloubů třetího prstu levé nohy. Od počátku bylo onemocnění provázeno vysokými hodnotami reaktantů akutní fáze zánětu (sedimentace erytrocytů, FW, 50–70/h; hodnota C‑reaktivního proteinu, CRP, v séru 70–90 mg/l; HLA‑B27 a revmatoidní faktor byly negativní). V roce 2000 byla provedena resekce proximálních interfalangeálních (proximal interphalangeal, PIP) kloubů třetího prstu levé nohy; histologickým vyšetřením byla zjištěna kostní nekróza. Následně byla pacientka odeslána k revmatologickému vyšetření.
Na našem pracovišti byla poprvé vyšetřena v lednu 2001, kdy byla zjištěna aktivní polyartritida s asymetrickou distribucí. Klinicky dominovala pravostranná gonitida a artritidy drobných kloubů pravé ruky. Stav byl hodnocen zprvu jako nediferencovaná séronegativní artritida, později byla diagnóza s ohledem na typický klinický obraz a familiární výskyt psoriázy uzavřena jako PsA bez kožního postižení.
Pacientka byla léčena pomocí NSA, sulfasalazinem a intraartikulárními injekcemi glukokortikoidů, vše jen s částečným účinkem. V roce 2002 byla provedena synoviortéza pravého kolenního kloubu a následně artroskopie, při které byla provedena resekce mediální pliky a biopsie synoviální membrány (bez zánětlivých změn). Nález na pravém kolenním kloubu se stabilizoval, nicméně postižení kloubů pravé ruky i levé nohy progredovalo. S pacientkou byly opakovaně probrány jiné léčebné možnosti (methotrexatem, později i biologickými léčivy), jež však pacientka odmítala z obavy z nežádoucích účinků.
V roce 2008 byla při zjevné progresi artritidy na pravé ruce (rozvoj deformity „stříšky“ na třetím prstu pravé ruky) znovu navržena radikálnější léčba a pacientka již souhlasila s terapií methotrexatem (MTX). Užívala jej v letech 2008–2009 v dávce 10–15 mg týdně, rovněž s částečným účinkem, načež musela být léčba ukončena pro dyspeptické obtíže. Znovu byla zahájena léčba sulfasalazinem v běžné i maximální dávce (2–3 g denně perorálně), bez většího účinku. V roce 2009 prodělala pacientka korekční ortopedickou operaci levé nohy.
V roce 2010 dále progredovaly deformity třetího prstu pravé ruky (teleskopický prst). Byla nutná úprava terapie, pacientka nadále odmítala biologickou léčbu, a proto byla zahájena terapie leflunomidem. Léčba vedla ke zmírnění obtíží i k poklesu hodnot reaktantů akutní fáze zánětu, nicméně po několika týdnech se u pacientky objevily silné průjmy, pro které bylo nutné léčbu ukončit. Jako poslední pokus o léčbu konvenčním DMARD byl podán znovu MTX v injekční aplikaci. Tuto léčbu pacientka tolerovala, nicméně ani maximální dávka 25 mg týdně nevedla ke snížení aktivity, následně navíc došlo k rozvoji toxické jaterní léze, pro niž bylo nutno léčbu MTX ukončit. Po normalizaci aktivity jaterních enzymů bylo obnoveno podávání sulfasalazinu, nicméně o rok později musela být tato léčba ukončena pro alergickou kožní reakci.
Po vyčerpání všech možností konvenční terapie pacientka souhlasila s léčbou biologickou. S ohledem na obavy z nežádoucích účinků byla zvolena léčba etanerceptem, která byla zahájena v srpnu 2012. Terapie vedla rychle k poklesu aktivity onemocnění i k normalizaci hodnot FW a CRP; při kontrolním rtg vyšetření po jednom roce léčby nebyla pozorována žádná progrese postižení. Nicméně pacientka bohužel po každé aplikaci injekce pozorovala bole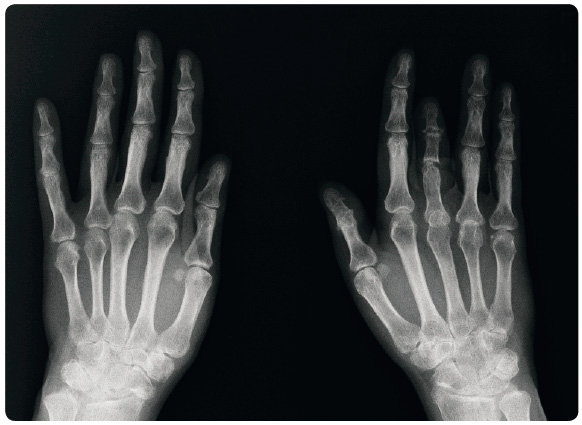 sti, motání hlavy a pokles krevního tlaku, jež odeznívaly během tří dnů. Tyto obtíže, jistě zvýrazňované úzkostnou poruchou, se v průběhu léčby spíše akcentovaly a posléze pacientce velmi komplikovaly život.
sti, motání hlavy a pokles krevního tlaku, jež odeznívaly během tří dnů. Tyto obtíže, jistě zvýrazňované úzkostnou poruchou, se v průběhu léčby spíše akcentovaly a posléze pacientce velmi komplikovaly život.
Proto byla navržena změna léčby a v listopadu 2013 bylo zahájeno podávání golimumabu, kterým je pacientka úspěšně léčena až dodnes. Subjektivní obtíže spojené s injekcí se sice od počátku léčby vyskytovaly v malé míře dále, nicméně se snesitelnou frekvencí jednou měsíčně. Pacientka je dlouhodobě bez kloubních obtíží, s léčbou je spokojena a dosažený terapeutický úspěch měl vliv i na její úzkostné vnímání nežádoucích účinků, které se během léčby podstatně zmírnilo. Po dvou letech léčby je pacientka v remisi, má normální hodnoty reaktantů zánětu a stabilizovaný je rovněž rtg nález (obr. 1).
Kasuistika 2: těžká polyartikulární psoriatická artritida refrakterní k léčbě sDMARDs
Pacientka narozená v roce 1967. Od věku 15 let trpí psoriázou. Lupénku má i její matka a otec matky, ti však nemají kloubní postižení. Kloubní obtíže ve smyslu PsA má pacientka asi dvacet let, kdy byla v péči revmatologa v místě trvalého bydliště, nicméně až do roku 2014 byly kloubní projevy velmi mírné a při léčbě MTX v dávce 15 mg týdně byl stav relativně stabilizovaný.
V únoru 2014 prodělala pacientka závažnou infekci močových cest, pro kterou byla nucena přerušit léčbu MTX. Vzápětí došlo k prudkému zhoršení stavu a k akutní exacerbaci artritidy, objevily se bolesti a otoky kloubů ruky a obou kolenních kloubů s Bakerovou cystou. Byla znovu zavedena léčba MTX v dávce až 30 mg týdně, jež však neměla žádný vliv na aktivitu choroby, a proto byl MTX přechodně podáván i kontinuálně v dávce 10 mg denně, rovněž bez účinku. Od prosince 2014 byl pacientce podáván MTX v kombinaci s leflunomidem v dávce 20 mg denně, opět bez účinku. Biologická léčba jí nikdy navržena nebyla.
Na jaře 2015 byla pacientka vyšetřena v Revmatologickém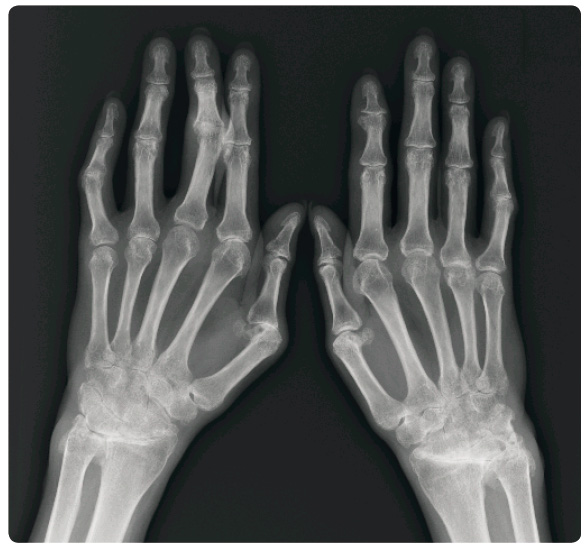 ústavu. Při prvním vyšetření byla zjištěna pokročilá polyartikulární forma PsA. Pacientka měla bolestivé a oteklé zejména klouby rukou (zápěstí oboustranně, na pravé ruce metakarpofalangeální, MCP, skloubení II–V, PIP V vpravo, PIP III vlevo), současně byly již patrny deformity – semiankylózy obou zápěstí, mírná ulnární deviace v MCP skloubeních pravé ruky, deformity „stříšky“ na pátém prstu pravé ruky a na čtvrtém a pátém prstu levé ruky. Klouby dolních končetin postiženy nebyly. Pacientka měla vysokou hodnotu FW (81/h) a mírně zvýšenou hodnotu CRP (13,82 mg/l). Na rtg snímku byly patrné rozsáhlé destruktivní změny v oblasti rukou a nespecifické změny nevylučující postižení páteře (obr. 2).
ústavu. Při prvním vyšetření byla zjištěna pokročilá polyartikulární forma PsA. Pacientka měla bolestivé a oteklé zejména klouby rukou (zápěstí oboustranně, na pravé ruce metakarpofalangeální, MCP, skloubení II–V, PIP V vpravo, PIP III vlevo), současně byly již patrny deformity – semiankylózy obou zápěstí, mírná ulnární deviace v MCP skloubeních pravé ruky, deformity „stříšky“ na pátém prstu pravé ruky a na čtvrtém a pátém prstu levé ruky. Klouby dolních končetin postiženy nebyly. Pacientka měla vysokou hodnotu FW (81/h) a mírně zvýšenou hodnotu CRP (13,82 mg/l). Na rtg snímku byly patrné rozsáhlé destruktivní změny v oblasti rukou a nespecifické změny nevylučující postižení páteře (obr. 2).
Pacientka splňovala indikační kritéria pro biologickou léčbu a s ohledem na charakter zaměstnání a problematické návštěvy lékaře během školního roku (učitelka na 1. stupni ZŠ) byla doporučena subkutánní léčba golimumabem, která byla zahájena v květnu 2015. Léčba MTX v dávce 15 mg týdně byla ponechána, léčba leflunomidem byla ukončena.
Již při první kontrole s odstupem jednoho měsíce byl stav nemocné výrazně zlepšen. Bolesti kloubů byly minimální, potřeba analgetik se snížila na minimum (1–2 tablety týdně). Pacientka začala opět rekreačně sportovat. Objektivně měla kromě deformit bolestivé a oteklé tři drobné klouby ruky; poprvé za poslední dva roky měla normální hodnotu FW (17/h) i CRP (4,49 mg/l).
Při dalších kontrolách se stav dále zlepšoval. Pacientka léčbu toleruje dobře, s výjimkou zvýšeného padání vlasů, které je spíše důsledkem terapie MTX. V současné době bolesti kloubů nemá, analgetika nepotřebuje, vrátila se k aktivnímu životu, pravidelně sportuje a vdala se. Hodnoty FW a CRP jsou dále normální a kožní projevy minimální.
Kasuistika 3: těžká axiální forma psoriatické artritidy s rizomelickým postižením
Pacient narozený v roce 1972. Psoriázou trpí od věku 30 let, jinak je zdráv. V roce 2012 se u něj objevily první kloubní obtíže – gonitida s recidivujícími výpotky, které po intraartikulárních injekcích glukokortikoidů později ustoupily. Přidaly se však bolesti pravého kyčelního kloubu a bolesti zad zánětlivého typu s velmi dobrou odezvou na léčbu NSA a na rozcvičení. V posledním roce se zhoršil i kožní nález. K lokální léčbě byl přidán acitretin podávaný perorálně v dávce 35 mg denně. Opakovaně bylo zjištěno středně vysoké zvýšení hodnot FW a CRP.
V říjnu 2012 byl pacient vyšetřen v Revmatologickém ústavu, kde byl stav vyhodnocen jako aktivní PsA s axiálním a rizomelickým postižením. V klinickém obraze dominovalo postižení pravého kyčelního kloubu, jehož hybnost byla omezená a provázená bolestí (flexe 90°, rotace nulové); na ostatních kloubech byl nález normální. Pacient měl dále bolestivá obě sakroiliakální skloubení, páteř se rozvíjela normálně, všechny distance i dechové exkurze byly normální.
Při vstupním vyšetření byla zjištěna hodnota FW 35/h, CRP 41,14 mg/l a mírné zvýšení aktivity jaterních enzymů; ostatní vyšetřené hodnoty včetně revmatoidních faktorů a autoprotilátek byly v normě. V rtg obraze bylo nápadné axiální postižení – oboustranná sakroiliitida a gracilní, místy přemosťující návalky, nejvíce na hrudní páteři. Na rtg snímku kolenních kloubů byly pouze známky počínající gonartrózy, rtg obraz rukou a kyčelních kloubů byl normální, sonograficky však byla zjištěna pravostranná koxitida.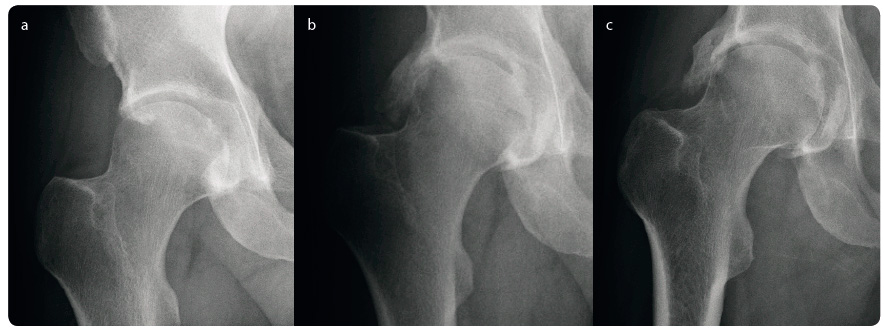
Pacientovi byl nejprve podáván diclofenac. Po této léčbě však došlo ke zhoršení hepatopatie. Po jejím ukončení a záměně za kyselinu tiaprofenovou se jaterní enzymy vrátily k mírně nadhraničním hodnotám. Pacientovi byla doporučena chůze o francouzských holích s odlehčováním postižené končetiny a fyzické šetření. Léčba DMARDs zatím zvažována nebyla z důvodu sporné účinnosti u axiální formy PsA a z důvodu trvalého zvýšení aktivity jaterních aminotransferáz.
Na podzim 2013 se u pacienta objevily i bolesti levého kyčelního kloubu a kontrolním ultrazvukovým vyšetřením se zjistilo oboustranné postižení kyčelních kloubů zánětem, trvalo zvýšení hodnot reaktantů akutní fáze a byla indikována biologická léčba.
Pacientův stav se dále zhoršoval, zejména hybnost v obou kyčelních kloubech. Kontrolní sonografické vyšetření v lednu 2014 sice již koxitidu neprokázalo, nicméně na novém rtg snímku kyčelních kloubů se objevila rozsáhlá kalcifikace v oblasti pravého kyčelního kloubu. Vyšetření magnetickou rezonancí kalcifikace v této oblasti potvrdilo a dále odhalilo atypické periartikulární osifikační změny i vlevo, které by mohly odpovídat chondromatóze, ale i změnám synovie po proběhlém oboustranném zánětu. Ortoped hodnotil stav jako kalcifikující koxitidu a doporučil intenzivní rehabilitaci zaměřenou na zvětšení rozsahu hybnosti v obou kyčelních kloubech. Pacient absolvoval ambulantní rehabilitaci na našem pracovišti a v lázních, bohužel bez většího účinku. Na podzim 2014 stav dále progredoval, pacient se cítil špatně, udával silné bolesti v obou kyčelních kloubech a výrazné snížení hybnosti levého kyčelního kloubu, v němž byla při vyšetření zjištěna flexe 45° a nulové rotace. Dále udával bolest a otok pravého kolene a silné bolesti zad, pro které byl nucen užívat kombinaci analgetik. Sedimentace byla mírně zvýšená (26/h), hodnota CRP v séru byla 19,96 mg/l.
Vzhledem k velmi rychlé progresi postižení byla v tu dobu jediným možným řešením kloubní náhrada. V lednu 2015 byla pacientovi implantována totální endoprotéza levého kyčelního kloubu a naplánována operace pravého kyčelního kloubu.
Pooperační průběh byl bez komplikací a vzápětí byla zavedena biologická léčba golimumabem, první injekce byla aplikována v květnu 2015. Léčba vedla ke zmírnění bolestí zad i pravého kyčelního kloubu; přetrvává pouze omezení hybnosti v pravém kyčelním kloubu, nález na ostatních periferních kloubech je normální. Po zavedení golimumabu do léčebného schématu došlo též ke kompletní regresi kožního postižení a léčba acitretinem byla dermatologem postupně omezována a ukončena. Stále probíhá rehabilitace.
Zcela se normalizovaly laboratorní hodnoty, které byly po celou dobu onemocnění mírně až středně zvýšené.
Při poslední kontrole v listopadu 2015 byl stav pacienta stabilizovaný, vyskytovaly se pouze mírné bolesti zad, proti kterým užívá malou dávku NSA (kyseliny tiaprofenové) podle potřeby. Ostatní klouby včetně pravého kyčelního kloubu v klidu nebolí. Objektivní nález na kloubech a páteři byl s výjimkou pooperačního nálezu na levém kyčelním kloubu a omezené a mírně bolestivé hybnosti pravého kyčelního kloubu zcela normální.
Závěr
Golimumab je účinným biologickým léčivem v terapii PsA. Je vhodný pro pacienty s aktivní PsA po selhání konvenční léčby jako lék první volby, ale lze jej podobně jako u RA použít i jako lék druhé volby po selhání prvního biologika, včetně jiného inhibitoru TNFα. Uvedené případy dokládají, že i u závažných, pokročilých forem PsA, které jsou refrakterní k léčbě syntetickými DMARDs, může léčba golimumabem vést ke snížení aktivity a ke kompletní remisi artritidy i k regresi kožního postižení. Komfortní dávkování jednou měsíčně představuje velkou výhodu zejména pro pacienty zaměstnané a pro pacienty s problematickým vnímáním injekční léčby.
Seznam použité literatury
- [1] Štolfa J, Štork J a kol. Psoriatická artritida a psoriáza. Praha: Maxdorf, 2007; 19–46.
- [2] Štolfa J. Psoriatická artritida. In: Pavelka K, Vencovský J, Horák P, et al. Revmatologie. Praha: Maxdorf Jessenius, 2012; 308–332.
- [3] Husted JA, Gladman DD, Farewell VT, Cook RJ. Health related quality of life of patients with psoriatic arthritis: a comparison with patients with rheumatoid arthritis. Arthritis Rheum 2001; 45: 151–158.
- [4] Štolfa J, Vencovský J, Pavelka K. Doporučené postupy České revmatologické společnosti pro léčbu psoriatické artritidy. Čes Revmatol 2012; 20: 13–18.
- [5] Štolfa J. Terapie psoriatické artritidy. In: Pavelka K, Arenberger P, Lukáš M, et al. Biologická léčba zánětlivých autoimunitních onemocnění v revmatologii, gastroentero-logii a dermatologii. Praha: Grada Publishing, 2014; 167–179.
- [6] Olejárová M. Golimumab. In: Olejárová M. Biologická léčba v revmatologii. Praha: Mladá fronta, 2010; 51–62.
- [7] Kavanaugh A, McInnes IB, Mease PJ, et al. Clinical efficacy, radiographic and safety findings through 2 years of golimumab treatment in patients with active psoriatic arthritis: results from a long term extension of the randomised, placebo controlled GO REVEAL study. Ann Rheum Dis 2013; 72: 1777–1785.
- [8] Kay J, Fleischmann R, Keystone E, et al. Golimumab 3 year safety update: an analysis of pooled data from the long term extensions of randomised, double blind, place-bo controlled trials conducted in patients with rheumatoid arthritis, psoriatic arthritis or ankylosing spondylitis. Ann Rheum Dis 2015; 74: 538–546.
- [9] Kavanaugh A, McInnes IB, Mease P, et al. Clinical efficacy, radiographic and safety findings through 5 years of subcutaneous golimumab treatment in patients with active psoriatic arthritis: results from a long term extension of a randomised, placebo controlled trial (the GO REVEAL study). Ann Rheum Dis 2014; 73: 1689–1694.