Inhalační anticholinergika a fixní trojkombinace Enerzair® v léčbě průduškového astmatu – od teorie k praxi
Souhrn:
Nevrlka J. Inhalační anticholinergika a fixní trojkombinace Enerzair® v léčbě průduškového astmatu – od teorie k praxi. Remedia 2021; 31: 427–433.
Značný počet pacientů s průduškovým astmatem není pod uspokojivou kontrolou ani při intenzifikaci léčby kombinací inhalačního kortikosteroidu (IKS) s další léčebnou modalitou (standardně LABA). Přidání dlouhodobě působících anticholinergik (LAMA) do trojkombinace má potenciál v těchto případech žádoucí kontrolu nad astmatem zajistit, a to při zachování plné tolerance léčby. Mimo specifický případ syndromu překryvu astmatu a CHOPN (ACOS) jsou pro léčbu asthma bronchiale v České republice aktuálně indikovány a hrazeny tři inhalační přípravky s obsahem LAMA. Jedním z nich je fixní trojkombinace IKS/LABA/LAMA v inhalátoru Breezhaler® pod názvem Enerzair®. Článek navazuje na farmakologické profily přípravku Enerzair® Breezhaler® zveřejněné v tomto časopise dříve a zamýšlí se nad využitím inhalačních anticholinergik a konkrétně léčivého přípravku Enerzair® v praxi astmatologů.
Summary:
Nevrlka J. Inhalation anticholinergics and fixed triple combination Enerzair® in the treatment of bronchial asthma – from theory to practice. Remedia 2021; 31: 427–433.
A considerable number of patients with bronchial asthma are not under satisfactory control even with treatment intensification combining inhalation corticosteroid (ICS) with another treatment modality such as long‑acting β2 agonist (LABA). The addition of long‑acting muscarinic antagonists (LAMA) to triple combination has the potential to ensure sufficient control in these cases, with the maintenance of complete treatment tolerance. Currently, there are three inhalation drugs containing LAMA indicated and reimbursed in the Czech Republic, except for asthma‑COPD overlap syndrome. One of them is a fixed triple combination of ICS/LABA/LAMA in the Breezhaler® inhaler called Enerzair®. The article follows the pharmacological profiles of Enerzair® Breezhaler® published earlier in this magazine, and reflects the use of inhalation anticholinergics, specifically with Enerzair®, in the practice of asthmatologists.
Key words: bronchial asthma, inhalation anticholinergics, LAMA, triple combination of ICS/LABA/LAMA, Enerzair – Breezhaler
Úvod
Asthma bronchiale (průduškové astma, AB) je heterogenní onemocnění charakterizované chronickým zánětem a remodelací průdušek spojenými s jejich hyperreaktivitou a variabilní, často reverzibilní obstrukcí. Odhaduje se, že v České republice je až 800 tisíc astmatiků. Choroba může nabývat různých podob. Při klasifikaci AB se snažíme určit jednak závažnost nemoci ve smyslu obecném i aktuálním (tíže a kontrola), jednak se snažíme určit fenotyp [1]. Správná klasifikace konkrétního pacienta má zásadní význam pro určení adekvátní léčby [2]. Diagnostický a léčebný postup můžeme opřít o propracované guidelines mezinárodní (zejména dokumenty Global Initiative for Asthma, GINA [3]) i národní. Naší základní směrnicí je Doporučený postup diagnostiky a léčby bronchiálního astmatu jako společný dokument České společnosti alergologie a klinické imunologie (ČSAKI ČLS JEP) a České pneumologické a ftizeologické společnosti (ČPFS ČLS JEP) [4].
Obecně lze říci, že pacient včas a adekvátně léčený a dodržující léčebný režim má ve většině případů všechny předpoklady k zachování plné kvality života a dobrou prognózu. Číselně vyjádřeno, uspokojivé kontroly nad chorobou by mělo být dosahováno pomocí standardní farmakoterapie až u 95 % pacientů [5]. Některé zahraniční práce nicméně pro reálnou praxi odhadují, že navzdory rozvinutým možnostem léčby zůstává až 45 % pacientů s AB nedostatečně kontrolovaných [6]. To představuje nepřijatelnou zátěž pro kvalitu života pacientů, ale i zvýšené společenské náklady přímé (v rámci zdravotní péče) a nepřímé (například v důsledku ztráty pracovní produktivity).
Syndrom překryvu astmatu s chronickou obstrukční plicní nemocí (ACOS)
Z dnešního pohledu nejsou AB a chronická obstrukční plicní nemoc (CHOPN) uzavřenými nozologickými jednotkami. Výrazem toho je tzv. syndrom překryvu astmatu a CHOPN (Asthma Chronic obstructive pulmonary disease Overlap Syndrome, ACOS), který spočívá v perzistující bronchiální obstrukci a kombinaci znaků spojovaných s AB nebo naopak s CHOPN. Prevalence ACOS v primárně astmatické populaci se odhaduje mezi 15–20 %, zejména jde o kuřáky a profesní astmatiky. Prevalence ACOS v populaci primárně trpící CHOPN se pohybuje kolem 10 %, jedná se především o pacienty s častými exacerbacemi [7].
Léčba průduškového astmatu
Léčebná strategie je založena na požadavku dosáhnout a udržet tzv. plnou kontrolu nad astmatem. Obecně jsou preferována preventivní opatření a farmakoterapie zaměřená na potlačení bronchiálního zánětu a současně hyperreaktivity průdušek. Cílem je odstranit obtěžující projevy onemocnění, zabránit vzniku exacerbací, ale i bránit ireverzibilní remodelaci tkáně dolních cest dýchacích. Současně se usiluje o minimalizaci nutné farmakoterapie (zejména podávané dávky glukokortikoidů) v zájmu dosažení co nejmenšího rizika nežádoucích účinků [3,4].
Základní léčebnou modalitou
splňující výše uvedené požadavky jsou inhalační
kortikosteroidy (přesněji glukokortikoidy, IKS). Mají vliv
na široké spektrum zánětlivých procesů a jsou téměř
vždy viditelně účinné. Zlepšují významně prognózu astmatika
[8]. Stran nežádoucích systémových účinků lze říci, že
v nízkých dávkách nepředstavují problém. Rizika zvažujeme
až od středních dávek, a to s přihlédnutím
k předpokládané responzibilitě (např. osteoporóza u žen
po menopauze) a komorbiditám. Paušálně je třeba tato
rizika zohlednit až od vysokých dávek [9]. Dávkové srovnání
IKS přehledně uvádí tabulka 1 [3].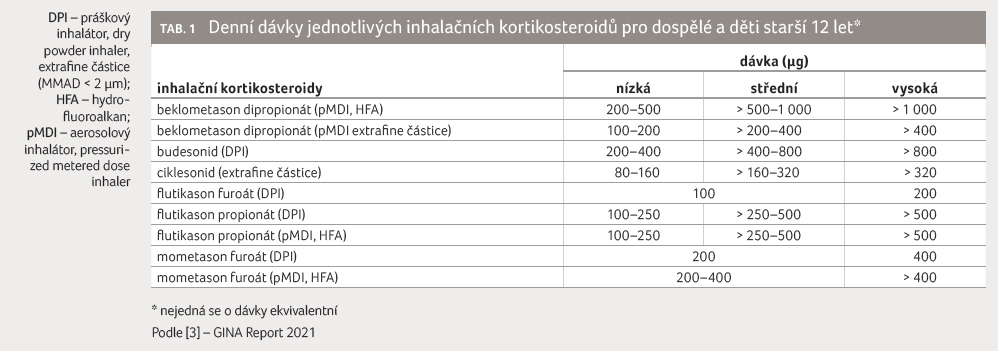
Navyšování denní dávky IKS nad tzv. střední dávku přináší většinou jen malý účinek, ale současně zvyšuje významně riziko nežádoucích účinků. Proto k nízkým a středně vysokým dávkám IKS obvykle přidáváme další léčebnou modalitu, typicky β2 agonistu s dlouhodobým účinkem (long acting β2 agonist, LABA), resp. s ultradlouhodobým účinkem (ultra long acting β2 agonist, U LABA). Lze tu (zejména při fixní kombinaci) dokonce očekávat synergický efekt. Pro praxi se udává, že přidání LABA k IKS vede k obdobným až lepším efektům než zdvojnásobení původní dávky IKS [10].
Dalšími léčebnými modalitami indikovanými zejména do kombinací s IKS jsou antileukotrieny (leukotriene receptor antagonist, LTRA), anticholinergika, ev. také kromony a teofyliny. Speciální postavení má specifická alergenová imunoterapie a biologická léčba [3,4].
Anticholinergika v léčbě astmatu
V léčbě AB jsou dlouhodobě jako alternativa k úlevovým β2 agonistům dostupná anticholinergika s krátkodobým účinkem (short acting muscarinic antagonists, SAMA), konkrétně molekula ipratropium bromid. Existuje samostatně i jako fixní kombinace s fenoterolem v tlakovém aerosolovém dávkovači. Bronchodilatační efekt má odlišný mechanismus (blokace acetylcholinové signalizace přes muskarinové receptory dýchacích cest) než β2 agonisté, a je tak v případné kombinaci s nimi aditivní. Ipratropium bromid má rychlý nástup účinku a zvažuje se především u pacientů vyššího věku a pacientů s některými kardiovaskulárními komorbiditami [4].
Inhalační anticholinergika s dlouhodobým účinkem neboli dlouhodobě působící muskarinoví antagonisté (long acting muscarinic antagonists, LAMA), resp. přípravky s ultradlouhodobým účinkem (ultra long acting muscarinic antagonists, U LAMA) byla původně primárně určena pro paušální léčbu CHOPN. V této souvislosti se logicky nabízí jejich použití v rámci překryvného syndromu ACOS, což je ale limitováno indikačním omezením na pneumology. Relativní novinkou je použití LAMA pro udržovací léčbu AB jako takového (i mimo ACOS). Teoreticky vychází z aditivního bronchodilatačního efektu po přidání k LABA, ale i z průkazu určitých protizánětlivých účinků [11].
Klinicky bylo prokázáno už v roce
2012, že přídavek LAMA (tiotropium bromid) u pacientů se
špatně kontrolovaným astmatem navzdory použití kombinace
IKS/LABA má své výhody [12]. Další důkazy, i pro jiné
molekuly LAMA a pro fixní kombinace, na sebe nenechaly
dlouho čekat. Recentně v roce 2021 vyšly hned dvě práce
shrnující výsledky dosud publikovaných randomizovaných
klinických studií (RCT) fáze III hodnotících účinky fixních
kombinací IKS/LABA/LAMA (single inhaler triple therapy, SITT)
u pacientů s diagnózou AB. Jde o studie TRIMARAN
[13], TRIGGER [14], IRIDIUM [15], ARGON [16] a CAPTAIN [17],
které zahrnuly celkem 9 535 pacientů. Podle metaanalýzy
Roglianiho a kol. [18] byly SITT s vysokodávkovými IKS
obecně účinnější než ty se středními dávkami IKS (pokud jde
o zlepšení funkce plic a snížení závažných
exacerbací), různé hodnocené SITT byly (při kontrole astmatu)
podobně účinné a nebylo zaznamenáno zvýšení
bezpečnostních rizik. Systematický přehled Agustiho a kol.
[19] pak doplnil, že SITT byly zvláště prospěšné (zlepšení
plicních funkcí a redukce exacerbací) u pacientů
s pokročilou a špatně reverzibilní obstrukcí, snížení
středně těžkých a těžkých exacerbací bylo pozorováno
zejména v zimě a že efekt na snížení
výskytu exacerbací nebyl o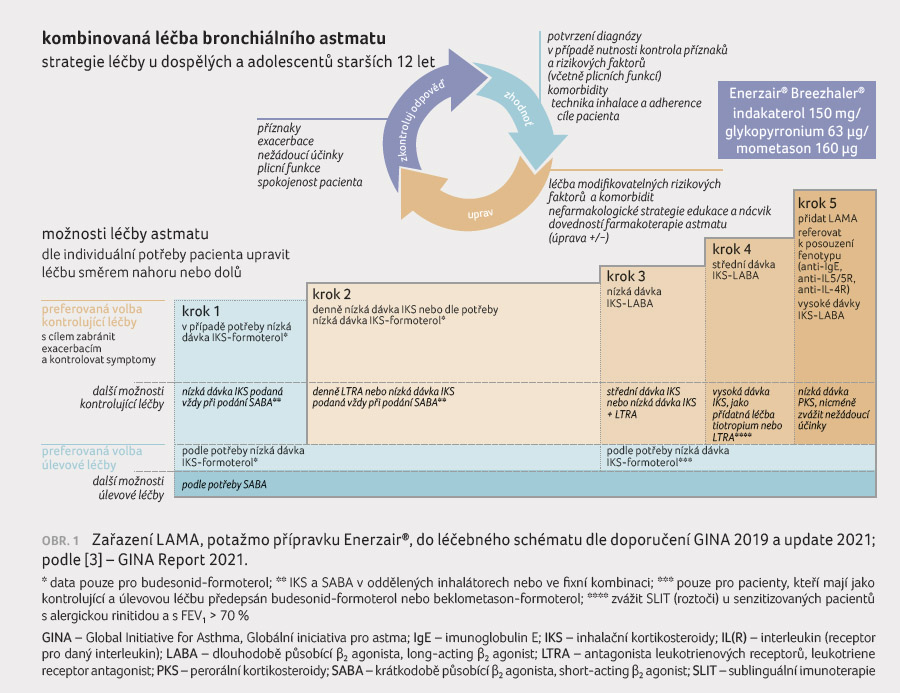 vlivněn individuální koncentrací
eozinofilů. Závěr o pozitivním vlivu přídavku LAMA
ke kombinaci IKS/LABA ve smyslu dalšího zlepšení
plicních funkcí a oddálení těžkých exacerbací astmatu
považuje GINA za průkazný (vědecký důkaz stupně A, resp.
pro druhý stupně B). Zařazení LAMA, potažmo léčivého
přípravku Enerzair,
do léčebného schématu AB dle recentního doporučení GINA
přehledně ukazuje obrázek 1.
vlivněn individuální koncentrací
eozinofilů. Závěr o pozitivním vlivu přídavku LAMA
ke kombinaci IKS/LABA ve smyslu dalšího zlepšení
plicních funkcí a oddálení těžkých exacerbací astmatu
považuje GINA za průkazný (vědecký důkaz stupně A, resp.
pro druhý stupně B). Zařazení LAMA, potažmo léčivého
přípravku Enerzair,
do léčebného schématu AB dle recentního doporučení GINA
přehledně ukazuje obrázek 1.
V České republice (ČR) byl pro diagnózu AB (i mimo ACOS) schválen jako první LAMA tiotropium bromid ve formě monokomponentního přípravku v aerosolovém systému s jemnou mlžinou Respimat. Druhou v pořadí se stala v roce 2021 molekula glykopyrronium bromidu jako fixní trojkombinace. Nejprve v kombinaci s IKS mometason furoátem a U LABA indakaterolem v práškovém systému Breezhaler a recentně od 1. září 2021 společně s IKS beklometason dipropionátem a LABA formoterolem v tlakovém aerosolovém systému.
Léčivý přípravek Enerzair® a jeho pozice v léčbě astmatu
Léčivý přípravek Enerzair byl schválen k použití jako udržovací (preventivní) léčba u dospělých pacientů s průduškovým astmatem Evropskou lékovou agenturou (EMA) v červenci 2020. Pro ČR je plně k dispozici získáním úhrady ze zdravotního pojištění od 1. května 2021. Předpokladem indikace (a úhrady) je skutečnost nedostatečně kontrolovaného astmatu u dospělého pacienta při léčbě kombinací vysokých dávek IKS a LABA a současně existence jedné nebo více exacerbací astmatu u tohoto pacienta v předchozím roce. Lék je preskripčně omezen na specializaci pneumolog nebo alergolog [20].
Přípravek je dostupný ve formě tvrdých tobolek obsahujících prášek k inhalaci s trojkombinací účinných látek, pomocnými látkami a nosičem, kterým je monohydrát laktózy v množství 25 mg. Účinnými látkami jsou kombinace U LABA indakaterolu v množství 150 µg + U LAMA glykopyrronia v množství 50 µg (resp. v komplexu glykopyrronium bromidu 63 µg) + IKS mometason furoátu v množství 160 µg. Označení léku nicméně v souladu s novými principy vychází z dávky podané, tj. z dávky, která skutečně opouští náustek inhalátoru při optimální aplikaci. Tato podaná (a balením deklarovaná) dávka představuje pro indakaterol 114 µg, glykopyrronium 46 µg a mometason furoát 136 µg [20].
V podrobnějších údajích o vlastnostech použitých účinných látek a o výsledcích odpovídající klinické studie (IRIDIUM) odkazuji na SPC [20] a farmakologické profily přípravku Enerzair zveřejněné v letošním ročníku tohoto periodika [21,22]. Nicméně vycházeje z těchto a dalších podkladů, zdůrazňuji několik skutečností, které mohou mít dopady na praktické použití přípravku lékařem:
Bezpečnost i účinnost připravku Enerzair v léčbě AB (i CHOPN) je dle klinických studií i dosavadní praxe na vysoké úrovni. Dostatečně robustní data nemáme zatím jen u dětí a mladistvých (do věku 18 let) a u těhotných žen.
Tachyfylaxe nebyla v průběhu klinických studií pozorována. Populační farmakokinetická analýza neukazuje na klinicky relevantní závislost účinku léku na věku, pohlaví, tělesné hmotnosti a kouření. U starších pacientů (65 let a starší) a pacientů trpících mírnou až středně těžkou renální nebo hepatální insuficiencí není potřeba upravovat dávku. Farmakodynamicky se Enerzair vyznačuje rychlým nástupem účinku (do 5 minut po podání) a jeho trváním po celých 24 hodin. Doporučenou frekvencí podávání je proto inhalace jednou denně, nejlépe ve stejnou denní dobu. Volbu denní doby je možno nechat na pacientovi, neovlivňuje efekt ani snášenlivost léku [23].
Dávkování přípravku Enerzair (potažmo mometason furoátu) 1× denně zvyšuje obecně adherenci k léčbě. Tato možnost se jinak stran IKS týká jen nízkých dávek budesonidu, nízkých až středních dávek ciklesonidu a flutikason furoátu. V ostatních případech je v zájmu zachování optimálního efektu IKS doporučováno dávkování dvakrát denně [4,24].
Maximální denní dávka je definována jako jedna tobolka denně. I proto by k sanaci akutních příznaků astmatu měl být pacient vybaven samostatnou úlevovou bronchodilatační léčbou.
Podobně jako pro fixní kombinace IKS/LABA lze i pro trojkombinaci IKS/LABA/LAMA předpokládat, že synergický efekt bude posilován aplikací těchto léčebných modalit ve fixní kombinaci. To může být výhodou vůči kombinacím IKS/LABA s monokomponentním přípravkem s obsahem LAMA [25].
Léčba přípravkem Enerzair je dobře snášena. Jedinou kontraindikací je hypersenzitivita na obsažené léčivé nebo pomocné látky. Nicméně vzhledem ke zvýšenému riziku některých nežádoucích účinků, jež se odvozují ze skupinových vlastností použitých léčivých látek, je třeba u určitých pacientů zvýšené opatrnosti. Pro indakaterol platí, že obdobně jako jiná β2 mimetika může u citlivých pacientů vyvolat kardiovaskulární nežádoucí účinky, jako je tachykardie, vzácněji i zvýšený krevní tlak nebo změny na EKG, jako je prodloužení intervalu QT. Obecně se doporučuje opatrnost při aplikaci u pacientů s kardiovaskulárními poruchami a u pacientů se změnami na EKG výše uvedeného typu [26].
Obdobně jako u jiných anticholinergik se v případě podávání glykopyrronia doporučuje opatrnost u pacientů trpících glaukomem s uzavřeným úhlem a u pacientů s hyperplazií prostaty, resp. obstrukcí hrdla močového měchýře obecně. Na druhé straně inhalační anticholinergika jsou ve stáří (kde lze výše uvedené poruchy očekávat častěji) respektovanou lékovou skupinou pro svůj efekt i dobrou toleranci [4].
Klinické studie s mometason furoátem nepřinesly žádné důkazy o případné supresi osy hypotalamus hypofýza nadledvinky i při dlouhodobé inhalační léčbě dávkami vyššími než 800 μg mometason furoátu denně (v přípravku Enerzair je aplikováno denně jen 160 μg, resp. 136 μg). Mometason furoát se vyznačuje zvláště vysokou vazebnou afinitou ke glukokortikoidním receptorům (např. 5× vyšší než budesonid a 1,5× vyšší než flutikason propionát) [27]. I to zajišťuje při podání nízkou systémovou biologickou dostupnost, která výrazně redukuje riziko systémových nežádoucích účinků. V této souvislosti je třeba při léčbě přípravkem Enerzair opatrnosti pouze při současné terapii silnými inhibitory CYP3A4 (např. ketokonazol, itrakonazol), které mohou zvyšovat systémovou expozici IKS. Opatrnost se skupinově doporučuje také u pacientů s nově vzniklými očními potížemi, při tuberkulóze a u pacientů s chronickými nebo neléčenymi infekcemi.
Parametry inhalátoru Breezhaler® a jeho pozice v léčbě astmatu
Breezhaler je práškový inhalátor (Dry Powder Inhaler, DPI), kde vlastní účinné látky (Enerzair) jsou uloženy odděleně od inhalačního zařízení ve formě tobolek. Tělo tobolky je průhledné a umožňuje vizuální kontrolu obsahu (bílý prášek). Tobolky jsou jednotlivě chráněny v snadno oddělitelných komůrkách blistru. Balení obsahuje tři blistry vždy s 10 tobolkami. Základní aplikační postup je následující: Tobolka musí být vyjmuta z blistru bezprostředně před použitím, vložena do inhalátoru a perforována pevným stiskem postranních tlačítek. Nádechový manévr musí být rychlý, intenzivní a hluboký. V takovém případě je během inhalace slyšet chrčivý zvuk (zvuková kontrola). Po inhalaci se lze ujistit, zda je tobolka prázdná (zraková kontrola). Následuje výplach úst vodou s vyplivnutím jako prevence lokálních nežádoucích účinků [20].
V otázce inhalačního zařízení
je třeba pro praxi vymezit dvě oblasti. První jsou technické
parametry inhalátoru a jeho schopnost zajistit podání plné
dávky léku na cílová místa u nejrůznějších
pacientů. Tyto technické parametry vystupují do popředí
zejména u nemocných s těžším funkčním
postižen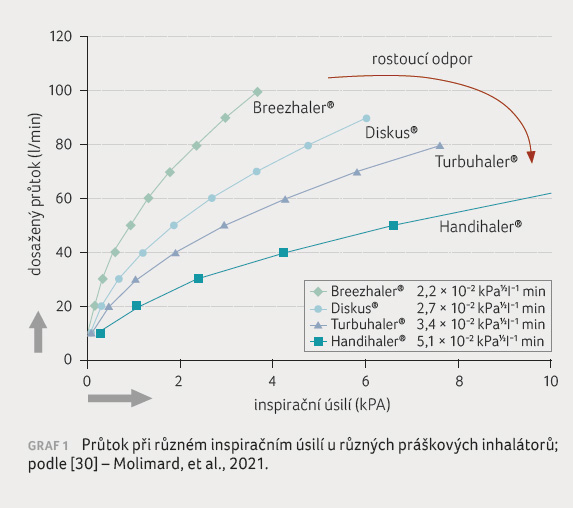 ím plic a při potížích s dosažením plné
kontroly nad chorobou. U práškových inhalátorů je věnována
pozornost zejména vnitřnímu odporu kvůli požadavku na větší
nádechové úsilí při inhalaci léku [28]. Konkrétně systém
Breezhaler se vyznačuje
nízkým vnitřním odporem a doporučená hodnota nádechové
rychlosti je od 60 l/min. Je nicméně prokázáno, že
Breezhaler zajišťuje
vysokou úroveň konzistence podané dávky léku v plicích
v širokém rozsahu průtokových rychlostí mezi 30 a 90 l/min
[29]. Tyto charakteristiky umožňují efektivní použití přípravku
Breezhaler s menším
inspiračním úsilím, než jaké je třeba u některých
jiných DPI systémů (graf 1) [30]. To může být
prospěšné zejména u starších pacientů a pacientů se
závažným stupněm funkční plicní poruchy, kteří mají potíže
s vytvářením potřebného inspiračního toku [29].
ím plic a při potížích s dosažením plné
kontroly nad chorobou. U práškových inhalátorů je věnována
pozornost zejména vnitřnímu odporu kvůli požadavku na větší
nádechové úsilí při inhalaci léku [28]. Konkrétně systém
Breezhaler se vyznačuje
nízkým vnitřním odporem a doporučená hodnota nádechové
rychlosti je od 60 l/min. Je nicméně prokázáno, že
Breezhaler zajišťuje
vysokou úroveň konzistence podané dávky léku v plicích
v širokém rozsahu průtokových rychlostí mezi 30 a 90 l/min
[29]. Tyto charakteristiky umožňují efektivní použití přípravku
Breezhaler s menším
inspiračním úsilím, než jaké je třeba u některých
jiných DPI systémů (graf 1) [30]. To může být
prospěšné zejména u starších pacientů a pacientů se
závažným stupněm funkční plicní poruchy, kteří mají potíže
s vytvářením potřebného inspiračního toku [29].
Druhou oblastí určující vhodnost inhalačního zařízení k indikaci je jeho uživatelská příjemnost a současně rezistence k případným aplikačním chybám. Obecně v léčbě AB platí, že je třeba vždy počítat s možnou chybovostí v aplikační technice inhalačních léků. Inhalační techniku je nemocného zapotřebí řádně naučit a v budoucnu ji opakovaně kontrolovat [31]. Nedávná studie podchytila nesprávnou manipulaci s inhalátory u téměř 70 % pacientů s astmatem [32]. U některých pacientů je vhodné zohlednit tato rizika už při výběru typu inhalátoru. Jde o faktory, jako jsou schopnosti manuální a intelektuální, preference estetické, cena atd. [33]. Dlužno dodat, že už sama možnost poskytnout lék ve fixní kombinaci oproti několika lékům podávaným samostatně (zvláště při použití různých inhalačních systémů) významně zlepšuje adherenci pacienta k léčbě [4]. Konkrétně systém Breezhaler se dle autora článku sice vyznačuje na první pohled obtížnější manipulací, ale nácvik inhalační techniky je v praxi snadný (zvláště pak u pacientů, kteří dříve používali technicky podobný systém Aerolizer) a při adekvátní edukaci potenciální chybovost výrazně klesá. Tento názor odpovídá výsledkům studie INHALER, kde terénní lékaři posuzovali chybovost inhalační techniky u různých inhalátorů u pacientů s CHOPN (celkem 2 935 pacientů). Systém Breezhaler měl největší podíl pacientů bez chyb obecně (36,5 %) i bez chyb tzv. kritických (15,4 %) [34].
Při použití systému Breezhaler lze popsat následující výhody a limity: Oproti pMDI systémům odpadají u systému Breezhaler problémy s koordinací „ruka mozek“ (neoptimální aplikace dávky zmáčknutím kontejneru před samotným nádechem). Tento problém může přitom vystupovat do popředí i jen nepravidelně, např. při zátěži pacienta rozčilením, nedostatkem času, zhoršením fyzického stavu apod. Dále je eliminována nutnost tzv. primingu (u nových či dlouho nepoužívaných inhalátorů je zapotřebí první 2–4 dávky odstříknout). Naopak limitující u práškových forem může být případná intolerance laktózového nosiče, nemožnost jejich použití se spacerem či případné specifické aplikační kroky zvyšující možnost chybovosti při aplikaci dávky.
Oproti DPI systémům se zásobníky odpadá vzhledem k zabalení jednotlivých dávek léku do tobolek dále chráněných hliníkovou fólií riziko poškození léku vlhkostí a vzhledem k viditelně danému počtu dávek v blistrech riziko pokračující aplikace z již prázdného zásobníku. Toto je do jisté míry vykoupeno obtížnější manipulací (vkládání tobolek do zařízení s následnou nutností jejich perforace) a skladností léku. Je třeba také myslet na možnost totálního nepochopení aplikačního postupu ze strany pacienta („polykání tobolek“). Na druhou stranu tento postup umožňuje vizuální kontrolu, zda byl lék z kapsle skutečně nadechnut. Toto může být velmi cenné, protože základním aplikačním požadavkem u DPI systémů bývá provedení rychlého a intenzivního nádechu.
Specialitou systému Breezhaler je možnost předpisu a připojení elektronického digitálního senzoru, který zaznamenává údaje o inhalacích pacienta a odesílá je do e aplikace na chytrém telefonu, tabletu nebo počítači. Zvláště mladší pacienty tak může motivovat k lepší adherenci k léčbě [20].
Závěr
Závěrem lze říci, že kombinovaná terapie indakaterol/glykopyrronium/mometason furoát v systému Breezhaler (lék Enerzair) představuje novou bezpečnou a účinnou terapeutickou možnost pro pacienty s astmatem nekontrolovaným vysokými dávkami IKS v kombinaci s LABA (z hlediska úhrady současně s požadavkem na jednu nebo více exacerbací astmatu v předchozím roce a omezením na specializaci pneumolog a alergolog). Podtrhnout je třeba možnost podávání jednou denně pomocí jediného inhalátoru, což má potenciál zlepšit kontrolu nad onemocněním i prostřednictvím posílení adherence pacienta k léčbě. Dalším prostředkem posílení adherence je zatím jedinečný volitelný digitální dávkovací senzor propojený s e aplikací. Výhodou může být také možnost zvukové a zrakové kontroly nad manévrem vlastní inhalace léku a nízký vnitřní odpor zařízení snižující nároky na inspirační úsilí pacientů.
Seznam použité literatury
- [1] Terl M, Sedlak V, Cap P, et al. Asthma management: A new phenotype‑based approach using presence of eosinophilia and allergy. Allergy 2017; 72: 1279‒1287.
- [2] McDonald VM, Fingleton J, Agusti A, et al. Treatable traits: a new paradigm for 21(st) century management of chronic airway diseases. Eur Respir J 2019; 53: 1802058.
- [3] GINA Report, Global Strategy for Asthma Management and Prevention (2021 update). Dostupné na: https://ginasthma.org/wp‑content/uploads/2021/05/GINA‑Main‑Report‑2021‑V2‑WMS.pdf
- [4] Teřl M, Čáp P, Dvořáková R, et al. Asthma bronchiale. In: Kolek V, et al. Doporučené postupy v pneumologii. Praha: Maxdorf, 2016; 55–108 [online]. Dostupné na: http://www.pneumologie.cz/ guidelines.
- [5] Sedlák V, Chlumský J, Teřl M, et al. Obtížně léčitelné astma. In: Kolek V, et al. Doporučené postupy v pneumologii. Praha: Maxdorf, 2016; 108–126.
- [6] Price D, Fletcher M, van der Molen E. Asthma control and management in 8,000 European patients: the REcognise Asthma and LInk to Symptoms and Experience (REALISE) survey. NPJ Prim Care Respir Med 2014; 24: 14009.
- [7] Hardin M, Silverman EK, Barr RG, et al. The clinical features of the overlap between COPD and asthma. Respir Res 2011; 12: 127.
- [8] Abdullah AK, Khan S. Evidence‑based selection of inhaled corticosteroid for treatment of chronic asthma. J Asthma 2007; 44: 1–12.
- [9] Lipworth BJ. Systemic adverse effects of inhaled corticosteroid therapy: A systematic review and meta‑analysis. Arch Intern Med 1999; 159: 941–955.
- [10] Schmidt M, Michel MC. How can 1 + 1 = 3? β2‑adrenergic and glucocorticoid receptor agonist synergism in obstructive airway diseases. Mol Pharmacol 2011; 80: 955–958.
- [11] Barnes PJ. Severe asthma: advances in current management and future therapy. J Allergy Clin Immunol 2012; 129: 48–59.
- [12] Kerstjens HAM, Engel M, Dahl R, et al. Tiotropium in asthma poorly controlled with standard combination therapy. N Engl J Med 2012; 367: 1198−1207.
- [13] Papi A, Virchow JC, Singh D, et al. Extrafine triple therapy and asthma exacerbation seasonality: TRIMARAN and TRIGGER post hoc analyses. J Allergy Clin Immunol 2021; 148: 262−265.e2.
- [14] Singh D, Virchow JC, Canonica GW, et al. Determinants of response to inhaled extrafine triple therapy in asthma: analyses of TRIMARAN and TRIGGER. Respir Res 2020; 21: 285.
- [15] Kerstjens HAM, Maspero J, Chapman KR, et al. Once‑daily, single‑inhaler mometasone‑indacaterol‑glycopyrronium versus mometasone‑indacaterol or twice‑ daily fluticasone‑salmeterol in patients with inadequately controlled asthma (IRIDIUM): a randomised, double‑blind, controlled phase 3 study. Lancet Respir Med 2020; 8: 1000−1012.
- [16] Gessner C, Kornmann O, Maspero J, et al. Fixed‑dose combination of indacaterol/glycopyrronium/mometasone furoate once‑daily versus salmeterol/fluticasone twice‑daily plus tiotropium once‑daily in patients with uncontrolled asthma: a randomised, phase IIIb, non‑ inferiority study (ARGON). Respir Med 2020; 170: 106021.
- [17] Lee LA, Bailes Z, Barnes N, et al. Efficacy and safety of once‑daily single‑inhaler triple therapy (fluticasone furoate/umeclidinium/vilanterol (FF/UMEC/VI) versus FF/VI in patients with inadequately controlled asthma: a double‑blind, randomised, Phase IIIA trial (CAPTAIN study). Lancet Respir Med 2020; 9: 3–5.
- [18] Rogliani P, Ritondo BL, Calzetta L. Triple therapy in uncontrolled asthma: a network meta‑analysis of phase III studies. Eur Respir J 2021; 58: 2004233.
- [19] Agusti A, Fabbri L, Lahousse L, et al. Single inhaler triple therapy (SITT) in asthma: Systematic review and practice implications. Allergy 2021; doi: 10.1111/all.15076.
- [20] Souhrn údajů o přípravku Enerzair® Breezhaler®. Dostupné na: https://www.ema.europa.eu/en/documents/product‑information/enerzair‑breezhaler‑epar‑product‑information_cs.pdf
- [21] Krčmová I, Novosad J. Enerzair Breezhaler – první léčivý přípravek ve fixní inhalační trojkombinaci k léčbě astmatu. Remedia 2020; 30: 1–6.
- [22] Krčmová I, Novosad J, Sedlák V. Nové fixní léčebné kombinace v terapii bronchiálního astmatu ‒ Atectura® a Enerzair® v práškovém inhalátoru Breezhaler®. Remedia 2021; 31: 1–7.
- [23] Beier J, Watz H, Scholz V, et al. The Efficacy of the Combination Indacaterol/Glycopyrronium/Mometasone Furoate Is Independent of Time of Dosing in Patients with Asthma. Am J Respir Crit Care Med 2019; 199: A1277.
- [24] Stanford RH, Averell C, Parker ED, et al. Assessment of adherence and asthma medication ratio for a once‑daily and twice‑daily inhaled corticosteroid/long‑acting beta‑agonist for asthma. J Allergy Clin Immunol Pract 2019; 7: 1488−1496. e7.
- [25] Zhang S, King D, Rosen VM, Ismaila AS. Impact of single combination inhaler versus multiple inhalers to deliver the same medications for patients with asthma or COPD: a systematic literature review. Int J Chron Obstruct Pulmon Dis 2020; 15: 417−438.
- [26] Khindri S, Sabo R, Harris S, et al. Cardiac safety of indacaterol – no clinical effect on QT in healthy subjects. 19th Annual Congress of the European Respiratory Society 2009; Vienna, Abstr No P2031.
- [27] Bousquet J. Mometason furoate: an effective anti‑inflammatory with well‑define safety and tolerability profile in the treatment of asthma. Int J Clin Pract 2009; 63: 806–819.
- [28] Kašák V, Teřl M. Inhalační systémy v léčbě nemocí s chronickou bronchiální obstrukcí. Praha: Maxdorf 2017.
- [29] Molimard M, D’Andrea P. Once‑daily glycopyrronium via the Breezhaler® device for the treatment of COPD: pharmacological and clinical profile. Expert Rev Clin Pharmacol 2013; 6: 503–517.
- [30] Molimard, Kottakis I, Jauernig J, et al. Performance Characteristics of Breezhaler® and Aerolizer® in the Real‑World Setting. Clin Drug Invest 2021; 41: 415–424.
- [31] Pohunek P. Adherence k léčbě perzistujícího astmatu. Alergie 2017; 19: 269–277.
- [32] Román‑Rodríguez M, Metting E, García‑Pardo M, et al. Wrong inhalation technique is associated to poor asthma clinical outcomes. Is there room for improvement? Curr Opin Pulm Med 2019; 25: 18–26.
- [33] Kašák V, Feketeová E. Vliv nesprávné inhalační techniky na úroveň kontroly nad astmatem. Alergie 2010; 12: 244–257.
- [34] Molimard M, Raherison C, Lignot S, et al. Chronic obstructive pulmonary disease exacerbation and inhaler device handling: real‑life assessment of 2935 patients. Eur Respir J 2017; 49: 1601794.