Lakosamid v graviditě a během laktace – kazuistika
Souhrn:
Zárubová J. Lakosamid v graviditě a během laktace – kazuistika. Remedia 2019; 29: 372–373.
Lakosamid (LCM) v monoterapii a v přídatné léčbě fokální epilepsie je v České republice dostupný osm let. Zkušenosti s jeho užíváním v graviditě a během laktace jsou minimální. Přibývá žen s fokální epilepsií, u nichž léčba LCM vede ke kontrole záchvatů. Pokud antiepileptika vhodná k léčbě fokálních záchvatů s dokumentovanou nízkou teratogenitou (lamotrigin, levetiracetam) selhala, nebo je žena netolerovala, je otázkou, jakou další antiepileptickou léčbu lze doporučit. Pokud se LCM u ženy s fokální epilepsií ve fertilním věku osvědčil při kontrole záchvatů, lze v jeho podávání pokračovat i v případě plánování gravidity? Teratogenní riziko není známo. Je nutné upravovat dávku LCM během těhotenství? Data o eventuálních změnách plazmatické koncentrace LCM v průběhu gravidity nejsou dostupná. Pokud žena užívající LCM porodí, může kojit? Potenciální riziko pro kojené novorozence/děti není známo. Studie na zvířatech prokázaly, že se LCM do mateřského mléka vylučuje, což lze předpokládat i u člověka vzhledem k malé vazbě na plazmatické bílkoviny. V článku jsou prezentována data z období těhotenství a laktace u pacientky při monoterapii LCM.
Summary:
Zarubova J. Lacosamide in gravidity and lactation – a case report. Remedia 2019; 29: 372–373.
Treatment with lacosamide (LCM) in monotherapy and adjunctive therapy of focal epilepsy is available in the Czech Republic for 8 years. Experience with its use during pregnancy and lactation is minimal. Lacosamide is used and efficient in women with epilepsy (WWE). If other antiepileptics suitable for the treatment of focal seizures with documented low teratogenicity (lamotrigine, levetiracetam) have failed or a woman has not tolerated them, the question is what other antiepileptic treatment can be recommended? If LCM in a woman with focal epilepsy at fertile age is proven to control seizures, can it be continued for the duration of pregnancy planning? A teratogenic risk is not known. Is it necessary to modify the LCM dose during pregnancy? The data on possible changes in the plasma concentration of LCM during pregnancy are not available. If a woman taking LCM gives birth, can she breastfeed? A potential risk to breastfed infants/children is not known. Animal studies have shown that LCM is excreted in breast milk which can be expected in humans as well due to low binding with plasma proteins. The article presents data from the period of pregnancy and lactation in a patient on LCM monotherapy.
Key words: lacosamide, pregnanc, plasma and breast milk levels.
Úvod
Při léčbě žen s epilepsií novými antiepileptiky se neurolog/epileptolog dříve nebo později setká s otázkou, zda je možné podávat je i v průběhu gravidity a kojení. Obecně jsou farmaceutické společnosti velmi opatrné a před podáváním nových antiepileptik v těhotenství a během laktace varují nebo ho přímo nedoporučují. Klinické zkušenosti tak lze iniciálně získat z jednotlivých neplánovaných otěhotnění. Syntetický derivát aminokyseliny D serinu lakosamid (LCM) je indikován k monoterapii nebo přídatné léčbě epileptických záchvatů fokálních s přechodem/nebo bez přechodu do bilaterálních tonicko klonických. Pokud antiepileptika vhodná k léčbě fokálních záchvatů s dokumentovanou nízkou teratogenitou (lamotrigin, levetiracetam) [1] selhala, nebo je žena netolerovala, může být LCM další volbou. Studie na zvířatech neprokázaly teratogenní účinky LCM u potkanů ani u králíků, ale při dávkách toxických pro matku byla pozorována embryotoxicita. Potenciální riziko u člověka není známo. Lakosamid nemá být během těhotenství podáván, pokud to není nezbytně nutné (přínos pro matku jednoznačně převyšuje potenciální riziko pro plod). Pokud se žena rozhodne otěhotnět, je nutné užívání tohoto přípravku znovu pečlivě zvážit. Publikována byla zatím anekdotická data [2].
Kazuistika
Pacientka s kompenzovanou fokální epilepsií nezjištěné etiologie otěhotněla při monoterapii LCM 200 mg/den. Po diskusi a poskytnutí srozumitelné informace o rizicích se rozhodla v graviditě pokračovat. V průběhu těhotenství byly měřeny plazmatické koncentrace LCM matky v každém trimestru, byla stanovena koncentrace LCM při porodu v krvi matky a v pupečníkové krvi a dva týdny po porodu také třikrát v mateřském mléce (před podáním dávky 100 mg LCM a za 2 a 6 hodin po této dávce).
Jednalo se o pacientku bez známých
rizik pro fokální epilepsii, která prodělala ve věku od 14
do 23 let sporadické záchvatové příhody s poruchou
vědomí, o nichž nebylo zřejmé, jaké jsou etiologie. Ve 23
letech byl poprvé bez pochyb objektivizován fokální epileptický
záchvat s přechodem do bilaterálního tonicko klonického
(FBTCS). Ve standardním EEG nálezu byla zachycena
intermitentní pomalá aktivita frontotemporálně střídavě vlevo
nebo vpravo. Magnetická rezonance neodhalila strukturální lézi
mozku. Ambulantní neurolog diagnostikoval fokální epilepsii
a zahájil léčbu antiepileptiky. První volbou byl lamotrigin
(LTG) vytitrovaný na dávku 2× 50 mg denně. Pacientka
byla rok bez záchvatů, ale došlo ke zhoršení projevů
atopického ekzému. Po snížení dávky LTG o 25 mg
nastal relaps FBTCS. V dalším průběhu byla zvolena
sekvenční monoterapie levetiracetamem (LEV) s postupnou
titrací do 2 000 mg/den. Tato druhá volba byla dobře
tolerovaná, ale neúčinná (nemocná prodělala další tři
FBTCS). Až po přidání LCM záchvaty ustaly. Pacientka
kombinaci LEV + LCM dobře tolerovala. Po roce bez
záchvatů byla postupně převedena na monoterapii LCM
2× 100 mg denně. Při této dávce byla plazmatická
koncentrace LCM 19,7 µmol/l (referenční rozmezí 8‒40 µmol/l).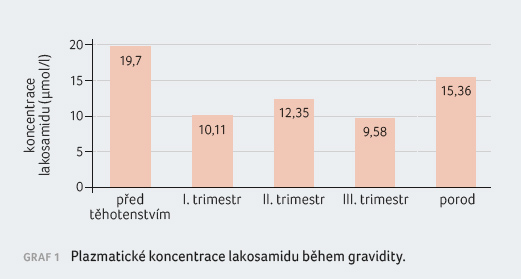
Pacientka otěhotněla a po diskusi
o rizicích se rozhodla v graviditě pokračovat. Byl
sledován klinický průběh, změny v EEG a změny
v plazmatické koncentraci LCM. Nemocná zůstala během
gravidity i po porodu bez záchvatů a bez
epileptiformní aktivity v EEG. Z hlediska měřené
plazmatické koncentrace LCM došlo v prvním trimestru
k poklesu na 10,1 µmol/l (51 % prekoncepční
koncentrace). Pacientka negovala non adherenci. V druhém
trimestru byla plazmatická koncentrace 12,4 µmol/l a 11,5 µmol/l
(63 % a 58 %). V třetím trimestru, šest týdnů před
porodem, pak koncentrace LCM poklesla na 9,6 µmol/l (49 %),
graf 1. V průběhu
spontánního porodu byla odebrána jak pupečníková krev, tak
periferní krev matky a byly stanoveny koncentrace LCM
16,7 µmol/l a 15,4 µmol/l (poměr 1,08). Narodil se zdravý
chlapec o hmotnosti 3 430 g, výšce 50 cm, s APGAR
skóre 10 10 10, obvod hlavičky 33 cm. Po zvážení
rizik a prospěchu kojení se pacientka rozhodla kojit. Dvacátý
den po porodu byla stanovena koncentrace LCM v mateřském
mléce před požitím 100 mg LCM, za 2 hodiny a za 6
hodin po požití. Hodnoty byly 14,3, 21,8 a 16,9 µmol/l,
graf 2.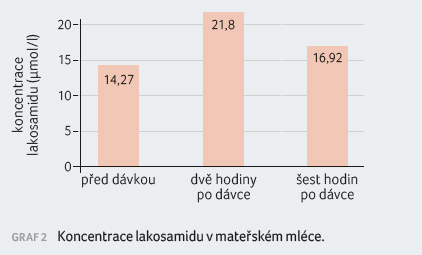
Diskuse
U této konkrétní pacientky můžeme diskutovat volbu LCM, léčivé látky prodlužující pomalou inaktivaci Na+ kanálu, pro léčbu její fokální epilepsie. Volba vycházela z potvrzené neúčinnosti LEV a naopak z účinnosti, ale nesnášenlivosti léku ovlivňujícího rychlou inaktivaci Na+ kanálu, LTG. Bylo důležité se vyhnout riziku opakování alergické reakce na jiná léčiva s podobným mechanismem účinku jako LTG (karbamazepin a eslikarbazepin). Pro další antiepileptika první a druhé volby k monoterapii fokálních záchvatů [3] s jinými mechanismy účinku existují data o zvýšené teratogenitě a kognitivních rizicích pro ženu s epilepsií (topiramát), nebo také není dostatek informací z hlediska bezpečnosti v graviditě (zonisamid). Gabapentin má nevýhodu nutnosti podávání třikrát denně a nižší účinnosti. Valproát není lékem volby pro ženy ve fertilním věku.
Ze zkušenosti zejména s LTG je známo, že změny farmakokinetiky léčiva v průběhu těhotenství mohou vést k významnému poklesu plazmatické koncentrace podávaného antiepileptika. Lakosamid je primárně metabolizován CYP2C19 demetylací v játrech na neaktivní O desmetyl metabolit (30 %) a přibližně 40 % LCM je vyloučeno prostřednictvím mechanismů renální exkrece [4]. Pokles plazmatické koncentrace LCM v graviditě může být rizikem pro relaps záchvatů. U referované pacientky došlo k prakticky 50% poklesu plazmatické koncentrace LCM již od prvního trimestru a k jejímu lehkému zvýšení až při porodu. Tento pokles nevedl ke zhoršení EEG nálezu ani ke klinickému relapsu záchvatů, a proto nebyla denní dávka LCM zvýšena. Je otázkou, zda by neměl být postup stejně proaktivní jako v současné době u LTG, zda titrovat denní udržovací dávku tak, aby se plazmatická koncentrace LCM v těhotenství blížila hodnotě prekoncepční.
Poměr koncentrace LCM v periferní krvi matky a v pupečníkové krvi ukazuje, že tato léčivá látka prostupuje ve sto procentech placentou. Novorozenec byl vystaven stejné koncentraci LCM, jaká byla v době porodu v periferní krvi matky.
Z hlediska koncentrace LCM v mateřském mléce bylo u pacientky zjištěno, že nejvyšší koncentrace bylo dosaženo dvě hodiny po užití jedné 100mg dávky, zatímco nejnižší byla doložena před užitím dávky. Ženám užívajícím během laktace LCM lze doporučit, aby se snažily nakojit před užitím dávky a poté co nejpozději po užití dávky.
Závěr
U námi popsané pacientky proběhla gravidita i laktace při monoterapii LCM bez komplikací. Pozorovali jsme významný pokles plazmatické koncentrace LCM od prvního trimestru. Sledování plazmatické koncentrace antiepileptik v graviditě je známým a důležitým preventivním opatřením proti relapsu záchvatů. Je otázkou, zda bude námi pozorovaný pokles plazmatické koncentrace LCM v graviditě potvrzen i u dalších žen. Sledování klinické, EEG a plazmatických koncentrací je možným postupem, jak optimalizovat péči o ženu s epilepsií v těhotenství [4].
Seznam použité literatury
- [1] Tomson T, Battino D, Bonizzoni E, et al. Comparative risk of major malformations with eight different antiepileptic drugs: a prospective cohort study of the EURAP registry. Lancet Neurol 2018; 17: 530‒538.
- [2] Lattanzi S, Cagnetti C, Foschi N, et al. Lacosamide during pregnancy and breastfeeding. Neurol Neurochir Pol 2017; 51: 266‒269.
- [3] Marusic P, a kol. Terapie epilepsie podle typu záchvatů v Souboru minimálních diagnostických a terapeutických standardů u pacientů s epilepsií. EpiStop 2017; 2.4: 22.
- [4] Jacob S, Nair AB. An updated Overview on Therapeutic Drug monitoring of Recent Antiepileptic Drugs. Drugs R D 2016; 16: 303‒316.