Léčba atopické dermatitidy dupilumabem
Souhrn:
Litvik R. Léčba atopické dermatitidy dupilumabem. Remedia 2020; 30: 592–595.
Atopická dermatitida (AD) je běžným zánětlivým kožním onemocněním, které postihuje dospělé a děti. Základem lokální léčby AD jsou emoliencia, kortikosteroidy a inhibitory kalcineurinu. Pro pacienty s těžší formou AD jsou využívána celková imunosupresiva. Dupilumab je prvním biologikem k léčbě AD. Jeho účinnost a bezpečnost byla prokázána mnoha klinickými studiemi.
Summary:
Litvik R. Treatment of atopic dermatitis with dupilumab. Remedia 2020; 30: 592–595.
Atopic dermatitis (AD) is a common, inflammatory skin disease affecting adults and children. Topical agents including emollients, corticosteroids and calcineurin inhibitors are the mainstay of AD therapy. For more severely affected subjects, systemically administered immunosuppressant drugs are used. Dupilumab is the first biologic available to treat AD. Its effectiveness and safety were demonstrated in many clinical trials.
Key words: atopic dermatitis, cytokines, dupilumab
Úvod do problematiky
Atopická dermatitida (AD) je chronické, recidivující, svědivé kožní onemocnění, které se vyznačuje suchou kůží a zánětlivou reakcí. Jedná se o nepřiměřenou reakci imunitního systému organismu na jinak zcela neškodné látky či podněty ze zevního prostředí, včetně potravy. U AD je situace dále komplikována současnou porušenou bariérovou funkcí kůže [1].
Toto chronické nebo chronicky recidivující onemocnění má výrazný dopad na kvalitu života nemocného i celé jeho rodiny. Proto se léčebná péče v současnosti zaměřuje na nové postupy, které by toto onemocnění zkrotily. Atopická dermatitida představuje chronické onemocnění, léčba proto musí tuto skutečnost zohlednit a měla by být plánována s dlouhodobou perspektivou. Základem terapie AD je vyvarování se specifických a nespecifických provokačních faktorů a pravidelná hydratace kůže emolienciem [1].
Emoliencia jsou nedílnou součástí léčby tohoto onemocnění, obnovují porušenou kožní bariéru, zabraňují ztrátám vody z horních vrstev kůže, zlepšují kapacitu vázat vodu v kůži a také přímo vodu do suchých vrstev kůže dodávají. Existují rovněž klinické studie, které prokazují kortikosteroidy šetřící účinek emoliencií. Emoliencia hrají v léčbě AD významnou roli [1].
Zcela zásadní je v léčbě AD protizánětlivá terapie lokálními kortikosteroidy (topical corticosteroids, TCS), lokálními imunomodulátory (inhibitory kalcineurinu), lokálními inhibitory fosfodiesterázy (IPDE) a lokálními inhibitory Janusových kináz [1‒3]. Lokální léčba u některých pacientů nevede ke kontrole AD, proto přichází na řadu fototerapie UV zářením (zejména 311 nm UVB) a systémová léčba kortikosteroidy, cyklosporinem A, metotrexátem, azatioprinem a mykofenolát mofetilem a inhibitory Janusových kináz. K systémové léčbě AD je určen pouze cyklosporin A, ostatní výše zmíněná imunosupresiva představují metody off label terapie AD nebo se jedná o léčbu dostupnou tč. pouze v klinických studiích (inhibitory Janusových kináz). Pacienti se středně těžkou a těžkou formou AD, kteří nedosáhli adekvátní kontroly AD za léčby cyklosporinem A nebo tuto léčbu netolerovali nebo u nich byla léčba cyklosporinem A kontraindikována, mohou být léčeni biologickou terapií dupilumabem [4].
Dupilumab
Dupilumab, rekombinantní lidská monoklonální protilátka třídy IgG4, inhibuje signální dráhu interleukinu (IL) 4 a IL 13. Tyto cytokiny hrají klíčovou roli v rozvoji zánětlivé reakce druhého typu (atopická dermatitida, asthma bronchiale a chronická rinosinusitida s nosní polypózou). Interleukiny 4 a 13 jsou tvořeny zejména Th2 lymfocyty, mastocyty, bazofily a eozinofily. Dupilumab inhibuje signální dráhy IL 4 prostřednictvím receptoru typu I (IL 4Rα/γC) a signální dráhu IL 4 a IL 13 prostřednictvím receptoru typu II (IL 4Rα/IL 13Rα1). Receptor I. typu je lokalizován zejména na povrchu hemopoetických buněk (B lymfocytů, T lymfocytů, monocytů, eozinofilů), zatímco II. typ receptoru je přítomen na povrchu epiteliálních buněk, buněk hladkých svalů a fibroblastů [4,5].
Interleukiny 4 a 13 jsou klíčovými cytokiny Th2 zánětu a jejich mechanismus účinku je komplexní. Zvyšují sekreci imunoglobulinu E (IgE) a prozánětlivých chemokinů (tymální stromální lymfopoetin, eotaxin 3, thymus and activation regulated chemokin [TARC]), atrahují zánětlivé buňky a Th2 lymfocyty do místa zánětu, inhibují diferenciaci keratinocytů a snižují expresi proteinů kožní bariéry (filaggrin, involukrin, lorikrin), negativně ovlivňují syntézu lipidů v epidermis a tvorbu antimikrobiálních peptidů. Samy o sobě jsou významnými pruritogeny. Mechanismus účinku IL 4 a IL 13 je tedy komplexní, obecně se oba cytokiny podílejí na udržení zánětu druhého typu v kůži a prohlubují poruchu již narušené kožní bariéry. To vede k zesílení zánětlivé reakce, která dále negativně ovlivní funkci kožní bariéry. Porucha kožní bariéry vede u AD k suchosti kůže, roztočení bludného kruhu suchost kůže – svědění – škrábání kůže, dochází tak k dalšímu zhoršení projevů AD a k udržení kožního zánětu druhého typu [4,5].
Dupilumab v léčbě atopické
dermatitidy
Atopická dermatitida je jako chronické recidivující zánětlivé onemocnění kůže asociována s poruchou kožní bariéry a se zánětem druhého typu (Th2). Až 20 % dospělých trpí středně těžkou a těžkou formou AD, která negativně ovlivňuje kvalitu života (svědění kůže, recidivy AD, poruchy nálady a spánku). Až 85 % těchto pacientů trpí svěděním kůže, které u 41,5 % z nich trvá déle než 18 hodin denně a jehož intenzita je 6,5 (na numerické škále od 0 do 10). Celkem 55 % těchto pacientů špatně spí (a to více než pět dnů v týdnu), jsou pak nevyspalí, v práci nevýkonní a trpí poruchami nálad [5].
Lékem první volby AD jsou emoliencia a lokální protizánětlivá léčiva. Systémová imunosupresiva (cyklosporin A) se využívají tehdy, pokud lokální léčba nevede ke kontrole onemocnění. Dupilumab je určen k léčbě středně těžké a těžké formy AD u dospělých a dospívajících starších 12 let, u nichž terapie cyklosporinem A nevedla ke kontrole onemocnění nebo byla tato léčba kontraindikována.
Doporučená úvodní dávka dupilumabu je u dospívajících pacientů (věk 12‒17 let a tělesná hmotnost nižší než 60 kg) 400 mg, následovaná dávkou 200 mg každý druhý týden formou subkutánní injekce. U dospělých pacientů je úvodní dávka 600 mg, následuje dávka 300 mg každý druhý týden formou subkutánní injekce. Dupilumab je možno používat v monoterapii nebo v kombinovaných léčebných režimech (spolu s lokálními kortikosteroidy nebo lokálními inhibitory kalcineurinu). U pacientů, kteří ani po 16 týdnech léčby nezaznamenají žádnou klinickou odpověď, by měla být tato terapie ukončena [4‒7].
Účinnost dupilumabu
Účinnost dupilumabu v léčbě AD v monoterapii nebo v kombinované terapii (s lokálními kortikosteroidy, lokálními imunomodulátory) byla prokázána mnoha randomizovanými, dvojitě zaslepenými klinickými studiemi kontrolovanými placebem. Tyto studie hodnotily krátkodobou i dlouhodobou účinnost dupilumabu. Všechna hodnocení prokázala statisticky významné zlepšení jak projevů AD, tak subjektivních pocitů a kvality života léčených pacientů.
Studie SOLO 1, SOLO 2 a LIBERTY AD CHRONOS celkem zhodnotily 2 119 léčených pacientů (SOLO 1: n = 671; SOLO 2: n = 708; LIBERTY AD CHRONOS: n = 740). Do studií byli zařazeni dospělí pacienti se středně těžkou a těžkou formou AD. Ve všech zmíněných klinických studiích byly sledovány společné cílové parametry. Jednalo se o procentní podíl pacientů s hodnotou IGA (Investigator Global Assessment) 0 nebo 1 (kompletní odhojení AD, resp. téměř odhojené projevy AD), u nichž došlo k jejímu snížení o ≥ 2 na škále IGA od 0 do 4, a o podíl pacientů se zlepšením podle skóre EASI (Eczema Area and Severity Index) o nejméně 75 % v 16. týdnu léčby ve srovnání s výchozí hodnotou (EASI 75). Dalšími hodnocenými parametry byly zlepšení skóre EASI alespoň o 50 % (EASI 50), resp. 90 % (EASI 90), zmírnění svědění měřené numerickou škálou od 0 do 10 a procentuální změna parametru SCORAD (SCORing Atopic Dermatitis) v 16. týdnu ve srovnání s výchozí hodnotou. Byla rovněž měřena kvalita života léčených pacientů (Dermatology Life Quality Index, DLQI).
Studiemi SOLO 1 a SOLO 2 byla po šestnáctitýdenní monoterapii dupilumabem (úvodní dávka 600 mg dupilumabu subkutánně s udržovací léčbou 300 mg dupilumabu subkutánně každé dva týdny) prokázána srovnatelná a vyšší účinnost dupilumabu v obou hodnoceních oproti placebu. Odpověď na léčbu hodnocená parametrem IGA činila 36‒38 % vs. 8‒10 % v rameni s placebem. Rovněž procentuální zastoupení respondérů na níže uvedené parametry bylo v obou studiích podobné: EASI 75 (44,2‒51,3 %) vs. placebo (11,9‒14,7 %), resp. EASI 90 (30,0‒35,7 %) vs. placebo (30,0‒35,7 %). Srovnatelný byl také podíl pacientů, kteří dosáhli jak signifikantní změny indexu EASI proti výchozí hodnotě (‒67,1 %, resp. ‒72,3 %), tak signifikantní změny indexu SCORAD proti výchozí hodnotě (‒51,1 %, resp. ‒57,7 %). Signifikantní zmírnění svědění bylo v obou studiích spojeno s ústupem objektivních i subjektivních příznaků AD (průměrná změna hodnoty svědění na numerické škále: ‒44,3 %, resp. ‒51 %) oproti placebu. Průměrná procentuální změna na základě DLQI činila oproti výchozí hodnotě ‒9,3 % vs. ‒3,6 %, resp. ‒5,3 % v rameni s placebem [6‒9].
Studie LIBERTY AD CHRONOS zhodnotila cílové parametry v 16. a 52. týdnu kombinované léčby s TCS. Léčba zahrnovala úvodní dávku 600 mg dupilumabu subkutánně s udržovací léčbou 300 mg dupilumabu subkutánně každé dva týdny a lokálně aplikované kortikosteroidy vs. placebo a lokálně aplikované kortikosteroidy. Odpověď na léčbu hodnocená parametrem IGA činila 38,7 % vs. 12,4 % v rameni s placebem a TCS (16. týden), resp. 36 % vs. 12,5 % v rameni s placebem a TCS (52. týden). Hodnocení EASI 75/90 v 16. týdnu odpovídalo 68,9 %/39,6 % oproti 23,2 %/11,1 % v rameni s placebem a TCS. V 52. týdnu vykázalo EASI 75/90 hodnotu 65,2 %/50,6 % oproti 21,6 %/15,5 % v rameni s placebem a TCS.
Podíl pacientů, kteří dosáhli signifikantní změny indexu EASI proti výchozí hodnotě, činil ‒80,5 % vs. ‒48,4 % v rameni s placebem a TCS v 16. týdnu, ‒84,9 % vs. ‒60,9 % v rameni s placebem a TCS v 52. týdnu. Podíl nemocných, kteří dosáhli signifikantní změny indexu SCORAD proti výchozí hodnotě, činil v 16. týdnu ‒63,9 % vs. ‒36,2 % v rameni s placebem a TCS, v 52. týdnu ‒69,7 % vs. ‒47,3 % v rameni s placebem a TCS. Signifikantní zmírnění svědění bylo v obou hodnoticích týdnech spojeno se zmírněním objektivních i subjektivních příznaků AD ‒ průměrná změna hodnoty svědění na numerické škále v 16. týdnu: ‒56,6 %, resp. v 52. týdnu ‒57 % vs. ‒30,3 % (16. týden) a ‒31,7 % (52. týden) v rameni s placebem a TCS [6‒9].
Pacienti ve studii LIBERTY AD CAFÉ, kteří dostatečně nereagovali na léčbu cyklosporinem A nebo jej z lékařských důvodů nemohli užívat, vykázali hodnotu EASI 75 v rameni s dupilumabem a TCS 62,6 % oproti 29,6 % v rameni s placebem a TCS [10].
Studie LIBERTY AD OLE zhodnotila dlouhodobou účinnost léčby dupilumabem ve 148. týdnu. Sledování prokázalo dlouhodobou výbornou účinnost dupilumabu v léčbě AD. V týdnu 148 dosáhlo kompletního nebo téměř kompletního odhojení (IGA 0 nebo 1) 74,1 % pacientů, výchozí průměrná hodnota EASI poklesla z 33,4 na 1,5. V týdnu 148 rovněž poklesla průměrná hodnota svědění (měřeno na numerické škále) z výchozích 7,2 na 2,1. Ve 148. týdnu dosáhlo EASI 50/75/90 celkem 98,3 %, 96,6 % a 87,9 % léčených pacientů [11].
V klinických studiích není
hodnoceno pouze zlepšení kožního nálezu, zmírnění
subjektivních a objektivních příznaků pacientů léčených
dupilumabem, ale efekt na subbuněčné a buněčné
úrovni. Dupilumab působí duální inhibici IL 4 a IL 13,
což vede k účinnému ovlivnění zánětlivé reakce typu 2
se snížením hodnot biomarkerů zánětu typu 2 v centrálním
kompartmentu (séru): chemokiny CCL17 (C C motif ligand,
označovaný také jako TARC) a CCL18, periostin, celkového
množství IgE a také množství specifických IgE. Rovněž
dochází k příznivému ovlivnění epidermální diferenciace
s příznivým účinkem na kožní bariéru (zvýšená
exprese filaggrinu, lorikrinu a klaudinů) a epidermální
metabolismus lipidů. Tato histologická a sekundárně pak
klinická zlepšení korelují s modulací exprese příslušných
genů po účinné blokádě zánětlivé reakce typu 2 [12].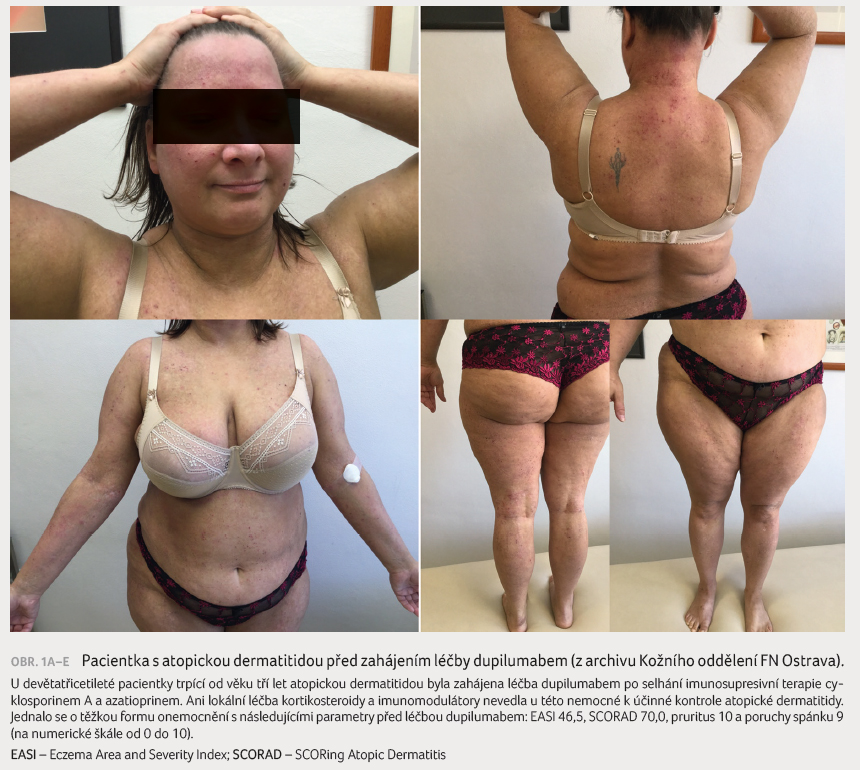
Doklad o účinnosti léčby dupilumabem přináší také popis případu z Kožního oddělení FN Ostrava (obr. 1A‒E, 2A‒E).
Bezpečnost léčby dupilumabem
Nejčastějšími nežádoucími účinky
léčby dupilumabem jsou reakce v místě aplikace, rozvoj
očních potíží (syndrom suchého oka, konjunktivitida,
blefaritida, keratitida) a infekce virem herpes simplex. Všechny
klinické studie vykázaly zvýšenou četnost očních nežádoucích
účinků oproti placebu. Mechanismus vzniku dupilumabem indukované
konjunktivitidy není zcela jasný. Hypotézami jsou zvýšená
aktivita ligandu OX40L daná blokádou signálních cest IL 4/IL 13
nebo role eozinofilů, jejichž počet se u pacientů léčených
dupilumabem přechodně zvyšuje. Do jaké míry tyto faktory
skutečně souvisejí se zvýšenou incidencí konjunktivitidy
navozené dupilumabem, je nutno ještě dále prokázat [13].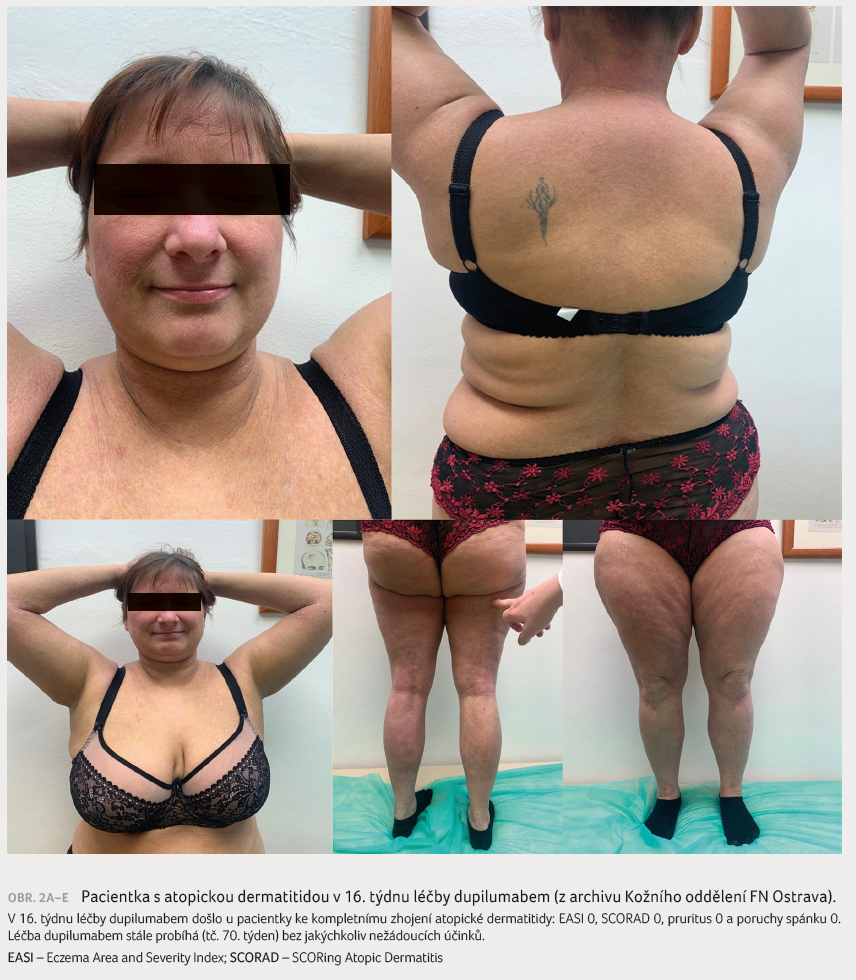
Závěr
Dupilumab je v dermatologii určen k léčbě pacientů se středně těžkou a těžkou formou AD, u kterých selhala celková léčba cyklosporinem A a/nebo u kterých léčba cyklosporinem byla kontraindikována a/nebo byla tato léčba pro nežádoucí účinky ukončena. Dupilumab působí duální inhibici IL 4 a IL 13, což vede k účinnému ovlivnění zánětlivé reakce typu 2. Dochází jak k příznivému ovlivnění kůže, tak k poklesu hodnot systémových biomarkerů zánětu typu 2 v séru. Účinnost a bezpečnost léčby AD dupilumabem byla prokázána četnými krátkodobými i dlouhodobými studiemi. Výzkum v oblasti ovlivnění zánětlivé reakce typu 2 nadále trvá, mnohé další molekuly čekají na vyhodnocení účinnosti v klinických studiích.
Seznam použité literatury
- [1] Litvik R. Atopický ekzém v dospělém věku. In Dermatologie v kazuistikách. Praha: Mladá fronta, 2008.
- [2] Jarnagin K, Chanda S, Coronado D, et al. Crisaborole Topical Ointment, 2% A Nonsteroidal, Topical, Anti‑Inflammatory Phosphodiesterase 4 Inhibitor in Clinical Development for the Treatment of Atopic Dermatitis. J Drugs Dermatol 2016; 15: 390‒396.
- [3] Chaplin S. Janus kinase inhibitors for autoimmune disorders. Prescriber 2017; 28: 33‒37.
- [4] Ferreira S, Torres T. Dupilumab for the treatment of Atopic Dermatitis. Actas Dermosifiliorg 2018; 109: 230‒240.
- [5] Matsunaga K, Katoh N, Fuieda S, et all. Dupilumab: Basic aspects and applications to allergic diseases. Allergol Int 2020; 69: 187‒196.
- [6] Beck LA, Thaçi D, Hamilton JD, et al. Dupilumab Treatment in Adults with Moderate‑to‑Severe Atopic Dermatitis. N Engl J Med 2014; 371: 130‒139.
- [7] Simpson EL, Bieber T, Guttman‑Yassky E, et al. Two Phase 3 Trials of Dupilumab versus Placebo in Atopic Dermatitis. N Engl J Med 2016; 375: 2335‒2348.
- [8] Wang C, Kraus Ch, Patel K, et al. Real‑world experience of dupilumab treatment for atopic dermatitis in adults: a retrospective analysis of patientsʼ records. Int J Dermatol 2020; 59: 253‒256.
- [9] Chaplin S. Dupilumab for the treatment of atopic dermatitis. Prescriber 2018; 29: 35‒37.
- [10] de Bruin‑Weller M, Thaçi D, Smith CH, et al. Dupilumab with concomitant topical corticosteroid treatment in adults with atopic dermatitis with an inadequate response or intolerance to ciclosporin A or when this treatment is medically inadvisable: a placebo‑controlled, randomized phase III clinical trial (LIBERTY AD CAFÉ). Br J Dermatol 2018; 178: 1083‒1101.
- [11] Beck L, Thaçi D, Deleuran M, et al. Dupilumab Provides Favorable Safety and Sustained Efficacy for up to 3 Years in an Open‑Label Study of Adults with Moderate‑to‑Severe Atopic Dermatitis. Am J Clinical Dermatol 2020; 21: 567‒577.
- [12] Guttman‑Yassky E, Bissonnette R, Ungar B, et al. Dupilumab progressively improves systemic and cutaneous abnormalities in patients with atopic dermatitis. J Allergy Clin Immunol 2019; 143: 155‒172.
- [13] Aszodi N, Thurau S, Seegräber M, et al. Management of dupilumab‑associated conjunctivitis in atopic dermatitis. J Dtsch Dermatol Ges 2019; 17: 488‒491.