Nové možnosti aplikace sekukinumabu (studie ALLURE a MATURE)
Souhrn:
Nečas M. Nové možnosti aplikace sekukinumabu (studie ALLURE a MATURE). Remedia 2022; 32: 419–424.
Do léčby závažné ložiskové psoriázy vstupují nové biologické přípravky, u nichž je kladen důraz nejen na účinnost a bezpečnost, ale také na co nejvyšší míru komfortu pacientů. To znamená možnost aplikovat léčbu v pohodlí domova, jednoduše a s co nejmenším počtem injekcí. V případě sekukinumabu došlo v rámci nových aplikačních forem ke snížení počtu injekcí na polovinu a dávku 300 mg lze aktuálně podat pouze v jedné aplikaci. Výsledky studií ALLURE a MATURE potvrdily, že tato inovace zvyšuje pohodlí pacientů a nemá negativní vliv na účinnost a bezpečnost léčby sekukinumabem.
Summary:
Necas M. The new options concerning secukinumab use (trials ALLURE and MATURE). Remedia 2022; 32: 419–424.
New biological drugs are being launched in the treatment of severe focal psoriasis while beside effectiveness and safety, the highest possible comfortability for the patients is aimed for. Above all, this means the possibility to apply the drugs at home, easily and using the least rational frequency of injections. In case of secukinumab, the frequency of injections was halved thanks to the new application devices and the 300mg dose may now be applied at a single time. The results of the ALLURE and MATURE trials have confirmed that the above innovations improve patient comfort without compromising the effectiveness and safety of secukinumab treatment.
Key words: psoriasis, secukinumab, application device, ALLURE trial, MATURE trial.
Úvod
Léčebné možnosti závažné ložiskové psoriázy se stále rozšiřují a u nových biologických přípravků je kladen důraz nejen na účinnost, bezpečnost a dlouhodobou zkušenost, ale také na co nejvyšší míru komfortu pacientů při této léčbě. To zahrnuje mimo jiné i možnost aplikovat léčbu v pohodlí domova, jednoduše a s co nejmenším počtem injekcí. Uvedený trend se aktuálně týká také sekukinumabu, u nějž došlo v rámci nových aplikačních forem ke snížení počtu injekcí na polovinu [1]. Dávku 300 mg přípravku je nově možné podat nikoliv ve dvou aplikacích, jak tomu bylo dosud, ale pouze v jediné [1]. Zda tato inovace přináší větší pohodlí pro pacienty a nemá negativní vliv na účinnost a bezpečnost léčby, zkoumaly studie ALLURE (s použitím předplněné 2ml injekční stříkačky obsahující dávku 300 mg sekukinumabu) a MATURE (za použití autoinjektoru UnoReady 300 mg pen). S výsledky obou těchto studií seznamuje následující sdělení.
Studie ALLURE
ALLURE byla 52týdenní randomizovaná,
dvojitě zaslepená, placebem kontrolovaná studie fáze III
s paralelními skupinami, která sestávala ze čtyř
period: screeningu (trvání do čtyř týdnů), léčebné
periody 1 (12 týdnů), léčebné periody 2 (40 týdnů)
a období následného sledování (follow up) bez léčby
(osm týdnů), jež však bylo realizováno pouze v případě,
že došlo k předčasnému ukončení léčby. Uspořádání
studie ukazuje obrázek 1 [2].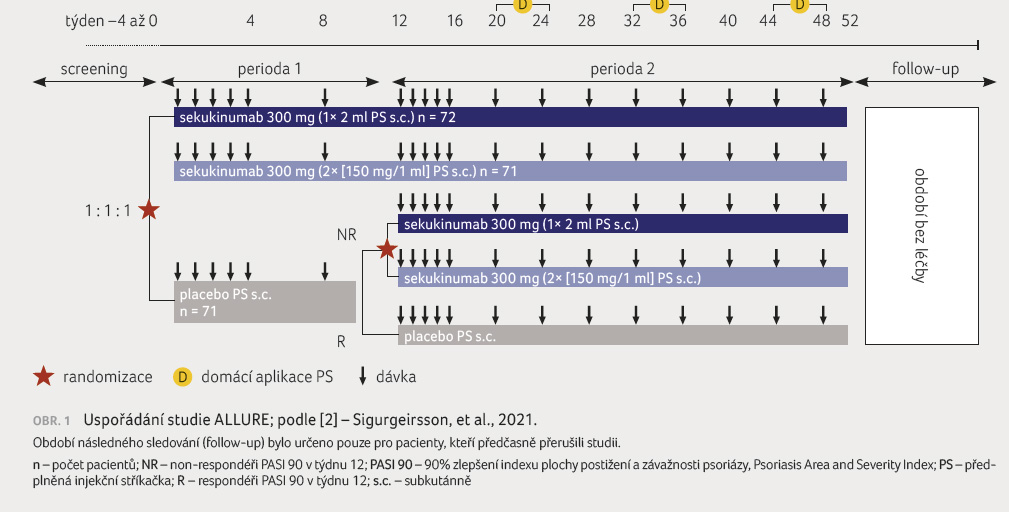
Cílem studie bylo zhodnocení
účinnosti, farmakokinetiky a snášenlivosti sekukinumabu
v dávce 300 mg podávané subkutánně v jedné
předplněné stříkačce o objemu 2 ml u pacientů se
středně závažnou až závažnou ložiskovou psoriázou.
Primárními cílovými ukazateli byly dosažení indexu PASI 75
(75% zlepšení indexu plochy postižení a závažnosti
psoriázy, Psoriasis Area and Severity Index) a modifikovaného
skóre IGA 0/1 (IGA mod 2011; Investigator’s Global Assessment).
Klíčové sekundární ukazatele zahrnovaly PASI 90 a PASI 100
v týdnu 12. Do studie bylo zařazeno 214 pacientů,
z nichž 209 (97,7 %) dokončilo periodu 1, 198 (92,5 %)
pacientů dokončilo periody obě [2]. Sekukinumab v dávce
300 mg v předplněné stříkačce byl účinnější oproti
placebu v parametru IGA mod 2011 (76,4 % vs. 1,4 %;
p < 0,0001) a PASI 75 (88,9 % vs.
1,7 %; p < 0,0001), PASI 90 i PASI
100 v týdnu 12 [2]. Léčba v obou ramenech
sekukinumabu (dávka 1× 300 mg i 2× 150 mg)
vykazovala přibližně stejnou účinnost, která narůstala až
do týdne 28 a poté se udržovala na stejné úrovni
až do týdne 52 (graf 1A–D) [2].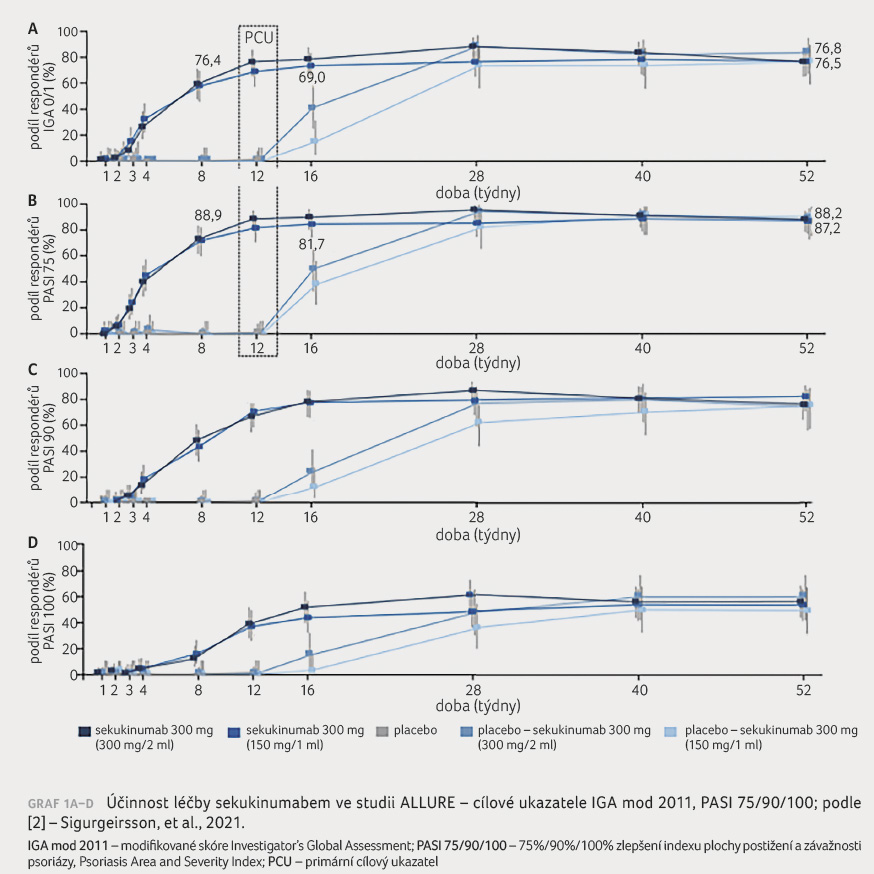
Co se týče bezpečnosti a snášenlivosti, rozdíly mezi oběma léčebnými rameny nebyly zjištěny a nebyly také zjištěny žádné nové bezpečnostní signály. Nejčastějšími nežádoucími účinky byly nazofaryngitida, bolesti hlavy, pruritus a bolesti zad. Výskyt reakcí v místě vpichu byl nízký (5,6 %), tabulka 1 [2].
Spokojenost pacientů s léčbou
sekukinumabem vzrostla z 52,1 % na začátku studie
na 87,5 % v týdnu 28. Přibližně 88 % pacientů
zvládlo hned od začátku (počáteční období a týden
1) bez problémů aplikovat sekukinumab pomocí předplněné
stříkačky [3].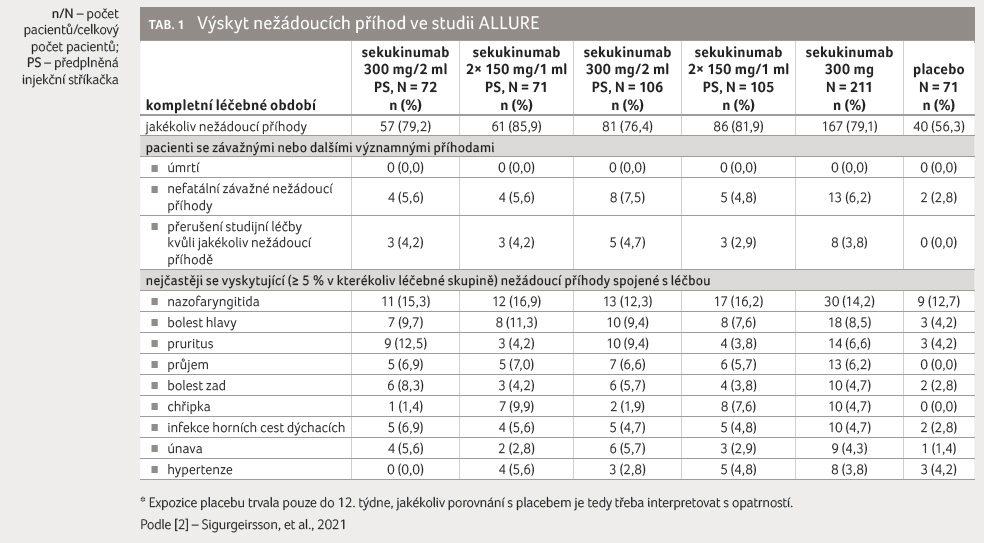
Léčba sekukinumabem podávaným v jedné dávce 300 mg v předplněné stříkačce byla bezpečná, s minimem reakcí v místě vpichu, s rychlým nástupem účinku a byla výrazně účinnější oproti placebu. V obou léčebných ramenech byly účinnostní i farmakokinetické parametry srovnatelné [4].
Studie MATURE
MATURE byla 52týdenní multicentrická,
randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie
fáze III u pacientů se středně závažnou až závažnou
psoriázou. Pacienti byli randomizováni do paralelních skupin,
kde dostávali buď sekukinumab v jedné dávce 300 mg
aplikované autoinjektorem, placebo, nebo sekukinumab ve dvou
předplněných injekcích po 150 mg. Tato studie probíhala
ve 22 centrech po celém světě (Německo, Polsko,
Španělsko, Island, Spojené státy americké a Kanada)
v období od prosince 2018 do srpna 2020. Zahrnovala
celkem 122 pacientů. Cílem studie bylo zhodnocení účinnosti,
bezpečnosti, snášenlivosti a farmakokinetiky sekukinumabu
podávaného v jedné dávce 300 mg subkutánně
autoinjektorem u pacientů se středně závažnou až závažnou
ložiskovou psoriázou. Uspořádání studie ukazuje obrázek 2
[5].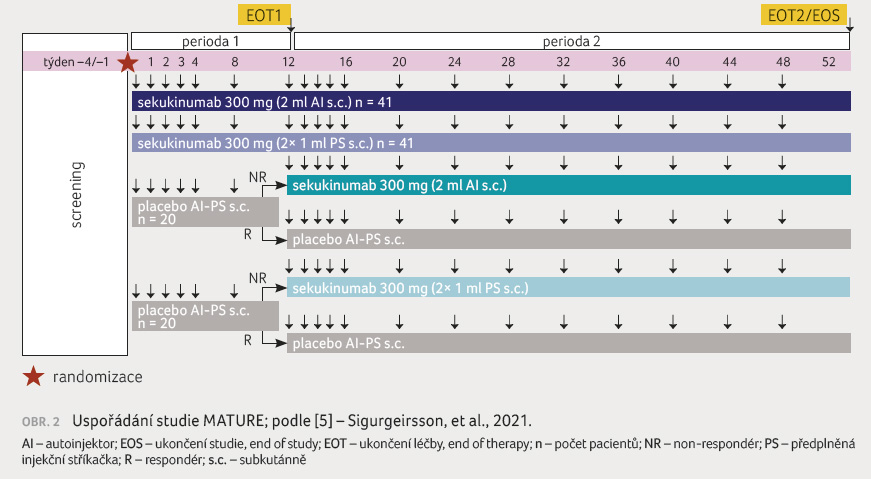
V obou léčebných ramenech byla
účinnost srovnatelná, numericky o něco vyšší u pacientů
léčených 300 mg sekukinumabu v jedné dávce podávané
autoinjektorem (graf 2) [5]. Sérové koncentrace
sekukinumabu byly mírně vyšší ve skupině pacientů
léčených autoinjektorem než ve skupině léčené
předplněnými stříkačkami (2× 150 mg), graf 3 [6].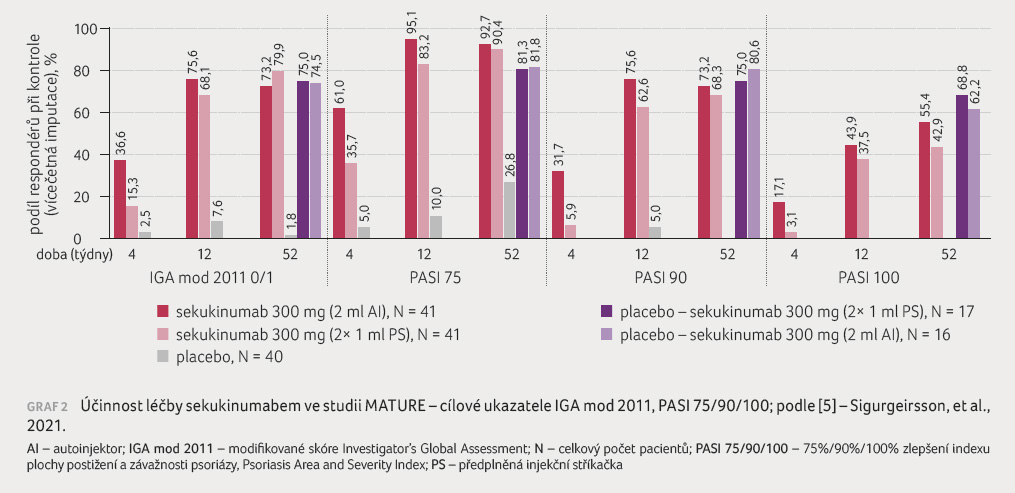
Co se týče kvality života, zřetelně
vyšší podíl pacientů dosáhl v týdnu 12 skóre DLQI
(Dermatology Life Quality Index) 0 nebo 1 (žádné nebo minimální
negativní ovlivnění kvality života) ve skupinách osob
léčených sekukinumabem (71,1 % ve skupině
s autoinjektorem, resp. 72,5 % ve skupině s injekcemi)
oproti skupině léčené placebem (8,1 %) a tyto hodnoty
přetrvávaly až do týdne 52 [5]. Co se týče jednoduchosti
použití, téměř 96 % pacientů bylo bez problémů schopno si
aplikovat první dávku autoinjektorem dle přiložených informací
k použití a spokojenost s používáním
autoinjektoru postupně narůstala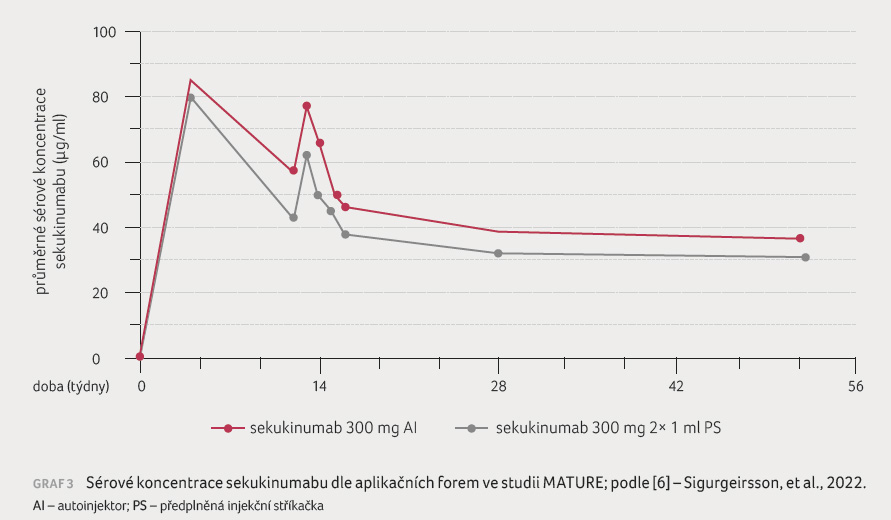 z 31,6 % na začátku
na 100 % v týdnu 28 (z toho 67,6 % osob bylo
velmi spokojených a 33,4 % spokojených) [6]. V průběhu
studie se neobjevily žádné nové negativní bezpečnostní
signály, pouze dva pacienti (1,7 %) udávali reakci v místě
vpichu autoinjektorem (z toho jeden měl sekukinumab a druhý
placebo). Obě reakce byly mírného stupně a nevedly
k přerušení, nebo dokonce ukončení studie [6]. Opět nebyly
identifikovány žádné nové bezpečnostní signály, nejčastějšími
nežádoucími účinky byly nazofaryngitida a infekce horních
cest dýchacích (tab. 2) [6].
z 31,6 % na začátku
na 100 % v týdnu 28 (z toho 67,6 % osob bylo
velmi spokojených a 33,4 % spokojených) [6]. V průběhu
studie se neobjevily žádné nové negativní bezpečnostní
signály, pouze dva pacienti (1,7 %) udávali reakci v místě
vpichu autoinjektorem (z toho jeden měl sekukinumab a druhý
placebo). Obě reakce byly mírného stupně a nevedly
k přerušení, nebo dokonce ukončení studie [6]. Opět nebyly
identifikovány žádné nové bezpečnostní signály, nejčastějšími
nežádoucími účinky byly nazofaryngitida a infekce horních
cest dýchacích (tab. 2) [6].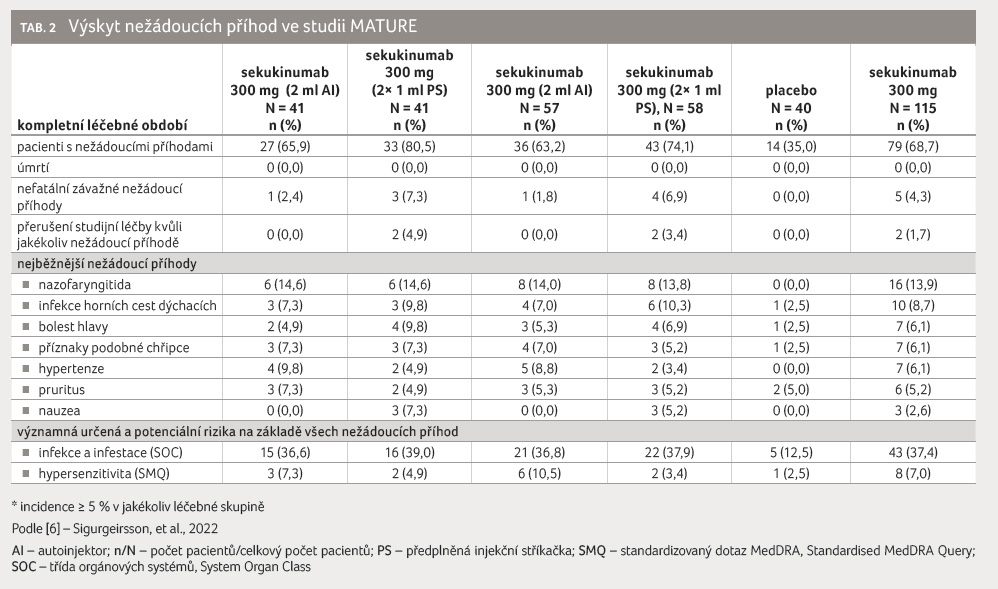
Ve studii MATURE tedy sekukinumab v dávce 300 mg podávaný subkutánně ve formě autoinjektoru pro jednorázovou aplikaci prokázal vysokou účinnost oproti placebu, dobrou snášenlivost a velmi snadné použití pro pacienty [6].
Závěr
Obě zmíněné studie prokázaly, že nové aplikační formy sekukinumabu (předplněná stříkačka s obsahem 300 mg sekukinumabu o objemu 2 ml a předplněné pero UnoReady 300 mg) mají minimálně stejnou účinnost jako předchozí aplikační formy, nenesou s sebou žádné nové nežádoucí bezpečnostní signály a jejich tolerabilita je výborná. Navíc snížení počtu nutných aplikací léčiva na polovinu výrazným způsobem zvyšuje komfort pacientů při podávání této terapie, a tím i celkovou spokojenost pacientů a adherenci k léčbě.
Seznam použité literatury
- [1] SPC Cosentyx. Dostupné na: https://www.sukl.cz
- [2] Sigurgeirsson B, et al. AAD Annual Meeting 2021 (P27519).
- [3] Novartis DOF. CAIN457A2325 Data Analysis Report. Satisfaction with self‑injection. December 2020.
- [4] Sigurgeirsson B, Schäkel K, Hong CH, et al. Efficacy, tolerability, patient usability, and satisfaction with a 2 mL pre‑filled syringe containing secukinumab 300 mg in patients with moderate to severe plaque psoriasis: results from the phase 3 randomized, double‑blind, placebo‑controlled ALLURE study. J Dermatolog Treat 2022; 33: 1718–1726.
- [5] Sigurgeirsson B, Browning J, Tyring S, et al. High efficacy, safety, and tolerability of secukinumab injection with 2 mL auto‑injector (300 mg) in adult patients with moderate to severe plaque psoriasis: 52‑week results from MATURE, a randomized, placebo‑controlled trial. Presented at EADV 30th Annual Congress 2021 (P1302).
- [6] Sigurgeirsson B, Browning J, Tyring S, et al. Secukinumab demonstrates efficacy, safety, and tolerability upon administration by 2 ml autoinjector in adult patients with plaque psoriasis: 52‑week results from MATURE, a randomized, placebo‑controlled trial. Dermatol Ther 2022; 35: e15285.