Studie DECLARE rozšiřuje indikace inhibitorů SGLT2
Souhrn:
Špinar J, Špinarová L. Studie DECLARE rozšiřuje indikace inhibitorů SGLT2. Remedia 2019; 29: 144–146.
V listopadu 2018 byly na kongresu Americké kardiologické asociace prezentovány výsledky studie DECLARE, která srovnávala dapagliflozin versus placebo u nemocných s diabetes mellitus 2. typu. Studie zařadila 17 160 nemocných s diabetes mellitus 2. typu, kteří byli randomizováni k podávání placeba nebo k léčbě dapagliflozinem v dávce 10 mg/den. Průměrný věk nemocných byl 63,8 ± 6,8 roku, průměrná doba trvání diabetu 11,8 ± 7,8 roku, průměrná hodnota glykovaného hemoglobinu 8,3 ± 1,2 %. Celkem 6 971 (40,6 %) nemocných mělo potvrzené kardiovaskulární onemocnění a 10 189 (59,4 %) vícečetné rizikové faktory. Ve výskytu primárního bezpečnostního cílového ukazatele dapagliflozin prokázal non‑inferioritu. Ve dvou účinnostních cílových ukazatelích byl při podávání dapagliflozinu zaznamenán menší výskyt tzv. velkých kardiovaskulárních příhod (MACE), 8,8 % u dapagliflozinu a 9,4 % u placeba (p = 0,17), nižší počet hospitalizací pro srdeční selhání a kardiovaskulární mortalitu (4,9 % vs. 5,8 %, p = 0,005). Výskyt renálního složeného cílového ukazatele představoval 4,3 % při léčbě dapagliflozinem vs. 5,6 % při podávání placeba a počet úmrtí z jakékoliv příčiny 6,2 % vs. 6,6 %, vše ve prospěch dapagliflozinu. Je velmi pravděpodobné, že výsledky studie DECLARE povedou ke změně guidelines, kdy inhibitory SGLT2 mohou získat indikaci k léčbě srdečního selhání a diabetes mellitus Ia,A, neboť máme k dispozici již minimálně dvě velké ukončené mortalitní studie.
Summary:
Spinar J, Spinarova L. DECLARE study widens the indication for SGLT2 inhibitors. Remedia 2019; 29: 144–146.
DECLARE is an international clinical trial with dapagliflozin and the final results were presented at the congress of American Heart Association (AHA) in November 2018. The study included 17,160 patients with diabetes mellitus type 2 who were randomised on placebo or dapagliflozin 10mg/daily. Mean age was 63.8 + 6.8 years, mean duration of diabetes 11.8 + 7.8 years, mean glycated haemoglobin 8.3% + 1.2%. Total 6,971 (40.6%) were patients with confirmed cardiovascular disease (CVD), 10,189 (59,4%) were patients with multiple risk factors (MRF). In the primary safety outcome analysis, dapagliflozin met the pre‑specified criterion for non‑inferiority to placebo with respect to MACE (8.8% dapagliflozin vs 9.4% placebo, p = 0.17) In the primary efficacy outcome dapagliflozin did result in a lower rate of cardiovascular deaths or hospitalisation for heart failure (4.9% vs 5.8%). A renal event occurred in 4.3% in the dapagliflozin group and in 5.6% in the placebo group and death from any cause occurred in 6.2% and 6.6% – all beneficial for dapagliflozin. It is expected that these data will change the guidelines for SGLT2 in the treatment of diabetes mellitus and heart failure to Ia, A because there are two finished mortality studies.
Key words: dapagliflozin, DECLARE, mortality, heart failure
Vstupní charakteristiky
Na kongresu Americké kardiologické asociace, který se konal 10.–12. listopadu 2018 v Chicagu, byly prezentovány výsledky studie DECLARE s dapagliflozinem u nemocných s diabetes mellitus v primární či sekundární prevenci ischemické choroby srdeční a současně byly publikovány v časopise New England Journal of Medicine. Studie DECLARE zařadila 17 160 nemocných s diabetes mellitus 2. typu, kteří byli randomizovaně rozděleni do skupin s léčbou dapagliflozinem v dávce 10 mg/den nebo s podáváním placeba. Průměrný věk nemocných byl 63,8 ± 6,8 roku, průměrná doba trvání diabetu 11,8 ± 7,8 roku, průměrná hodnota glykovaného hemoglobinu (HbA1c) 8,3 ± 1,2 %. U 6 971 (40,6 %) nemocných bylo potvrzeno kardiovaskulární onemocnění (tzv. skupina CVD, cardiovascular disease group) a u 10 189 (59,4 %) byly přítomny vícečetné rizikové faktory (tzv. skupina MRF, multiple risk factor group). Pacienti s kardiovaskulárním onemocněním byli častěji muži (72,1 % vs. 56,1 %) a měli podobnou délku trvání diabetes mellitus (12,0 roku vs. 11,7 roku) [1,2].
Ve skupině s kardiovaskulárním onemocněním byl častěji podáván metformin a derivát sulfonylurey než ve skupině s rizikovými faktory a byl zde také častěji podáván inzulin (44,2 % vs. 36,4 %). Často byla podávána antihypertenziva, výrazně častější byla ve skupině CVD léčba betablokátory oproti skupině MRF (66,6 % vs. 32,3 %). Ve skupině CVD byla taktéž více podávána antiagregační a antikoagulační terapie (kyselina acetylsalicylová 71,1 % vs. 39,1 %, klopidogrel 24,7 % vs. 1,5 %, warfarin 6,1 % vs. 3,5 %).
Předchozí infarkt myokardu, angioplastika nebo bypass byly hlášeny u 20,9 %, 21,3 % a 9,8 % z celé sledované populace a u skupiny CVD v 51,4 %, 52,4 % a 24,1 %. Překvapivě minimální rozdíly mezi oběma skupinami byly v hodnotách krevního tlaku a lipidů. Clearance kreatininu < 60 ml/min (podle Cocrofta Goulta) byla vylučovacím kritériem, průměrná odhadovaná glomerulární filtrace (eGFR, podle MDRD kalkulace) byla 86,1 ± 21,8 ml/min/1,73 m2.
Během tzv. run in periody bylo zařazeno 25 698 nemocných, ze kterých 17 160 splnilo vstupní kritéria. Celkem 3 962 nemocných ukončilo studii předčasně, ze skupiny s dapagliflozinem 1 811 z 8 574 zařazených (21,1 %), z placebové větve 2 151 z 8 569 (25,1 %) pacientů a celková doba sledování dosáhla 69 547 pacientských let.
Výsledky hodnocení
Dapagliflozin prokázal pozitivní
efekt na různé kardiovaskulární rizikové faktory:
u pacientů léčených dapagliflozinem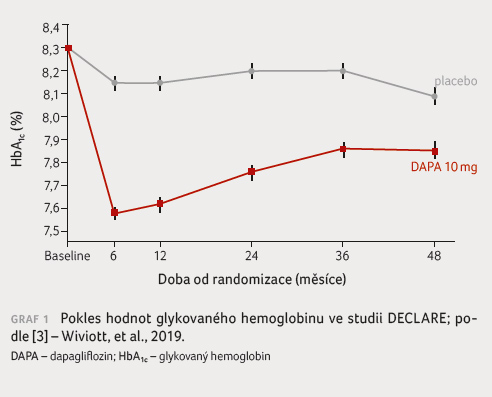 byly zaznamenány nižší
hodnoty HbA1c (graf 1)
[3]. Během studie bylo navíc 9,5 % nemocných ve skupině
s dapagliflozinem a 11,4 % ve skupině placeba
léčeno analogy GLP 1. Otevřenou léčbu SGLT2 dostalo
ve skupině dapagliflozinu 3,4 % nemocných, zatímco
ve skupině placeba 6,1 %. Nemocní léčení dapagliflozinem
měli nižší hmotnost (o 1,8 kg), nižší systolický
krevní tlak (o 2,7 mm Hg), graf 2, a nižší diastolický krevní tlak
(o 0,7 mm Hg).
byly zaznamenány nižší
hodnoty HbA1c (graf 1)
[3]. Během studie bylo navíc 9,5 % nemocných ve skupině
s dapagliflozinem a 11,4 % ve skupině placeba
léčeno analogy GLP 1. Otevřenou léčbu SGLT2 dostalo
ve skupině dapagliflozinu 3,4 % nemocných, zatímco
ve skupině placeba 6,1 %. Nemocní léčení dapagliflozinem
měli nižší hmotnost (o 1,8 kg), nižší systolický
krevní tlak (o 2,7 mm Hg), graf 2, a nižší diastolický krevní tlak
(o 0,7 mm Hg).
Dapagliflozin splnil předdefinované
kritérium pro non inferioritu pro MACE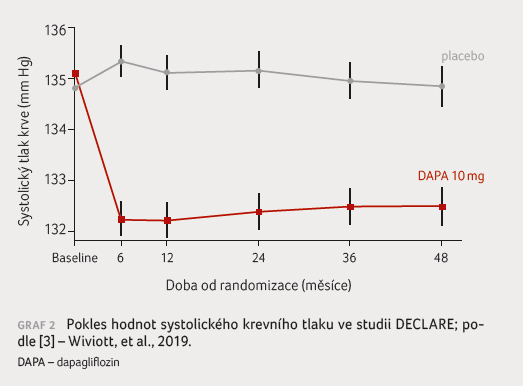 (velké kardiovaskulární
příhody, kardiovaskulární úmrtí, infarkt myokardu a ischemická
cévní mozková příhoda), 8,8 % vs. 9,4 % (p < 0,001
pro non inferioritu). Podávání dapagliflozinu vedlo k nižšímu
výskytu kardiovaskulárních úmrtí a hospitalizace pro
srdeční selhání (4,9 % vs. 5,8 %, p = 0,005),
čímž byla potvrzena jeho jasná superiorita (graf 3). Sledovaný cíl byl splněn především díky menšímu
počtu hospitalizací pro srdeční selhání a tento výsledek
byl podobný u nemocných s prokázaným kardiovaskulárním
úmrtím (7,8 % vs. 9,3 %) a s s vícečetnými
rizikovými faktory (2,8 % vs. 3,4 %), kdy samozřejmě
u nemocných s vícečetnými rizikovými faktory se tento
ukazatel vyskytoval téměř 3× méně než u nemocných
s prokázaným kardiovaskulárním onemocněním. U nemocných
s prokázaným kardiovaskulárním onemocněním byl výskyt
MACE doložen ve 13,9 % vs. 15,3 %, zatímco u nemocných
pouze s rizikovými faktory se nelišil, činil 5,3 % vs.
5,2 %.
(velké kardiovaskulární
příhody, kardiovaskulární úmrtí, infarkt myokardu a ischemická
cévní mozková příhoda), 8,8 % vs. 9,4 % (p < 0,001
pro non inferioritu). Podávání dapagliflozinu vedlo k nižšímu
výskytu kardiovaskulárních úmrtí a hospitalizace pro
srdeční selhání (4,9 % vs. 5,8 %, p = 0,005),
čímž byla potvrzena jeho jasná superiorita (graf 3). Sledovaný cíl byl splněn především díky menšímu
počtu hospitalizací pro srdeční selhání a tento výsledek
byl podobný u nemocných s prokázaným kardiovaskulárním
úmrtím (7,8 % vs. 9,3 %) a s s vícečetnými
rizikovými faktory (2,8 % vs. 3,4 %), kdy samozřejmě
u nemocných s vícečetnými rizikovými faktory se tento
ukazatel vyskytoval téměř 3× méně než u nemocných
s prokázaným kardiovaskulárním onemocněním. U nemocných
s prokázaným kardiovaskulárním onemocněním byl výskyt
MACE doložen ve 13,9 % vs. 15,3 %, zatímco u nemocných
pouze s rizikovými faktory se nelišil, činil 5,3 % vs.
5,2 %.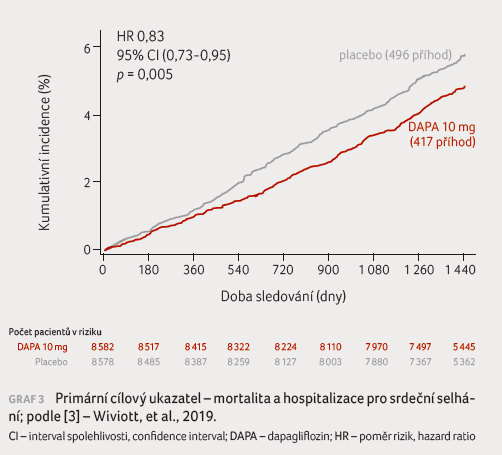
Výskyt renálního složeného cílového ukazatele činil 4,3 % při léčbě dapagliflozinem a 5,6 % při podávání placeba (p < 0,01), počet úmrtí byl statisticky nevýznamně nižší ve větvi s dapagliflozinem, 6,2 % vs. 6,6 %.
Během celé studie došlo k 3 724 (43,4 %) nežádoucím účinkům u nemocných léčených dapagliflozinem a k 3 871 (45,2 %) nežádoucím účinkům u nemocných ze skupiny placeba, z čehož jako závažné nežádoucí účinky bylo hlášeno 2 925 (34,1 %) událostí při léčbě dapagliflozinem a 3 100 (36,2 %) při podávání placeba. Hypoglykemií bylo méně při aktivní léčbě (58, 0,7 %) než v placebové skupině (83, 1,0 %), p = 0,02, naopak tomu bylo u ketoacidóz – při aktivní léčbě jich bylo zaznamenáno 27 (0,3 %), zatímco při podávání placeba 12 (0,1 %), p = 0,02. Tento výskyt byl ale celkově tak nízký, že z něj nelze vyvozovat větší závěry. Zhoršení renálních funkcí bylo častější v placebové skupině, urogenitální infekce se objevovaly častěji při léčbě dapagliflozinem. Fournierova gangréna (polymikrobiální infekce mužského genitálu) byla doložena v jednom případě ve skupině dapagliflozinu a v pěti případech ve skupině placeba. Výskyt karcinomu močového měchýře byl zaznamenán v 0,3 % při podávání dapagliflozinu a v 0,5 % v placebové větvi (p = 0,02).
Diskuse
Dapagliflozin je vysoce selektivní inhibitor společného transportéru pro sodík a glukózu (sodium glucose co transporter 2, SGLT2), který snižuje hyperglykemii potenciací glykosurie. Účinkuje tedy nezávisle na funkci beta buněk a doplňuje mechanismy účinku antidiabetik závislé na inzulinu s minimálním rizikem vzniku hypoglykemie. Dapagliflozin je nové perspektivní antidiabetikum s komplexním působením a malým rizikem nežádoucích účinků, jež nepochybně významně zvýší kvalitu antidiabetické léčby.
Základní hypotézou studie DECLARE je, že zlepšení metabolických parametrů – snížení glykemie i krevního tlaku a tělesné hmotnosti – povede ke snížení výskytu kardiovaskulárních cílových ukazatelů, a to jak u populace s již známým kardiovaskulárním onemocněním (CVD), tak u populace s „pouze“ rizikovými faktory (MRF). Proto bylo do studie DECLARE zařazeno 59,4 % pacientů bez prokázaného kardiovaskulárního onemocnění, což ji odlišuje od předchozích klinických sledování. Studie EMPA REG zařadila pouze nemocné s prokázaným kardiovaskulárním onemocněním a program CANVAS zahrnul 3 486 (34,4 %) sledovaných s pouze vícečetnými rizikovými faktory, ale bez prokázaného kardiovaskulárního onemocnění [4–7].
Na základě dosavadních klinických studií doporučují současné gudelines pro léčbu diabetes mellitus inhibitor SGLT2 u nemocných s diabetes mellitus a s prokázaným kardiovaskulárním onemocněním [8,9]. Tato nová data posouvají inhibitory SGLT2 i do oblasti léčby nemocných bez kardiovaskulárního onemocnění, ale s vícečetnými rizikovými faktory. Tomuto se věnují dva komentáře publikované v časopise Lancet současně se studií DECLARE, které upozorňují, že u nemocných s prokázaným kardiovaskulárním onemocněním je doloženo snížení výskytu kardiovaskulárních příhod, zatímco u nemocných s vícečetnými rizikovými faktory je prokázána nefroprotekce a snížení počtu hospitalizací pro srdeční selhání [3,10].
Autoři ve svých závěrech pak nastiňují i budoucnost klinického výzkumu v této oblasti. Inhibitory SGLT2 doložily svůj přínos u nemocných trpících srdečním selháním a diabetes mellitus a do budoucna je třeba zjistit, zda budou účinné i u nemocných se srdečním selháním bez diabetes mellitus
Seznam použité literatury
- [1] Raz I, Mosenzon O, Bonaca MP, et al. DECLARE‑TIMI 58: Participants Baseline Charcteristics. Diabetes Obes Metab 2018; 20: 1102–1110.
- [2] Špinar J. Dapagliflozin a studie DECLARE – vstupní charakteristika. Kardiol Rev Int Med 2018; 20: 61–65.
- [3] Wiviott SD, Raz M, Bonaca O, et al. Dapagliflozin and cardiovascular outcomes in type 2 diabetes. N Engl J Med 2019; 380: 347–357.
- [4] Ferrannini E, Mark M, Mayoux E. CV Protection in the EMPA‑REG outcome trial: A “Thrifty Substrate” hypothesis. Diabetes Care 2016; 39: 1108–1114.
- [5] Kvapil M. EMPA‑REG OUTCOME. Důkaz, že populace pacientů s diabetem se mění. Remedia 2016; 26: 67–72.
- [6] Mudaliar S, Alloju S, Henry RR. Can a shift in fuel energetics explain the beneficial cardiorenal outcomes in the EMPA‑REG OUTCOME study? A unifying hypothesis. Diabetes Care 2016; 39: 1115–1122.
- [7] Perkovic V, Zeeuw D, Mahaffey KW, et al. Canagliflozin and renal outcomes in type 2 diabetes: results from the CANVAS Program randomised clinical trials. Lancet Diabetes Endocrinol 2018; 6: 691–704.
- [8] American diabetes association. 8. Pharmacologic approaches to glycemic treatment: standards of medical are in diabetes ‑ 2018. Diabetes Care 2018; 41: 73–85.
- [9] American diabetes association. 8. Pharmacologic approaches to glycemic treatment: standars of medical are in diabetes ‑ 2018. Diabetes Care 2018; 41: 86–104.
- [10] Zelniker TA, Wiviott SD, Raz I, et al. SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta‑analysis of cardiovascular outocome trials. Lancet 2019; 393: 31–39.