Studie EMPEROR‑Preserved
Souhrn:
Špinar J, Špinarová L, Vítovec J. Studie EMPEROR‑Preserved. Remedia 2022; 32: 139–143.
Inhibitory sodíko‑glukózového kotransportéru 2 (sodium‑glucose cotransporter 2, SGLT2) snižují riziko hospitalizací pro srdeční selhání u nemocných se srdečním selháním se sníženou ejekční frakcí (heart failure with reduced ejection fraction, HFrEF), avšak jejich účinek u pacientů se srdečním selháním se zachovanou ejekční frakcí (heart failure with preserved ejection fraction, HFpEF) není znám. Do dvojitě zaslepené studie EMPEROR‑Preserved bylo zařazeno 5 988 pacientů se srdečním selháním třídy II–IV dle NYHA (New York Heart Association) a s ejekční frakcí levé komory (EF LK) > 40 %, kteří byli randomizováni k podávání empagliflozinu v dávce 10 mg denně nebo k podávání placeba. Primárním složeným cílovým ukazatelem byly kardiovaskulární úmrtí a hospitalizace pro zhoršení srdečního selhání. V průměrné době sledování 26,2 měsíce se primární cílový ukazatel vyskytl u 415 z 2 997 (13,8 %) nemocných léčených empagliflozinem a u 511 z 2 991 (17,1 %) nemocných v placebové skupině (p < 0,001). Tento výsledek byl především z důvodu hospitalizace pro srdeční selhání. Pozitivní efekt empagliflozinu byl zjištěn bez ohledu na hodnoty EF LK < 50 %, 50–60 %, > 60 % a bez ohledu na přítomnost diabetes mellitus. Počet hospitalizací byl nižší u nemocných léčených empagliflozinem (p < 0,001). Nekomplikovaný urogenitální zánět a hypotenze byly častěji hlášeny v empagliflozinové skupině. V roce 2022 byla publikována subanalýza potvrzující, že empagliflozin zlepšuje rovněž kvalitu života. Léčba empagliflozinem redukuje počet kardiovaskulárních úmrtí a hospitalizací pro srdeční selhání a zvyšuje kvalitu života pacientů s HFpEF bez ohledu na přítomnost diabetes mellitus.
Summary:
Spinar J, Spinarova L, Vitovec J. EMPEROR‑Preserved trial. Remedia 2022; 32: 139–143.
Sodium‑glucose cotransporter‑2 (SGLT2) inhibitors reduce the risk of hospitalisations for heart failure with reduced ejection fraction (HFrEF). Still, their effects in patients with heart failure with preserved ejection fraction (HFpEF) are uncertain. In a double‑blind EMPEROR‑Preserved trial, we randomly assigned 5988 patients with class II‑IV heart failure and an ejection fraction >40% to receive empagliflozin (10 mg once daily) or placebo in addition to recommended therapy. The primary outcome was a composite of cardiovascular death and hospitalisation for worsening heart failure. Over a median of 26.2 months, the primary outcome occurred in 415 of 2997 patients (13.8%) in the empagliflozin group and in 511 of 2991 patients (17.1%) in the placebo group (p<0.001). This effect was mainly related to a 29% decrease in the risk of hospitalisation for heart failure. The effect of empagliflozin on the primary outcome was consistent in patients with ejection fraction <50%, 50% to 60% and >60%, regardless of the presence or absence of diabetes. The total number of hospitalisations for heart failure was lower in the empagliflozin group than in the placebo group (p<0.001). Uncomplicated genital and urinary infections and hypotension were reported more frequently with empagliflozin. A subanalysis confirming that empagliflozin improved the quality of life was published in 2022. Empagliflozin reduced the combined risk of cardiovascular death, hospitalisation for heart failure and improved the quality of life in patients with HFpEF regardless of the presence or absence of diabetes.
Key words: heart failure – empagliflozin – hospitalisations – quality of life.
Úvod
Pacienti se srdečním selháním mohou mít sníženou nebo zachovanou ejekční frakci levé komory (EF LK). Pacienti se sníženou EF LK (heart failure with reduced ejection fraction, HFrEF) mívají v anamnéze srdeční infarkt či jiné poškození srdečního svalu. Pacienti se zachovanou EF LK (heart failure with preserved ejection fraction, HFpEF) naopak mají mikrovaskulární dysfunkci, fibrózu či zánět srdečního svalu, často jsou obézní, mají hypertenzi, diabetes mellitus a další komorbidity [1,2].
U nemocných s diabetes mellitus a kardiovaskulárním rizikem inhibitory sodíko glukózového kotransportéru 2 (sodium glucose cotransporter 2, SGLT2) redukují riziko hospitalizací pro srdeční selhání a závažné nežádoucí renální příhody, což je efekt, který není pozorován u jiných perorálních antidiabetik. Ve velkých klinických studiích snižovalo podání inhibitorů SGLT2 riziko hospitalizací pro srdeční selhání o 30–35 %, a to především u nemocných s EF LK < 30 % [3–5]. Kromě toho empagliflozin redukuje riziko vzniku nežádoucích renálních příhod, včetně počtu renálních transplantací [3,6]. Tento účinek není vysvětlitelný poklesem glykemie, protože jiná antidiabetika snižují hodnotu glykemie dokonce více [7].
Studie EMPEROR Preserved (Empagliflozin and cardiovascular outcomes in heart failure with a preserved ejection fraction) byla určena pro nemocné s HFpEF a byla prezentována na kongresu Evropské kardiologické společnosti (ESC) 2021 a současně publikována v New England Journal of Medicine [8]. Toto klinické hodnocení volně navazuje na studii EMPEROR Reduced, jejíž výsledky byly prezentovány a publikovány o rok dříve [9,10].
Do studie bylo zařazeno 5 988 pacientů, muži i ženy starší 18 let, se srdečním selháním funkční třídy II–IV dle NYHA (New York Heart Association) a s EF LK > 40 %, kteří byli léčeni standardní medikací pro srdeční selhání a komorbidity. Hodnota natriuretického propeptidu typu B (NT proBNP) musela být > 300 pg/ml a u pacientů s fibrilací síní > 900 pg/ml. Screening trval 4–28 dní a nemocní byli randomizováni k podávání empagliflozinu v dávce 10 mg/den nebo k podávání placeba. Při randomizaci rozhodovala geografická poloha, přítomnost diabetes mellitus, EF LK < 50 % či hodnota glomerulární filtrace. Ostatní léčba srdečního selhání byla plně na ošetřujícím lékaři. Pacienti byli opakovaně sledováni podle klinického stavu, Kansaského dotazníku (Kansas City Cardiomyopathy Questionnaire, KCCQ) a nežádoucích účinků.
Primární a sekundární cílové
ukazatele
Primárním složeným cílovým
ukazatelem studie byly doba do kardiovaskulárního úmrtí nebo
hospitalizace pro srdeční selhání. Sekundární cílové
ukazatele zahrnovaly změnu v hodnotě glomerulární
filtrace a EF LK. Uspořádání studie ukazuje obrázek 1.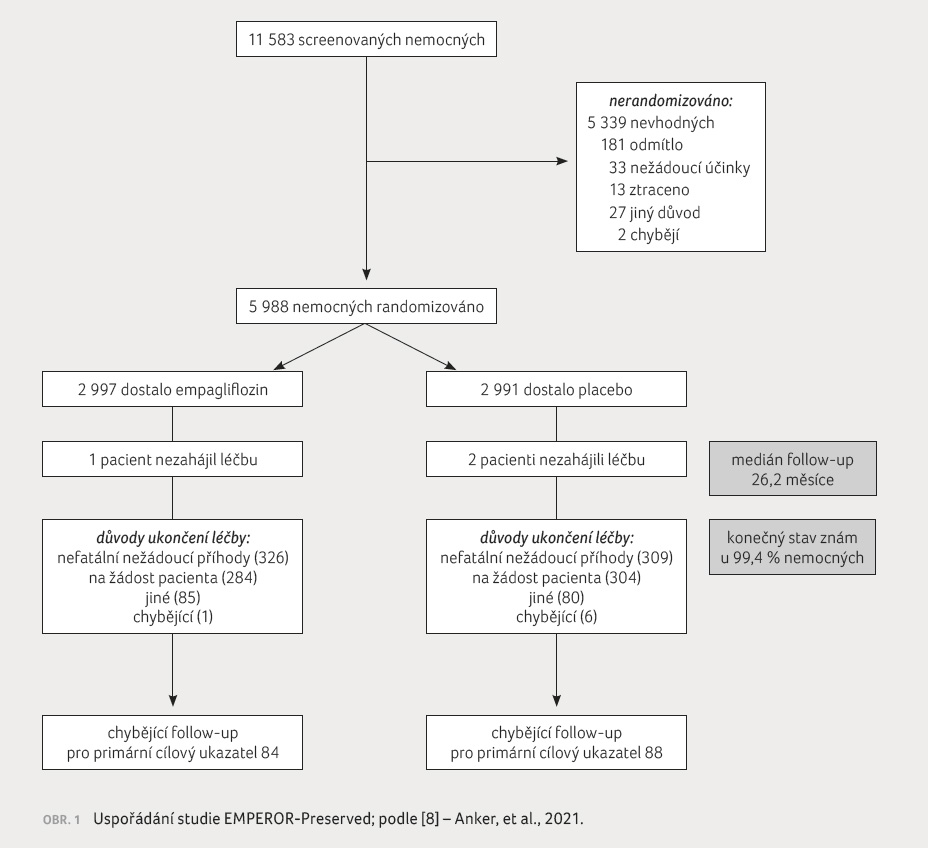
Výsledky
Od 27. března 2017
do 12. dubna 2020 bylo screenováno 11 583 nemocných
a 5 988 pacientů bylo randomizováno k podávání
empagliflozinu (2 997 osob) nebo placeba (2 991 osob)
v 621 centrech ve 23 zemích. Průměrný věk
nemocných činil 71,8 roku, resp. 71,9 roku, většina pacientů
byla ve třídě NYHA II, hodnota NT proBNP činila
994 pg/ml, resp. 946 pg/ml. Fibrilací síní trpělo zhruba 50 %
nemocných, hypertenzí 91 % osob a onemocněním
diabetes mellitus 49 % osob. Nemocní byli dobře
léčeni – blokátory systému renin angiotenzin
(RAS) užívalo 81 % osob a betablokátory 86 % osob.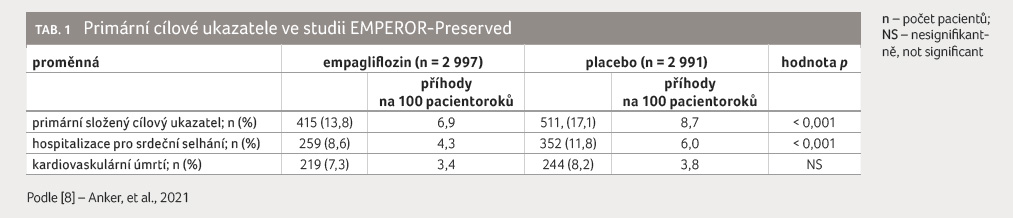
Studijní medikace byla ukončena
z jiného důvodu než úmrtí u 696 (23 %) nemocných
léčených empagliflozinem a u 699 (23,4 %) nemocných
v placebové skupině. U 17 (0,6 %) nemocných
léčených empagliflozinem a u 19 (0,6 %) nemocných
s placebem nebyl na konci studie znám jejich stav.
Průměrná doba trvání studie byla 26,2 měsíce.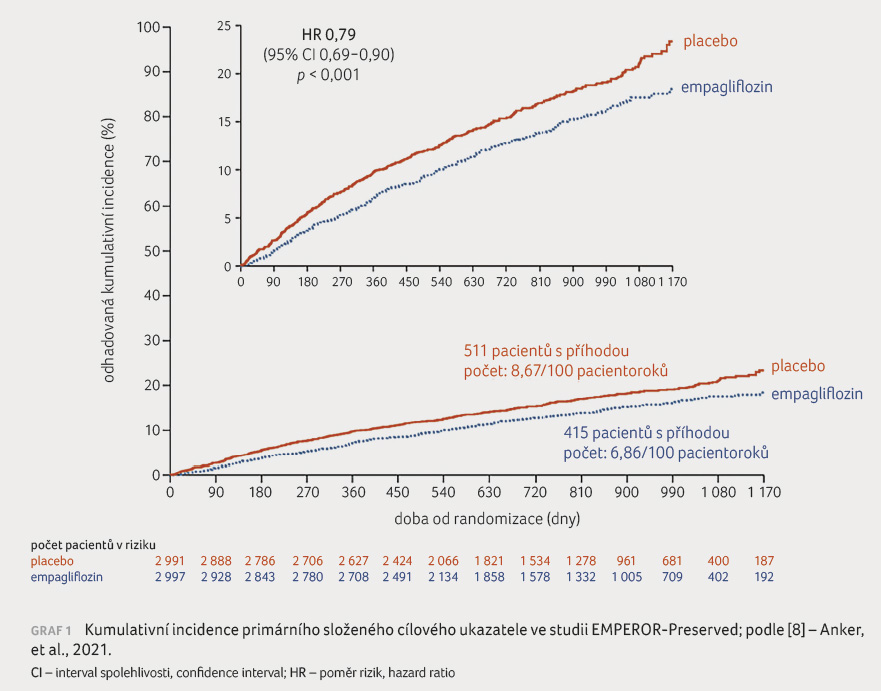
Primární cílový ukazatel kardiovaskulárního úmrtí nebo hospitalizace pro srdeční selhání se vyskytl u 415 (13,8 %) nemocných léčených empagliflozinem a u 511 (17,1 %) nemocných s placebem (p < 0,001), tabulka 1, graf 1. Celková mortalita se v obou skupinách nelišila (graf 2, tab. 2). Úmrtí z kardiovaskulárních příčin se vyskytlo u 219 (7,3 %) nemocných léčených empagliflozinem a u 244 (8,2 %) nemocných v placebové skupině (nesignifikantně). Hospitalizace pro srdeční selhání byla zaznamenána u 259 (8,6 %) nemocných v empagliflozinové skupině a u 352 (11,8 %) nemocných s placebem (p < 0,001), tabulka 1. Primární cílový ukazatel byl stejný u předdefinovaných podskupin pacientů, např. u nemocných s diabetes mellitus a bez diabetes mellitus či u nemocných s EF LK < 50 %, 50–60 % nebo > 60 %. Nelišily se ani změny v hmotnosti pacientů, hodnotě krevního tlaku, koncentraci kyseliny močové, NT proBNP či v hodnotě glykovaného hemoglobinu.
Tři nemocní (1 v empagliflozinové
skupině a 2 s placebem) nedostali léčbu a byli
vyřazeni z hodnocení. Závažné nežádoucí účinky byly
zaznamenány u 1 436 (47,9 %) nemocných léčených
empagliflozinem a u 1 453 (51,6 %) nemocných
s placebem. Nežádoucí účinky vedoucí k ukončení
léčby se vyskytly u 571 (19,1 %) nemocných
v empagliflozinové skupině a u 551 (18,4 %)
nemocných s placebem.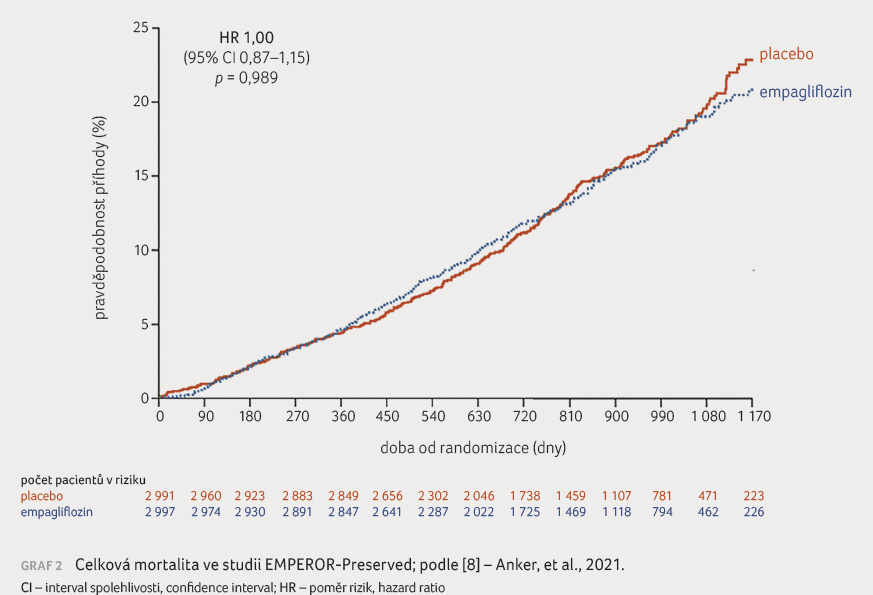
V lednu 2022 byla publikována v časopise Circulation subanalýza Kansaského dotazníku ve studii EMPEROR Preserved, která ukazuje, že empagliflozin nejen snižuje počet hospitalizací, ale rovněž zlepšuje kvalitu života pacientů [11].
Diskuse
U nemocných s HFpEF vedlo podávání inhibitoru SGLT2 empagliflozinu k 21% redukci výskytu složeného cílového ukazatele kardiovaskulárního úmrtí a hospitalizace pro srdeční selhání, na níž se podílelo především 29% snížení počtu hospitalizací pro srdeční selhání. Prospěch byl pozorován u všech nemocných bez ohledu na hodnotu EF LK či přítomnost diabetes mellitus. Léčba empagliflozinem významně snížila počet prvních hospitalizací pro srdeční selhání. Dané výsledky jsou velmi podobné studii s empagliflozinem u nemocných s HFrEF (EMPEROR Reduced) publikované v loňské roce [9,10].
Studie EMPEROR Preserved potvrzuje
předchozí výsledky, že inhibice SGLT2 snižuje počet úmrtí
a hospitalizací pro srdeční selhání u nemocných se
srdečním selháním a diabetes mellitus [12]. V těchto
studiích však pacienti neměli srdeční selhání při zařazení
do sledování. Již dřívější data ukazovala, že by
z léčby mohli mít prospěch také nemocní s HFpEF, tato
data ale byla zaznamenána spíše na menších souborech
[4,13]. Studie EMPEROR Preserved poprvé ukázala, že efekt
inhibitoru SGLT2 u pacientů s HFpEF je i u nemocných
bez diabetes mellitus.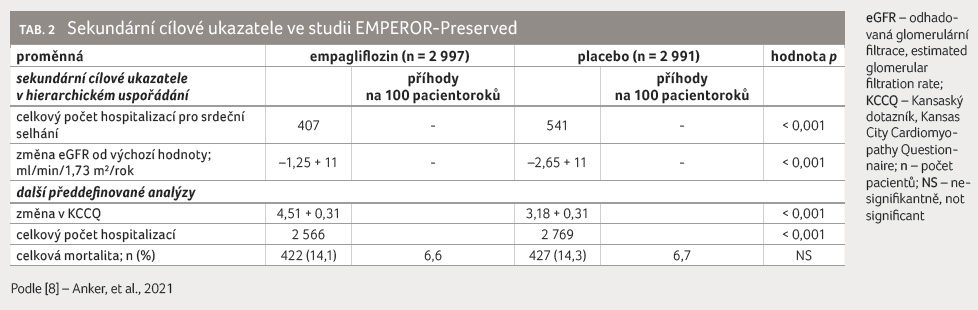
V předchozích studiích neměli nemocní s HFpEF jednoznačný prospěch z léčby. Klinická hodnocení s kandesartanem, spironolaktonem či kombinací sakubitril/valsartan měla pouze hraniční statistickou významnost [14–17]. Podskupinová analýza ukazovala, že prospěch mohou mít pacienti s EF LK 40–50 %, avšak ne s EF LK > 50 %, nebo dokonce > 60 % [16–18]. Ve studii EMPEROR Preserved na rozdíl od studií s kandesartanem, spironolaktonem či kombinací sakubitril/valsartan byl efekt empagliflozinu doložen rovněž u nemocných s EF LK > 50 %, či dokonce > 60 %.
Zdá se, že pozitivní efekt empagliflozinu může být plně vysvětlen. Srdeční selhání se zachovanou EF LK je úzce spjato s koronárním endoteliálním zánětem, což vede ke koronární mikrovaskulární dysfunkci a srdeční fibróze, které mohou limitovat roztažnost levé komory [1,19]. Na animálních modelech inhibitory SGLT2 u nemocných s HFpEF zmírňovaly srdeční zánět, koronární mikrovaskulární dysfunkci, fibrózu a zlepšovaly diastolické plnění, tedy parametry nezávislé na redukci glykemie.
Přestože empagliflozin snížil počet hospitalizací pro srdeční selhání, neredukoval celkovou mortalitu. Podobný nález byl pozorován i ve studiích s kombinací sakubitril/valsartan u podobného typu pacientů a s podobnou dobou sledování [15]. Jestliže tento výsledek demonstruje zpomalení progrese onemocnění, pak účinek na mortalitu by potřeboval delší dobu sledování.
Závěrem je možné říci, že empagliflozin snižuje kardiovaskulární mortalitu, počet hospitalizací pro srdeční selhání a zvyšuje kvalitu života u nemocných s HFpEF. Tento efekt je nezávislý na hodnotě EF LK a na přítomnosti diabetes mellitus.
Seznam použité literatury
- [1] Mohammed SF, Hussain S, Edwards SA, et al. Coronary microvascular rarefaction and myocardial fibrosis in heart failure with preserved ejection fraction. Circulation 2015; 131: 550–559.
- [2] Packer M, Lan GSP, Lund LH, et al. Characterisation of the inflammatory‑metabolic phenotype of heart failure with preserved ejection fraction: a hypothesis to explain influence of sex on the evolution and potential treatment of the disease. Eur J Heart Fail 2020; 22: 1081–1090.
- [3] Lo KB, Gul F, Ram P, et al. The effects of SGLT2 inhibitors on cardiovascular and renal outcomes in diabetic patients: a systematic review and meta‑analysis. Cardiorenal Med 2020; 10: 1–10.
- [4] Kato ET, Silverman MG, Mosenzon O, et al. Effect of dapagliflozin on heart failure and mortality in type 2 diabetes mellitus. Circulation 2019; 139: 2528–2536.
- [5] Zannad F, Ferreira JP, Pocock SJ, et al. SGLT2 inhibitors in patients with reduced ejection fraction: a meta‑analysis of the EMPEROR‑Reduced and DAPA‑HF trials. Lancet 2020; 396: 819–829.
- [6] Neuen BL, Young T, Heerspink HJL, et al. SGLT2 inhibitors for the prevention of kidney failure in patients with type 2 diabetes: a systematic review and meta‑analysis. Lancet Diabetes Endocrinol 2019; 7: 845–854.
- [7] Packer M, Lam GSP, Lund LH, et al. SGLT2 inhibitors produce cardiorenal benefits by promoting adaptive cellular reprogramming to induce a state of fasting mimicry: a paradigm shift in understanding their mechanism of action. Diabetes Care 2020; 43: 508–511.
- [8] Anker SD, Butler J, Filipatos JP, et al. Empagliflozin and cardiovascular outcomes in heart failure with a preserved ejection fraction. N Engl J Med 2021; 385: 1451–1461.
- [9] Špinar J, Špinarová L, Vítovec J. EMPEROR‑Reduced – empagliflozin u nemocných se srdečním selháním a nízkou ejekční frakcí. Hypertenze a kardiovaskulární prevence 2020; 2: 62–66.
- [10] Packer M, Anker SD, Butler J, et al. Cardiovascular and renal outcomes with empagliflozin in heart failure. N Engl J Med 2020; 383: 1413–1424.
- [11] Butler J, Filippatos G, Siddqi TJ, et al. Empagliflozin, health status, and quality of life in patients with heart failure and preserved ejection fraction: The EMPEROR‑Preserved trial. Circulation 2022; 145: 184–193.
- [12] Zelniker TA, Wiviot SD, Raz I, et al. SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta‑analysis of cardiovascular outcomes trial. Lancet 2019; 393: 3139.
- [13] Figtree GA, Radholm K, Barrett TD, et al. Effects of canagliflozin on heart failure outcomes associated with preserved and reduced ejection fraction in type 2 diabetes mellitus. Circulation 2019; 139: 2591–2593.
- [14] Vaduganthan M, Clagett BL, Jhund PS, et al. Estimation lifetime benefit of comprehensive disease‑modifying pharmacologic therapies in patients with heart failure with reduced ejection fraction: a comparative analysis of three randomized controlled trials. Lancet 2020; 396: 121–128.
- [15] Solomon SD, McMurray JJV, Abad IS, et al. Angiotensin‑neprylisin inhibition in heart failure with preserved ejection fraction. N Engl J Med 2019; 381: 1609–1620.
- [16] Pitt B, Pfeffer M, Assmann SF. Spironolacton for heart failure with preserved ejection fraction. N Engl J Med 2014; 370: 1383–1392.
- [17] Lund LH, Clagget B, Liu J, et al. Heart failure with mid‑range ejection fraction in CHARM: characteristics, outcomes and effect of candesartan across the entire ejection fraction spectrum. Eur J Heart Fail 2018; 20: 1230–1239.
- [18] Butler J, Anker SD, Packer M. Redefining heart failure with reduced ejection fraction. JAMA 2019; 322: 1761–1762.
- [19] Hage C, Lofgren L, Michpoulos F, et al. Metabolomic profile in HFpEF vs HFrEF patients. J Card Fail 2020; 26: 1050–1059.