Studie EXCEED – sekukinumab versus adalimumab v léčbě aktivní psoriatické artritidy
Souhrn:
Suchý D. Studie EXCEED– sekukinumab versus adalimumab v léčbě aktivní psoriatické artritidy. Remedia 2020; 30: 571–574.
Psoriatická artritida (PsA) je heterogenní onemocnění zahrnující muskuloskeletální i kožní složku. Sekukinumab je plně humánní monoklonální protilátka, která selektivně neutralizuje působení interleukinu (IL) 17A a je schválena k léčbě PsA, psoriázy a ankylozující spondylitidy. V současné době je k dispozici rozsáhlá evidence o účinnosti sekukinumabu v terapii PsA. Studie EXCEED měla za cíl prokázat, že monoterapie sekukinumabem je superiorní oproti léčbě adalimumabem namířené proti tumor nekrotizujícímu faktoru alfa u biologicky naivních pacientů s PsA a plakovou psoriázou. Studie nesplnila svůj primární cíl, tedy průkaz superiority sekukinumabu nad adalimumabem, pokud jde o účinnost léku hodnocenou podle odpovědi na léčbu. Ve skupině léčené sekukinumabem byl ve srovnání s léčbou adalimumabem doložen vyšší podíl pacientů setrvávajících u léčby.
Summary:
Suchy D. EXCEED trial – secukinumab versus adalimumab in the treatment of active psoriatic arthritis. Remedia 2020; 30: 571–574.
Psoriatic arthritis (PsA) is a heterogeneous disease comprising of musculoskeletal and dermatological manifestations. Secukinumab, a fully human monoclonal antibody that selectively neutralizes IL‑17A, is approved in many countries for the treatment of PsA, psoriasis and ankylosing spondylitis. There is now an extensive body of evidence demonstrating the efficacy of secukinumab in PsA. The objective of the EXCEED study was to investigate whether secukinumab (SEC) is superior to adalimumab (ADA), a TNF inhibitor, as monotherapy in biologic‑naive active PsA patients with active plaque psoriasis. Secukinumab did not meet statistical significance for superiority versus adalimumab in the primary endpoint of ACR20 (American College of Rheumatology) response at week 52. However, secukinumab was associated with a higher treatment retention rate than adalimumab.
Key words: psoriatic arthritis – secukinumab – adalimumab
Psoriatická artritida (PsA) je druhou
nejčastější zánětlivou atropatií asociovanou s psoriázou
(PSO). Jedná se o heterogenní zánětlivé revmatické
onemocnění, které zahrnuje kromě postižení kůže a periferních
kloubů i zánětlivé postižení entezí, daktylitidy
a v některých případech postižení axiálního
skeletu.
Psoriatická artritida postihuje dle odhadů 0,3–1 % populace a vzniká u zhruba 30 % nemocných s PSO. Neléčená PsA způsobuje vážnou invaliditu a je spojena s komorbiditami.. Pacienti s PsA jsou ohroženi větším rizikem předčasného úmrtí ve srovnání s obecnou populací. U přibližně 50 % nemocných s PsA dochází během dvou let k vývoji nevratných kloubních erozí; kloubní poškození se projevuje poklesem funkčních schopností pacientů. Mezi negativní prognostické faktory onemocnění patří polyartritida, již přítomné strukturální poškození zjistitelné pomocí RTG vyšetření, zvýšené hodnoty reaktantů akutní fáze, daktylitida a postižení nehtů [1].
Dle aktualizovaných doporučení EULAR (Evropská liga proti revmatismu) z roku 2019 [2] by v léčbě pacientů s PsA měla být zvolena nejlepší možná péče, přičemž musí vycházet ze společného rozhodnutí pacienta a revmatologa a brát v úvahu účinnost a bezpečnost léčby a léčebné náklady. Primárním cílem léčby pacientů s PsA je:
- dosáhnout prostřednictvím kontroly příznaků co nejlepší kvality života s ohledem na zdravotní stav,
- předcházet strukturálnímu poškození,
- dosáhnout normálního fungování a sociální participace;
- důležitou komponentou k dosažení těchto cílů je odstranění zánětu [2].
Při léčbě pacientů s PsA je třeba zohlednit každou muskuloskeletální manifestaci a přizpůsobit jí léčebná rozhodnutí. Dále je třeba vzít v úvahu jiné než muskuloskeletální manifestace (kůže, oči a gastrointestinální trakt); je třeba také přihlédnout ke komorbiditám, jako je metabolický syndrom, kardiovaskulární onemocnění nebo deprese. Cílem léčby by mělo být dosažení remise nebo alternativně nízké aktivity onemocnění s pravidelným hodnocením aktivity onemocnění a vhodnou úpravou terapie [2].
Jednoznačné doklady o účinnosti u PsA mají v kategorii konvenčních syntetických léků (conventional synthetic disease modifying antirheumatic drugs, csDMARDs) pouze sulfasalazin a leflunomid, pro nejčastěji používaný metotrexát jsou důkazy o účinnosti rozporuplné. Z biologických léků mají jednoznačně prokázanou účinnost inhibitory tumor nekrotizujícího faktoru (TNF), ustekinumab a inhibitory interleukinu (IL) 17 (sekukinumab, ixekizumab). Dle doporučení České revmatologické společnosti z roku 2016 je biologická léčba PsA indikována po selhání léčby csDMARDs. V tomto dokumentu jsou inhibitory TNF doporučovány v první linii léčby [1], při nevhodnosti či kontraindikacích inhibitorů TNF je možná léčba inhibitorem IL-17/23 (ustekinumab) nebo inhibitorem IL-17 (sekukinumab). Doporučení EULAR pro léčbu PsA, resp. jejich nová verze z roku 2019 přichází se stanoviskem zahájit u pacientů s periferní artritidou a nedostatečnou odpovědí na nejméně jeden csDMARD terapii biologickými chorobu modifikujícími antirevmatickými léky (biologic disease modifying antirheumatic drugs, bDMARDs); v případě relevantního postižení kůže je možné preferovat inhibitor IL-17 nebo IL-12/23. U pacientů s převážně axiálním onemocněním, které je aktivní a nereaguje dostatečně na podávání nesteroidních antiflogistik (NSAID), by měla být zvážena terapie některým bDMARD, což je podle současné praxe inhibitor TNF; v přítomnosti významného postižení kůže je možné upřednostnit inhibitor IL-17 [2].
Doporučení již tedy zohledňuje vyšší účinnost anti IL-17 terapie u pacientů s rozsáhlejším kožním postižením.
Sekukinumab
Sekukinumab je plně humánní monoklonální protilátka IgG1κ, která se selektivně váže na prozánětlivý cytokin IL-17A a neutralizuje jeho aktivitu. Interleukin 17A hraje klíčovou roli v patogenezi ložiskové PSO i PsA. Bylo doloženo jeho zvýšené množství v psoriatických lézích a v synoviální tekutině pacientů s PsA. Sekukinumab je účinný u postižení kštice a nehtů, u palmoplantární, erytrodermické a pustulózní PSO a PsA. Program klinických hodnocení provedených se sekukinumabem u pacientů s PsA je velmi rozsáhlý, zahrnuje pět studií FUTURE [3] a studii MAXIMISE.
V klinické studii FUTURE 2 se dvěma třetinami biologicky naivních pacientů s PsA a třetinou non respondérů na anti TNF léčbu dosáhlo odpovědi ACR 20 (20% zlepšení dle hodnocení American College of Rheumatology) ve 24. týdnu (primární cílový ukazatel) 54 % pacientů (p < 0,0001) ve skupině sekukinumabu 300 mg (n = 100), 51 % (p < 0,0001) ve skupině sekukinumabu 150 mg (n = 100) a 15 % pacientů ve skupině placeba (n = 98). Dlouhodobá účinnost byla potvrzena i ve dvouleté a pětileté extenzi studie [4].
Ve studii FUTURE 5, jež obsáhla smíšenou populaci s více než dvěma třetinami biologicky naivních pacientů a s méně než třetinou non respondérů na anti TNF léčbu, byly odpovědi ACR 20 v týdnu 16 (primární cílový ukazatel) 63 % pro sekukinumab 300 mg (n = 222; p < 0,0001), 56 % pro sekukinumab 150 mg (n = 220; p < 0,0001) a 27 % pro placebo (n = 332). Došlo rovněž k významnému ovlivnění kožní a nehtové PSO, entezitid a daktylitid a k inhibici radiologických (strukturálních) změn [5].
Studie MAXIMISE byla prvním randomizovaným klinickým hodnocením, které se specificky zaměřilo na účinnost a bezpečnost biologického léku u nemocných s PsA s axiálními projevy. V rameni s 300 mg sekukinumabu bylo dosaženo v týdnu 12 odpovědi ASAS 20 (20% zlepšení dle hodnocení Assessment in SpondyloArthritis International Society; primární cílový ukazatel) u 62 % pacientů oproti 31 % pacientů ze skupiny placeba (p < 0,0001, n = 164). Studie tedy potvrdila efekt sekukinumabu i na axiální složku, nezávisle na současném podávání metotrexátu. Profil bezpečnosti sekukinumabu odpovídal předchozím zjištěním [6].
Studie EXCEED
Na podzim 2019 byly publikovány
výsledky studie EXCEED srovnávající sekukinumab (300 mg; poté
každé 4 týdny) proti přípravku Humira (adalimumab 40 mg každý
druhý týden) u pacientů s aktivní PsA. Jednalo se
o 52týdenní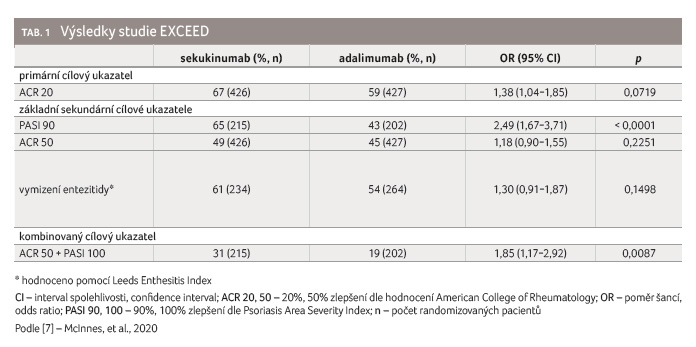 dvojitě zaslepenou klinickou studii typu
head to head fáze IIIb, která zahrnovala více než 800
biologicky dosud neléčených pacientů s PsA. Do studie
byli zařazeni pacienti s aktivní PsA (≥ 3 bolestivé
klouby ze 78 a ≥ 3 oteklé klouby ze 76)
a s předchozí nedostatečnou odpovědí na csDMARDs
včetně metotrexátu nebo ti, kteří léčbu ukončili z důvodu
bezpečnosti/nesnášenlivosti. Předchozí expozice jakékoliv
biologické léčbě PsA a PSO byla vylučovacím kritériem
[7]. Demografické údaje i aktivita PsA byly v obou
ramenech studie velmi podobné. V rameni se sekukinumabem bylo
zastoupeno více žen.
dvojitě zaslepenou klinickou studii typu
head to head fáze IIIb, která zahrnovala více než 800
biologicky dosud neléčených pacientů s PsA. Do studie
byli zařazeni pacienti s aktivní PsA (≥ 3 bolestivé
klouby ze 78 a ≥ 3 oteklé klouby ze 76)
a s předchozí nedostatečnou odpovědí na csDMARDs
včetně metotrexátu nebo ti, kteří léčbu ukončili z důvodu
bezpečnosti/nesnášenlivosti. Předchozí expozice jakékoliv
biologické léčbě PsA a PSO byla vylučovacím kritériem
[7]. Demografické údaje i aktivita PsA byly v obou
ramenech studie velmi podobné. V rameni se sekukinumabem bylo
zastoupeno více žen.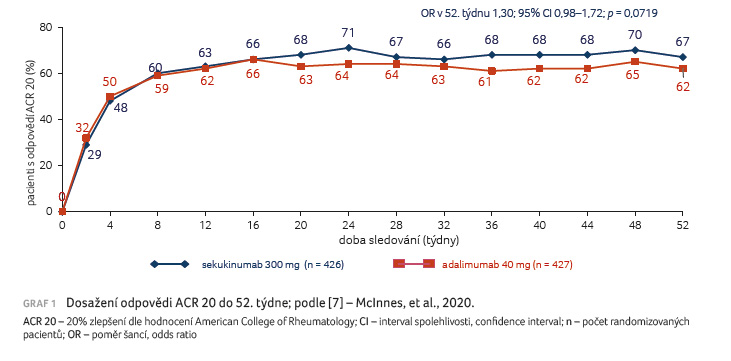
Primárním cílovým ukazatelem byl průkaz superiority sekukinumabu oproti adalimumabu v hodnocení účinnosti podle Americké koleje revmatologů ACR 20 v 52. týdnu. Sekundárními cílovými ukazateli byly PASI 90 (90% zlepšení dle Psoriasis Area Severity Index), četnost odpovědi ACR 50 (50% zlepšení dle ACR), změny skóre disability HAQ (Health Assessment Questionnaire) a redukce entezitid v týdnu 52.
Primárního cíle studie v týdnu
52 nebylo dosaženo. Podle kritérií ACR 20 odpovědělo 67 %
pacientů ve skupině léčené sekukinumabem vs. 62 % při
terapii adalimumabem (poměr šancí [odds ratio, OR] 1,30, 95%
interval spolehlivosti [confidence interval, CI] 0,98−1,72,
p = 0,0719). Při hodnocení sekundárních cílů
dosáhl signifikantně větší počet pacientů léčených
sekukinumabem PASI 90 a kombinované odpovědi ACR 50 a PASI
100 (tab. 1, graf 1, 2).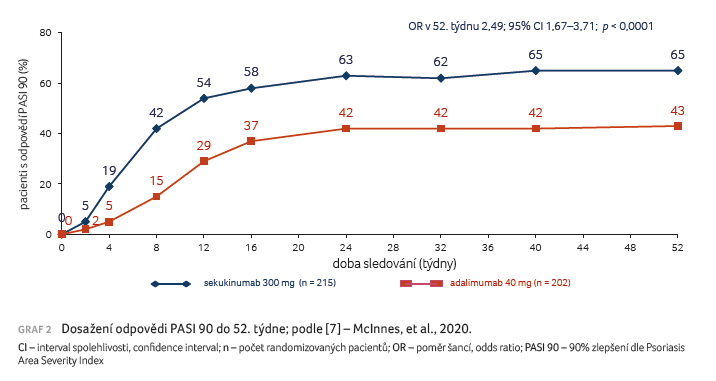
Analýza odpovědí na léčbu ACR
20 a PASI 90 byla provedena rovněž ve skupině se středně
těžkou a těžkou PSO (definovanou hodnotami skóre Body
Surface Area [BSA] nebo PASI ≥ 10). V tomto subsetu
pacientů byla zaznamenána odpověď ACR 20 u 76 % pacientů
při terapii sekukinumabem oproti 68 % v rameni
s adalimumabem. Odpovědi PASI 90 bylo dosaženo u 69 %
vs. 42 % pacientů [8]. Kombinované odpovědi ACR 50 a PASI
100 dosáhlo v týdnu 52 významně více pacientů léčených
sekukinumabem oproti adalimumabu (30,7 % vs. 19,2 %; p = 0,0087
(graf 3).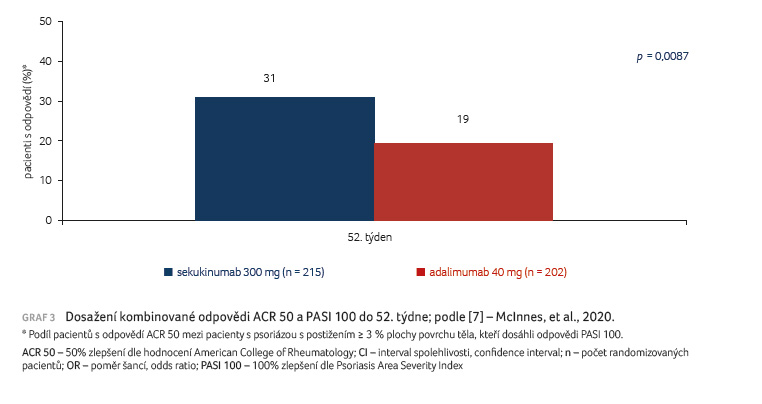
V rameni se sekukinumabem byl
zaznamenán nižší podíl pacientů, kteří léčbu přerušili.
Vyšší podíl pacientů léčených adalimumabem ukončil účast
ve studii z důvodů ztráty účinnosti, nežádoucích
účinků či reakcí v místě vpichu (graf 4).
Bezpečnostní profil obou hodnocených léčiv byl konzistentní
s předchozími údaji a byl velmi podobný v obou
ramenech studie. U dvou pacientů došlo při léčbě
sekukinumabem ke vzplanutí preexistujícího nespecifického
střevního zánětu (IBD). Závažné kardiovaskulární nežádoucí
účinky byly zaznamenány u dvou pacientů při léčbě
sekukinumabem (infarkt myokardu) a u jednoho pacienta při
léčbě adalimumabem (progrese srdečního selhání) [7].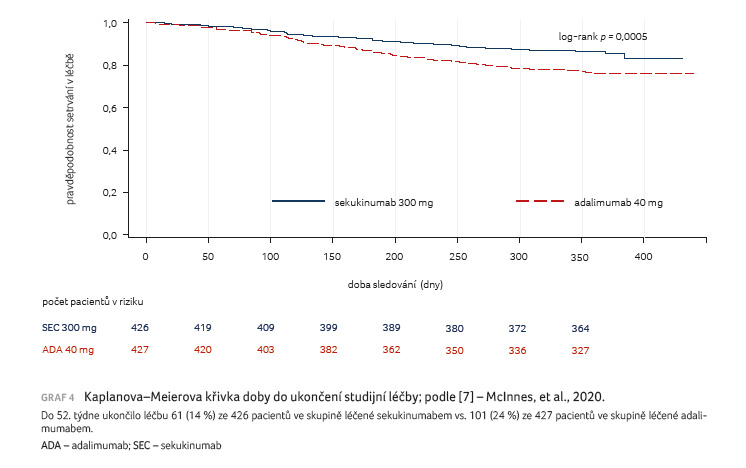
Závěr
Studie prokázala non inferioritu sekukinumabu oproti adalimumabu, ale nesplnila primární cíl, tedy prokázat superioritu sekukinumabu nad adalimumabem, pokud jde o účinnost léku podle kritéria ACR 20. Ve skupině pacientů se středně těžkou a těžkou PSO byla účinnost sekukinumabu vyšší. Více pacientů léčených adalimumabem ukončilo studii z důvodů ztráty účinnosti nebo nežádoucích účinků.
Seznam použité literatury
- [1] Štolfa J, Vencovský J, Pavelka K. Doporučené postupy České revmatologické společnosti pro léčbu psoriatické artritidy. Čes Revmatol 2012; 20: 13–18.
- [2] Gossec L, Baraliakos X, Kerschbaumer A, et al. EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2019 update. Ann Rheum Dis 2020; 79: 700–712.
- [3] Garcia‑Montoya L, Marzo‑Ortega H. The role of secukinumab in the treatment of psoriatic arthritis and ankylosing spondylitis. Ther Adv Musculoskelet Dis 2018; 10: 169−180.
- [4] McInnes IB, Mease PJ, Kirkham B, et al. Secukinumab, a human anti‑interleukin‑17A monoclonal antibody, in patients with psoriatic arthritis (FUTURE 2): a randomised, double‑blind, placebo‑controlled, phase 3 trial. Lancet 2015; 386: 1137–1146.
- [5] Mease P, van der Heijde D, Landewé R, et al. Secukinumab improves active psoriatic arthritis symptoms and inhibits radiographic progression: primary results from the randomised, double‑blind, phase III FUTURE 5 study. Ann Rheum Dis 2018; 77: 890–897.
- [6] Baraliakos X, Coates L, Gossec L, et al. Secukinumab Improves Axial Manifestations in Patients with Psoriatic Arthritis and Inadequate Response to NSAIDs: Primary Analysis of Phase 3 Trial. 2019 ACR/ARP Annual Meeting, Abstr. Nr. 288.
- [7] McInnes IB, Behrens F, Mease PJ, et al.; EXCEED Study Group. Secukinumab versus adalimumab for treatment of active psoriatic arthritis (EXCEED): a double‑blind, parallel‑group, randomised, active‑controlled, phase 3b trial. Lancet 2020; 395: 1496–1505.
- [8] Gottlieb AB, Behrens F, Nash P, et al. Comparison of secukinumab versus adalimumab efficacy on skin outcomes in psoriatic arthritis: 52‑week results from the EXCEED study. Ann Rheum Dis 2020; 79: 763–764.