Terapeutická doporučení pro profylaktickou léčbu migrény a podávání anti‑CGRP monoklonálních protilátek
Souhrn:
Grünermelová M, Nežádal T. Terapeutická doporučení pro profylaktickou léčbu migrény a podávání anti‑CGRP monoklonálních protilátek. Remedia 2020; 30: 54–59.
Migréna je jedním z nejčastějších neurologických onemocnění s velkým dopadem na kvalitu života pacientů. Ke stávající profylaktické terapii patří betablokátory, blokátory kalciových kanálů, antiepileptika, antidepresiva. Všechny tyto léky jsou pro léčbu migrény nespecifické. Monoklonální protilátky proti calcitonin‑gene related peptide (CGRP) nebo proti jeho receptoru představují novou cílenou skupinu preventivních léků. Evropská a americká doporučení upravují užití monoklonálních protilátek v prevenci migrény.
Summary:
Grunermelova M, Nezadal T. Therapeutic recommendations for a prophylactic treatment of migraine and the administration of anti‑CGRP monoclonal antibodies. Remedia 2020; 30: 54–59.
Migraine is one of the most frequent disabling neurological disorder with a major impact on these patientsʼ quality of life. Current profylactic drugs for migraine treatment contain betablockers, calcium channel blockers, antiepileptic drugs, antidepressants. All these drugs are non‑specific for the migraine therapy. Monoclonal antibodies acting on the calcitonin gene‑related peptide (CGRP) or on its receptor are new drugs targeted for migraine. EHF (European Headache Federation) and AHS (American Headache Society) guidelines contain the usage of monoclonal antibodies for migraine prevention.
Key words: profylactic drugs for migraine treatment, anti‑CGRP monoclonal antibodies, American, European and Czech guidelines
Úvod
Migréna je chronické neurologické onemocnění charakterizované opakovanými záchvaty pulzující bolesti hlavy středně těžké až těžké intenzity s trváním 4‒72 hodin, které jsou provázeny nauzeou, zvracením, fotofobií, fonofobií. Je třetí nejčastější chorobou na světě a trápí více než miliardu lidí. Prevalence dosahuje 15–18 % [1‒4]. Je šestou nejvíce handicapující nemocí podle Světové zdravotnické organizace (World Health Organization, WHO) a stává se jednou z hlavních příčin disability s výraznými ekonomickými a společenskými dopady [2].
V České republice postihuje přibližně milion lidí, z toho 170 000–200 000 trpí epizodickou migrénou s častými záchvaty a chronickou migrénou. Nejčastěji se vyskytuje epizodická migréna, která je definována počtem záchvatů nižším než 15 dní v měsíci.
Asi 30 % pacientů má bolesti hlavy více než 1× za týden a celých 8 % potom častěji než 10‒14× do měsíce. K progresi do chronické formy každoročně dojde asi u 2,5 % nemocných [5].
Chronická migréna je podle mezinárodní klasifikace International Classification of Headache Disorders 3rdedition (ICHD 3) z roku 2018 samostatnou jednotkou definovanou jako bolest hlavy vyskytující se alespoň 15 dní v měsíci po dobu minimálně tří měsíců po sobě jdoucích, přičemž nejméně osm dní musí splňovat kritéria migrény bez aury nebo s aurou. Postihuje 1‒3 % pacientů [1,6].
Tento typ bolesti je často kombinován s nadužíváním akutní medikace a s rozvojem lékově navozené bolesti hlavy (medication overuse headache, MOH). Jde o poměrně komplikovanou diagnózu definovanou jako bolest migrenózního, tenzního nebo smíšeného typu vyskytující se 15 a více dní v měsíci a nadužívání musí trvat minimálně tři měsíce. Jestliže nemocný užívá jednosložková analgetika (paracetamol, metamizol) nebo nesteroidní antirevmatika, o nadužívání se hovoří, užije li léky 15 a více dní v měsíci [1].
Užívá li kombinovaná analgetika, triptany, opioidy či přípravky s ergotaminem, jedná se o nadužívání v případě jejich užití 10 a více dní v měsíci (2‒3 dny v týdnu).
Profylaktická léčba migrény
Předpokladem účinné terapie migrény je správná diagnostika, zjištění spouštěcích faktorů, frekvence a intenzity bolestí, zhodnocení rizika progrese a transformace epizodické migrény do chronické formy s možným rozvojem MOH.
Léčba migrény je jednak akutní, se kterou zpravidla vystačíme u nižší frekvence záchvatů, jednak preventivní. Ta je indikována tam, kde má pacient čtyři a více dní s bolestí hlavy do měsíce, dále tam, kde výrazně ovlivňuje každodenní aktivity nemocného, kde jsou záchvaty prolongované, akutní léčba je neefektivní, má nežádoucí účinky nebo je z jakýchkoliv důvodů kontraindikována. V neposlední řadě tam, kde hrozí transformace epizodické formy migrény do chronické, s eventuálním rizikem MOH. Profylaktickou léčbu rovněž použijeme v případě prevence vzácných typů migrén, kde hrozí trvalý neurologický deficit, jako je tomu u hemiplegické migrény, migrény s kmenovými příznaky, migrény s prolongovanou aurou či u anamnézy migrenózního infarktu. Profylaktická léčba patří vždy do rukou neurologa.
Podle doporučených postupů je
nejvýhodnější podání monoterapie v nízké dávce, kterou
postupně titrujeme. Zásadní je podávání preventivní léčby po
dostatečně dlouhou dobu, minimálně tři měsíce. Chybou by bylo
podávání léku ukončit po několikadenním užívání
z důvodu domnělé neúčinnosti a nahradit jej lékem
jiným. Za efektivní považujeme tu profylaxi, kdy dojde
ke snížení frekvence i intenzity alespoň o polovinu.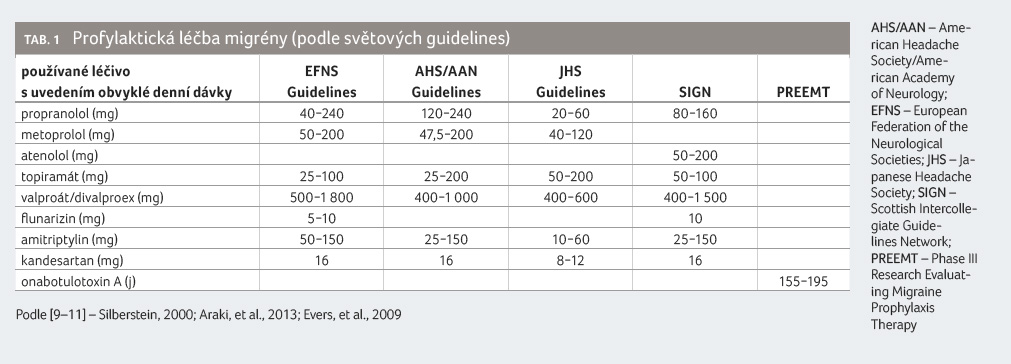
- antikonvulziva ‒ topiramát, valproát,
- betablokátory ‒ propranolol, metoprolol, bisoprolol,
- antidepresiva – amitriptylin, venlafaxin,
- antagonisté angiotenzinu II ‒ kandesartan,
- blokátory kalciových kanálů – flunarizin, cinarizin.
Je velmi důležité vybrat vždy léčbu s nejmenším rizikem a největším efektem pro konkrétního nemocného.
Doposud užívaná preventivní terapie
má svá úskalí a často není úspěšná. Počet pacientů
odpovídajících na léčbu je pouze 45 %, po šesti
měsících užívá profylaktickou léčbu pouze čtvrtina
nemocných, po 12 měsících 86 % pacientů léčbu ukončí
[5].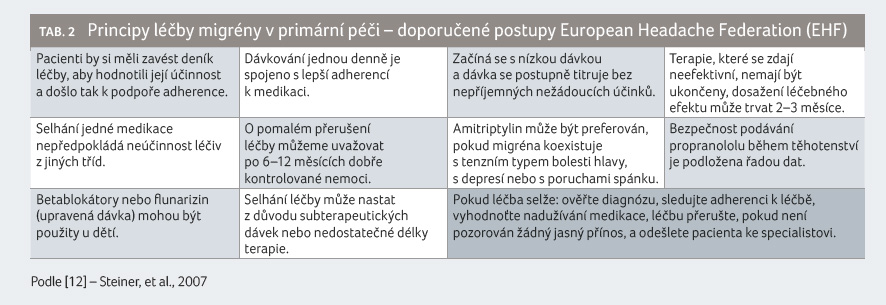
Příčinou je nedostatečná specificita, nedostatečná adherence a perzistence pacienta k léčbě, dlouhá doba nástupu efektu, nežádoucí účinky a špatná informovanost nemocného (tab. 2).
Monoklonální protilátky v terapii
migrény
Novou účinnou metodu terapie farmakorezistentní migrény představují anti CGRP protilátky. Calcitonin gene related peptide (CGRP) je klíčovým vazoaktivním neuropeptidem v patogenezi migrény. Skládá se z 37 aminokyselin. Účastní se vazodilatace meningeálních cév a rozvoje sterilního perivaskulárního zánětu. Jeho koncentrace v krvi se během neléčeného migrenózního záchvatu zvyšuje a je inhibován triptany. Bylo prokázáno, že intravenózní podání CGRP provokuje záchvat migrény [13].
Na základě těchto poznatků byly vyvinuty nové specifické léky zasahující cíleně do patogeneze migrény. Patří k nim dva typy protilátek: první jsou proti receptoru pro CGRP (erenumab) a druhé proti CGRP ligandu (galkanezumab, fremanezumab, eptinezumab).
Erenumab je plně humánní protilátka IgG2 namířená proti receptoru CGRP (schválená k léčebnému užití 17. května 2018 americkým Úřadem pro kontrolu potravin a léčiv [FDA], 1. dubna 2019 Evropskou lékovou agenturou [EMA]), fremanezumab, plně humanizovaná protilátka IgG2a s vazbou na CGRP (14. 9. 2018 – FDA, 1. 4. 2019 – EMA), galkanezumab – plně humanizovaná protilátka IgG4 cílená na CGRP ligand (27. 9. 2018 – FDA, 17. 11. 2018 – EMA).
Nyní vyvstává otázka, kteří pacienti jsou vhodní k léčbě anti CGRP protilátkami. Guidelines EHF a AHS nabízejí doporučení pro používání anti CGRP protilátek pro terapii migrény opírající se o důkazy (evidence based) a názory odborníků (expert based) [14,15].
Podle doporučení European Headache Federation (EHF) jsou to pacienti s frekventní epizodickou nebo chronickou migrénou, u kterých došlo k selhání minimálně dvou předchozích perorálních preventivních terapií z různých skupin a kteří nemohou užívat jinou preventivní léčbu v důsledku komorbidit, nežádoucích účinků nebo nedostatečné compliance.
Dle doporučení American Headache Society (AHS) jsou k léčbě anti CGRP protilátkami vhodní pacienti starší 18 let, kteří splňují diagnostická kritéria (ICHD 3) pro migrénu s aurou nebo bez ní nebo pro chronickou migrénu a zároveň netolerují alespoň dvě preventivní perorální léčby či na ně nedostatečně odpovídají.
Zhodnocení efektu by dle doporučení EHF mělo být provedeno za 3‒6 měsíců, přerušení podávání je zvažováno podle efektu po 6‒12 měsících užívání. Odpověď na léčbu se může rozvíjet i postupně. Pro pacienty s pouze částečnou odpovědí doporučuje EHF zvážit přidání jiné profylaktické perorální léčby.
AHS doporučuje zhodnocení účinku anti CGRP protilátek každé tři měsíce. Pokračování v terapii je možné při redukci počtu migrenózních dní alespoň o 50 %, současně musí být dokumentováno zlepšení v jednom vybraném testu z následujících tří – MIDAS (Migraine Disability Assessment), MPFID (Migraine Physical Function Impact Diary), HIT 6 (Headache Impact Test 6) o 5 a více bodů. Při hodnotě nad 20 bodů ve škále MIDAS se posuzuje jako signifikantní zlepšení pokles o 30 %.
Stávající perorální profylaktickou terapii EHF doporučuje u epizodické migrény ukončit před podáním anti CGRP protilátek, u chronické migrény ponechat a zvážit ukončení podle efektu protilátek. Pokračování v aplikaci botulotoxinu během podávání anti CGRP protilátek není doporučeno.
AHS doporučuje přidání protilátek ke stávající preventivní terapii, následně pak zhodnocení účinnosti před provedením dalších změn. Riziko interakcí s perorálními profylaktiky je nízké.
EHF a AHS se shodují v tom, kdy je terapie anti CGRP protilátkami kontraindikována. Je to u gravidních nebo kojících pacientek, u pacientů s abúzem alkoholu nebo drog, s těžkými kardiovaskulárními či cerebrovaskulárními onemocněními a s těžkou mentální poruchou.
Nežádoucí účinky anti CGRP
protilátek
Nežádoucí účinky monoklonálních protilátek jsou mírné a patří k nim lokální reakce v místě vpichu, mírná bolest, zarudnutí, pruritus, vyšší riziko infekcí horních cest dýchacích, močových infekcí, výjimečně únava, bolesti zad, artralgie, nauzea, zvracení [16,17].
Zatím nejsou léky podávány dostatečně dlouhou dobu, aby se zjistilo, zda nedojde k vytvoření neutralizačních protilátek. Při opakovaných odběrech toto zatím nebylo prokázáno.
Anti CGRP protilátky ‒ situace
v ČR
Léčba je indikována u pacientů s diagnózou migrény, kteří mají před iniciálním podáním terapie v průměru za poslední tři měsíce čtyři a více migrenózních dní za měsíc (monthly migraine days, MMD), a to po selhání, nedostatečné účinnosti nebo intoleranci minimálně dvou zástupců rozdílných skupin konvenční profylaktické terapie, z nichž alespoň jeden lék musí být antikovulzivum (topiramát nebo valproát), pokud tyto přípravky nejsou u pacienta kontraindikovány.
Podle našich zkušeností by alespoň u jedné ze skupin léků mělo být prokázáno selhání účinnosti při nejméně tříměsíčním užívání.
Výčet zástupců jednotlivých skupin konvenční profylaktické medikace:
- skupina 1: topiramát,
- skupina 2: valproát,
- skupina 3: betablokátory (metoprolol, bisoprolol, propranolol),
- skupina 4: antidepresiva (tricyklická antidepresiva, inhibitory zpětného vychytávání serotoninu a noradrenalinu, venlafaxin),
- skupina 5: blokátory kalciového kanálu (flunarizin a cinarizin).
U pacientů, u kterých ve třetím měsíci terapie nebude dosaženo adekvátní terapeutické odpovědi (pokles minimálně o 50 % MMD v porovnání s výchozím stavem před zahájením léčby anti CGRP protilátkami), nebudou anti CGRP protilátky dále hrazeny z prostředků veřejného zdravotního pojištění.
Terapie anti CGRP protilátkami dále nebude hrazena, pokud počet MMD v každém jednotlivém měsíci u tří po sobě jdoucích měsíců byl větší než 50 % výchozí hodnoty MMD (před zahájením léčby anti CGRP protilátkami).
Tento algoritmus je doporučen Státním ústavem pro kontrolu léčiv (SÚKL), v souladu s aktuálními doporučeními České neurologické společnosti ČLS JEP a v souladu se zahraničními doporučenými postupy v klinické praxi (tab. 3).
Léčivé přípravky budou
předepisovány pouze v centrech se zvláštní smlouvou se
zdravotními pojišťovnami na léčbu tímto typem léčivých
přípravků.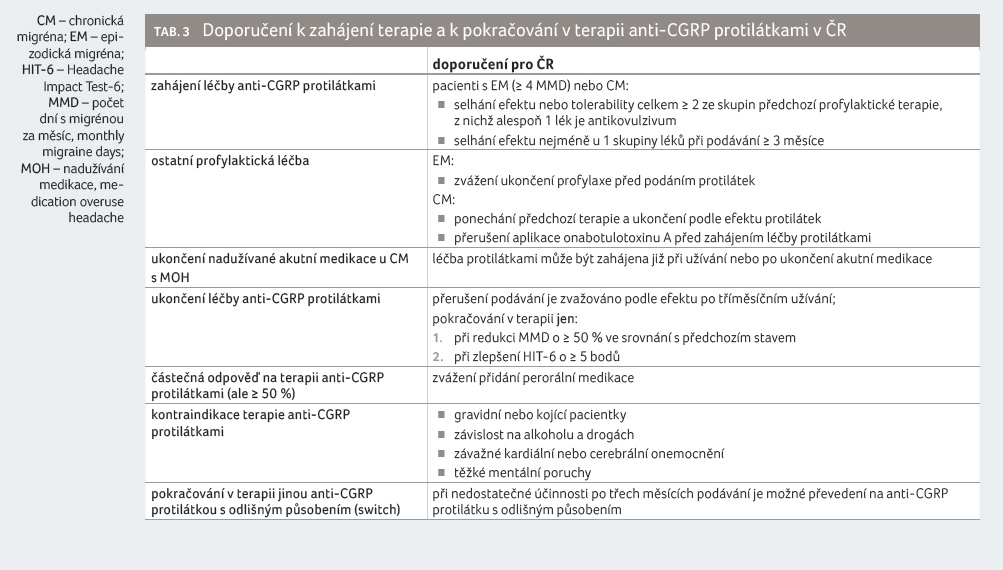
Závěr
Nová léčba anti CGRP protilátkami představuje průlom v terapii migrény. Jde o první profylaktickou terapii, která je založena na znalostech patofyziologie migrény. Je to léčba specifická, účinná, bezpečná, s dlouhodobým efektem. Představuje zásadní zmírnění zátěže pacientů a následně i zátěže pro celý zdravotní systém. Znamená začátek nové éry v terapii migrény.
Seznam použité literatury
- [1] Headache Classification Committee of the International Headache Society (IHS). The International Classification of Headache Disorders, 3rd edition. Cephalalgia 2018; 38: 1‒211.
- [2] World Health Organization. World Health Statistics 2013 (A Wealth Of Information Of Global Public Health). WHO Document Production Services: Switzerland, Geneva: 1–168.
- [3] GBD 2016 Disease and Injury Incidence and Prevalence Collaborators. Global, regional and national incidence, prevalence and years lived with disability for 328 diseases and injuries for 195 countries, 1990‒2016: a systematic analysis for the global burden of disease study 2016. Lancet 2017; 390: 1211‒1259.
- [4] Stovner LJ, Zwart JA, Hagen K, et al. Epidemiology of headache in Europe. Eur J Neurol 2006; 13: 333‒345.
- [5] Hepp Z, Dodick DW, Varon SF, et al. Persistence and switching patterns of oral migraine prophylactic medications among patients with chronic migraine: A retrospective claims analysis. Cephalalgia 2017; 37: 470–485.
- [6] Diamond S, Bigal M, Silberstein SD, et al. A Patterns of Diagnosis and Acute and Preventive Treatment for Migraine in the United States: Results from the American Migraine Prevalence and Prevention Study. Headache 2007; 47: 355−363.
- [7] Silberstein SD. Preventive Migraine Treatment. Continuum (Minneap Minn) 2015; 21: 973‒989.
- [8] Hepp, Z, Dodick DW, Varon SF, et al. Adherence to oral migraine‑preventive medications among patients with chronic migraine. Cephalalgia 2015; 35: 478–488.
- [9] Silberstein SD. Practice parameter: evidence‑based guidelines for migraine headache (an evidence‑based review): report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology 2000; 55: 754‒762.
- [10] Araki N, Takeshima T, Igarashi H, Shimizu T. Chronic Headache Clinical Practice Guideline Development Committee. Clinical Practice Guideline for Chronic Headache 2013. The Japanese Headache Society website.
- [11] Evers S, Afra J, Frese A, et al; European Federation of Neurological Societies. EFNS Guideline on the drug treatment of migraine‑revised report of an EFNS task force. Eur J Neurol 2009; 16: 968‒981.
- [12] Steiner TJ, Martelletti P. Aids for management of common headache disorders in primary care. J Headache Pain 2007; 8(Suppl 1): S2.
- [13] Kamm K, Straube A, Ruscheweyh R. Calcitonin gene‑related peptide levels in tear fluid are elevated in migraine patients compared to healthy controls. Cephalalgia 2019; 39: 033310241985664.
- [14] American Headache Society. The American Headache Society Position Statement On Integrating New Migraine Treatments Into Clinical Practise. Headache 2019; 59: 1‒18.
- [15] Sacco S, Bendtsen L, Ashina M, et al. European Headache Federation Guideline on the use of monoclonal antibodies acting on the calcitonin gene related peptide or its receptor for migraine prevention. J Headache Pain 2019; 20: 6.
- [16] Goadsby PJ, Reuter U, Hallström Y, et al. A Controlled Trial of Erenumab for Episodic Migraine. N Engl J Med 2017; 377: 2123−2132.
- [17] Dodick DW, Silberstein SD, Bigal ME, et al. Effect of Fremanezumab Compared With Placebo for Prevention of Episodic Migraine: A Randomized Clinical Trial. JAMA 2018; 319: 1999−2008.