Výsledky studie GALA – glatiramer acetát 40 mg třikrát týdně
Dvojitě slepá, randomizovaná studie GALA testovala účinnost léčby roztroušené sklerózy (RS) glatiramer acetátem (GA) podávaným v dávce 40 mg subkutánně 3krát týdně po dobu 12 měsíců v porovnání s placebem. Celkem 1404 pacientů bylo randomizovaně rozděleno v poměru 2 : 1. Relativní snížení rizika relapsů (risk ratio, RR) u pacientů léčených GA dosáhlo 34 % (RR: 0,656; konfidenční interval – 95% CI: 0,539–0,799; p < 0,0001). Progrese skóre EDSS (Expanded Disability Status Scale, škála umožňující popis stavu pacienta s roztroušenou sklerózou) za rok studie se mezi skupinami významně nelišila. Kumulativní počet gadolinium vychytávajících lézí byl o 45 % nižší (RR: 0,552; 95% CI: 0,436–0,699; p < 0,0001) a počet nových či zvětšujících se lézí v T2 váženém obraze byl o 35 % nižší (RR: 0,653; 95% CI: 0,546–0,780; p < 0,0001) u pacientů ve skupině s léčbou GA oproti skupině s placebem. Ve studii se vyskytly pouze očekávané nežádoucí účinky aplikace GA.
Úvod
Roztroušená skleróza (RS) je onemocnění postihující více než 2,5 milionu lidí na světě a bez léčby vede k trvalému neurologickému postižení. Ačkoliv nejsou plně objasněny všechny aspekty patofyziologie RS a nemoc nejsme schopni vyléčit, máme již téměř třicet let k dispozici léky významně zmírňující postup onemocnění (disease modifying drugs – DMD, chorobu modifikující léky). K jejich objevu došlo ve většině případů na základě empirických zkušeností. Léky první volby, jejichž podávání zahajujeme po diagnóze roztroušené sklerózy, jsou interferony beta (IFNβ) a glatiramer acetát (GA).
Glatiramer acetát je acetátová sůl různě dlouhých syntetických polypeptidů obsahující čtyři aminokyseliny (kyselina L-glutamová, L-lysin, L-alanin, L-tyrosin) a je výsledkem patentovaného výrobního procesu. Přesný mechanismus, kterým GA zmírňuje následky RS, není znám. Již od prvních kroků vývoje GA ve Weizmannově institutu věd v Izraeli v roce 1967 je zřejmé, že tato směs polypeptidů zmírňuje průběh a následky zánětu na podkladě autoimunitní reakce proti antigenům myelinu, což bylo ukázáno jak na zvířecím modelu RS, tak i v následných klinických zkouškách [1–3].
Glatiramer acetát podávaný v dávce 20 mg subkutánně (s.c.) denně byl schválen k léčbě remitentní RS na základě tří dvojitě zaslepených placebem kontrolovaných studií s celkovým počtem 538 pacientů, v nichž bylo pozorováno signifikantní snížení počtu relapsů ve srovnání s placebem; GA 20 mg s.c. denně je také indikován k léčbě pacientů s tzv. klinicky izolovanou epizodou neurologických příznaků a rizikem rozvoje RS. V rámci rozvoje poznatků o glatiramer acetátu v léčbě RS přistoupila farmaceutická společnost k testování účinnosti GA aplikovaného dávce 40 mg s.c. třikrát týdně.
Pacienti a metodika
Studie GALA (Glatiramer Acetate Low-frequency Administration) je randomizovaná, dvojitě slepá, placebem kontrolovaná studie fáze III, která testovala bezpečnost a účinnost léčby glatiramer acetátem podávaným v dávce 40 mg s.c. třikrát týdně po 12 měsíců [4]. Do studie byli zahrnuti pacienti s RS dle revidovaných McDonaldových kritérií ve věku 18–55 let, jejichž onemocnění dosahovalo intenzity stupně 0–5,5 EDSS (Expanded Disability Status Scale, škála kvantifikující postižení nervového systému a umožňující popis stavu pacienta s roztroušenou sklerózou). Aktivita onemocnění před nástupem do studie byla charakterizována přítomností nejméně jedné dokumentované ataky v předchozích 12 měsících nebo přítomností dvou atak v předchozích 24 měsících nebo přítomností jedné ataky v období 12 až 24 měsíců před začátkem studie a zároveň nálezem nejméně jedné gadolinium vychytávající léze na MR (magnetická rezonance) zobrazení mozku v posledním roce před studií. Do studie mohli být zahrnuti pacienti léčení v minulosti GA nebo IFNβ s odstupem nejméně dvou měsíců před započetím studie a pacienti léčení v minulosti mitoxantronem a chronickou kortikoterapií s odstupem nejméně šesti měsíců a pacienti léčení monoklonálními protilátkami s odstupem nejméně dvou let. Pacienti s progresivní RS byli ze studie vyloučeni. Randomizace byla provedena v poměru 2 : 1 na skupinu s léčbou GA 40 mg s.c. podávaným třikrát týdně a na skupinu s podáváním placeba (obsahujícího 40 mg mannitolu) s.c. třikrát týdně.
Charakteristika pacientů
Ve studii bylo randomizováno celkem 1404 pacientů. Ve skupině s léčbou GA (n = 943) byl průměrný věk pacientů 37,4 roku (SD – směrodatná odchylka – 9,4), skóre EDSS 2,8 (SD 1,2), s délkou onemocnění 7,7 roku (SD 6,7) a objemem T2 lézí 19,7 ml (SD 20,7). Pacienti randomizovaní do skupiny s placebem (n = 461) měli průměrný věk 38,1 roku (SD 9,2), skóre EDSS 2,7 (SD 1,2), délku onemocnění 7,6 roku (SD 6,4) a objem T2 lézí 17,4 ml (SD 17,4). Předchozí léčbu DMD dostávalo 13,6 % pacientů ve studii.
Výsledky
Tolerabilita a nežádoucí účinky
Ve studii byly pozorovány jen známé nežádoucí účinky léčby GA, tab. 1. Erytém v místě vpichu se vyskytl u 20,9 % pacientů ze skupiny s léčbou GA a u 1,5 % pacientů ze skupiny placeba, pruritus se vyskytl u 5,9 % pacientů ze skupiny s léčbou GA a u 0 % pacientů z těch, kteří dostávali placebo. Systémová poinjekční reakce po aplikaci GA se vyskytla u 7,6 % pacientů (u 1,7 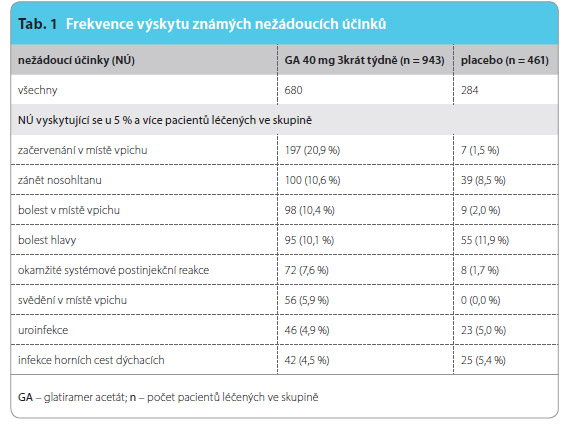 % ve skupině s placebem ) a manifestovala se dyspneou (3,1 %), pocity horka (1,3 %), tachykardií (1,1 %), začervenáním (1,0 %), palpitacemi (1,0 %), bolestí na hrudi (0,8 %) a dalšími méně častými příznaky. Závažné nežádoucí účinky byly zaznamenány u 4,5 % pacientů v obou skupinách. Studii nedokončilo 8,9 % pacientů ze skupiny s léčbou GA a 6,7 % pacientů ze skupiny placeba. Výskyt nežádoucího účinku byl nejčastějším důvodem k přerušení studie (3,1 % pacientů ze skupiny s GA, 1,3 % pacientů ze skupiny placeba).
% ve skupině s placebem ) a manifestovala se dyspneou (3,1 %), pocity horka (1,3 %), tachykardií (1,1 %), začervenáním (1,0 %), palpitacemi (1,0 %), bolestí na hrudi (0,8 %) a dalšími méně častými příznaky. Závažné nežádoucí účinky byly zaznamenány u 4,5 % pacientů v obou skupinách. Studii nedokončilo 8,9 % pacientů ze skupiny s léčbou GA a 6,7 % pacientů ze skupiny placeba. Výskyt nežádoucího účinku byl nejčastějším důvodem k přerušení studie (3,1 % pacientů ze skupiny s GA, 1,3 % pacientů ze skupiny placeba).
Klinická měření
Průměrná frekvence relapsů za rok, která představovala hlavní měřítko účinku léčby, byla ve skupině s GA 0,331 a v placebové skupině 0,505. Relativní snížení rizika (RRR – relative risk reduction) relapsu u pacientů léčených GA dosáhlo 34 % (GA vs. placebo – RR: 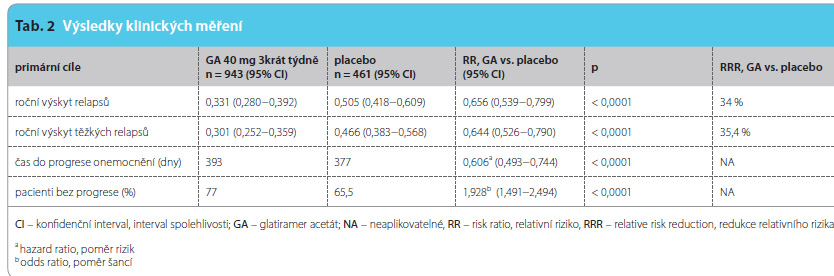 0,656; CI: 0,539–0,799; p < 0,0001). Doba do výskytu prvního relapsu ve studii byla statisticky významně delší u skupiny s léčbou GA ve srovnání se skupinou dostávající placebo (393 vs. 377 dní; poměr rizik – hazard ratio – HR: 0,606; 95% CI: 0,493–0,744), tab. 2. Progrese EDSS za rok studie se mezi skupinami významně nelišila.
0,656; CI: 0,539–0,799; p < 0,0001). Doba do výskytu prvního relapsu ve studii byla statisticky významně delší u skupiny s léčbou GA ve srovnání se skupinou dostávající placebo (393 vs. 377 dní; poměr rizik – hazard ratio – HR: 0,606; 95% CI: 0,493–0,744), tab. 2. Progrese EDSS za rok studie se mezi skupinami významně nelišila.
Měření pomocí magnetické rezonance
Zobrazení pomocí MR ve studii GALA přineslo následující výsledky: kumulativní počet gadolinium vychytávajících lézí byl o 45 % nižší (RR: 0,552; 95% CI: 0,436–0,699; p < 0,0001) a počet nových či zvětšujících se lézí v T2 váženém obraze byl o 35 % nižší (RR: 0,653; 95% CI: 0,546–0,780; p < 0,0001) u pacientů ve skupině s GA než ve skupině s placebem.
Závěr
Optimální dávka a frekvence podávání glatiramer acetátu byla v posledních deseti letech předmětem několika studií.
Studie fáze III porovnávající po dobu dvou let léčbu pacientů s RS glatiramer acetátem v dávce 20 mg s.c. denně (n = 44) s léčbou GA v dávce 40 mg denně (n = 46) ukázala pozitivní trend v klesajícím počtu nových gadolinium vychytávajících lézí v sedmém, osmém a devátém měsíci léčby u skupiny léčené vyšší dávkou GA (relativní snížení rizika lézí o 38 %; p = 0,0051) a trend ke zvýšení poměrného počtu pacientů bez relapsů onemocnění (p = 0,0183) [5].
Studii GALA předcházelo i několik explorativních studií iniciovaných Dr. O. Khanem, které se zabývaly sníženou frekvencí aplikace GA. Závěry dvouleté studie, která testovala u 30 pacientů účinek léčby glatiramer acetátem podávaným v dávce 20 mg s.c. ob den, srovnávala jej s účinkem GA podávaným ve stejné dávce denně a měřila účinek kombinovaným srovnáváním kontrolních zobrazení na MR a klinických výsledků, byly zveřejněny v roce 2008 na WCTRIMS (World Congress on Treatment and Research in Multiple Sclerosis) v Montrealu ve formě abstraktu [5]. Výsledky druhé dvouleté studie byly prezentovány na kongresu AAN (American Academy of Neurology) v roce 2010 [7]. Ve studii bylo randomizováno 48 klinicky stabilních pacientů léčených GA v dávce 20 mg na skupinu s pokračováním léčby GA podávaným v dávce 20 mg s.c. denně nebo GA 20 mg s.c. dvakrát týdně a sledováno po dobu dvou let. Ani jedna z těchto malých explorativních studií nezjistila žádný rozdíl ve frekvenci výskytu relapsů či změně objemu lézí na MR.
Studie GALA prokázala, že léčba glatiramer acetátem v dávce 40 mg s.c. třikrát týdně po dobu 12 měsíců v porovnání s placebem vedla k významně nižšímu výskytu relapsů a účinnost léčby byla potvrzena i zobrazovacími metodami. Bezpečnost a tolerabilita podávání glatiramer acetátu v tomto režimu je porovnatelná s podáváním glatiramer acetátu v dávce 20 mg denně, přičemž podávání nižšího počtu injekcí týdně je pro pacienty méně invazivní.
Seznam použité literatury
- [1] Webb C, Teitelbaum D, Arnon R, Sela M. In vivo and in vitro immunological cross-reactions between basic encephalitogen and synthetic basic polypeptides capable of suppressing experimental allergic encephalomyelitis. Eur J Immunol 1973; 3: 279–286.
- [2] Teitelbaum D, Webb C, Bree M, et al. Suppression of experimental allergic encephalomyelitis in rhesus monkeys by a synthetic basic copolymer. Clin Immunol Immunopathol 1974; 3: 2561–262.
- [3] Abramsky O, Teitelbaum D, Arnon R. Effect of a synthetic polypeptide (copolymer 1) on patients with multiple sclerosis and with acute disseminated encephalomyelitis. J Neurol Sci 1977; 31: 433–438.
- [4] Khan O, Rieckmann P, Boyko A, et al. GALA study group. Three times weekly glatiramer acetate in relapsing-remitting multiple sclerosis. Ann Neurol 2013; 6: 705−713.
- [5] Cohen JA, Rovaris M, Goodman AD, et al. Randomized, double-blind, dose-comparison study of glatiramer acetate in relapsing-remitting multiple sclerosis. Neurology 2007; 68: 939–944.
- [6] Khan O, Caon C, Zak I, et al. Randomized, prospective, rater blinded, four-year, pilot study to compare the effect of daily versus every-other-day glatiramer acetate 20 mg subcutaneous injections in relapsing-remitting multiple sclerosis. Mult Scler 2008; 14 (suppl 1): S296.
- [7] Khan O, Perumal J, Caon C, et al. Glatiramer acetate 20mg subcutaneous twice-weekly versus daily injections: results of a pilot, prospective, randomised, and rater-blinded clinical and MRI 2-year study in relapsing-remitting multiple sclerosis. Mult Scler 2009; 15 (suppl 2): S249–S250.