Tradiční hepatoprotektiva v terapii MASLD. Jaká je klinická evidence účinku?
Souhrn
Juřica J. Tradiční hepatoprotektiva v terapii MASLD. Jaká je klinická evidence účinku? Remedia 2025; 35: 64–74.
Článek v úvodu představuje jedno z nejčastějších onemocnění jater – nealkoholovou tukovou chorobu jater (NAFLD) a změnu v jejím názvosloví prezentovanou odbornými společnostmi v roce 2022. Nově se NAFLD označuje jako jaterní steatóza asociovaná s metabolickou dysfunkcí (MASLD). Dále jsou krátce přiblíženy možnosti farmakoterapie. Hlavním cílem tohoto přehledového článku je však seznámit čtenáře s evidencí účinku tradičních hepatoprotektiv registrovaných v ČR – tedy silymarinu a esenciálních fosfolipidů pro terapii MASLD. V databázi Web of Science byly dle klíčových slov uvedených v metodice vyhledány studie, které hodnotily účinek obou látek u pacientů s MASLD/NAFLD. Pro vyhledání nebylo aplikováno žádné omezení týkající se počtu pacientů, délky sledování nebo data publikování. Bylo nalezeno šest publikací hodnotících esenciální fosfolipidy a devět publikací prezentujících účinky silymarinu v terapii MASLD. Na základě nalezených publikací lze shrnout, že přestože esenciální fosfolipidy i silymarin snižují hodnoty některých laboratorních markerů MASLD, současná evidence o účinnosti těchto přípravků trpí nedostatkem přesvědčivých důkazů pro jejich rutinní klinické využití. To se nakonec odráží i v aktuálních klinických mezinárodních doporučeních, kde nejsou tradiční hepatoprotektiva v terapii MASLD doporučována.
Klíčová slova: MASLD – NAFLD – silymarin – esenciální fosfolipidy.
Summary
Jurica J. Traditional hepatoprotective agents in MASLD therapy. What is the clinical evidence of effect? Remedia 2025; 35: 64–74.
The article discusses non‑alcoholic fatty liver disease (NAFLD), one of the most common liver diseases, and its renaming to metabolic dysfunction‑associated liver steatosis (MASLD) by professional societies in 2022. It briefly outlines pharmacotherapy options but primarily focuses on evaluating the efficacy of traditional hepatoprotective agents registered in the Czech Republic – silymarin and essential phospholipids – for MASLD treatment. A systematic search of the Web of Science database identified six studies on essential phospholipids and nine on silymarin; the search was made without restrictions on patient numbers, follow‑up duration, or publication period. While both agents improve some laboratory parameters, the evidence supporting their routine clinical use remains insufficient. This is reflected in current clinical guidelines, which do not recommend traditional hepatoprotective agents for MASLD treatment.
Key words: MASLD – NAFLD – silymarin – essential phospholipids.
Úvod
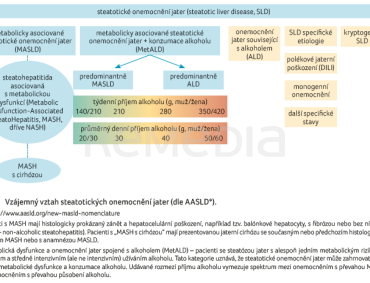 Jedním z nejčastějších onemocnění jater je v současnosti nealkoholová tuková choroba jater (non‑alcoholic fatty liver disease, NAFLD). Jedná se o spektrum onemocnění charakterizované steatózou jater, a to za stavu bez konzumace alkoholu. Jeho prevalence ve vyspělých zemích stoupá, dosahuje v současnosti přes 30 % a odhaduje se, že v roce 2035 dosáhne 50 % [1–3]. Obezita je jedním z hlavních rizikových faktorů, přičemž prevalence ve vyspělých zemích přesahuje 60 % a stále narůstá [4]. Od roku 2018 došlo k několika změnám v terminologii a přístupu k NAFLD. V červnu 2023 došlo na Delphi panelu ke konsenzu více odborných společností pod vedením Americké asociace pro studium jater (American Association for the Study of Liver Diseases, AASLD) a pro NAFLD bylo doporučeno nové označení, na konci roku 2024 odsouhlasené výborem České hepatologické společnosti ČLS JEP: metabolickou dysfunkcí podmíněné steatotické onemocnění jater (metabolic dysfunction‑associated steatotic liver disease, MASLD) [5]. Novou nomenklaturu steatotických onemocnění jater shrnuje obrázek 1. V roce 2024 Evropská asociace pro studium jater (European Association for the Study of the Liver, EASL) spolu s Evropskou asociací pro studium diabetu (European Association for the Study of Diabetes, EASD) a Evropskou asociací pro studium obezity (European Association for the Study of Obesity, EASO) publikovala doporučené postupy k managementu MASLD [6].
Jedním z nejčastějších onemocnění jater je v současnosti nealkoholová tuková choroba jater (non‑alcoholic fatty liver disease, NAFLD). Jedná se o spektrum onemocnění charakterizované steatózou jater, a to za stavu bez konzumace alkoholu. Jeho prevalence ve vyspělých zemích stoupá, dosahuje v současnosti přes 30 % a odhaduje se, že v roce 2035 dosáhne 50 % [1–3]. Obezita je jedním z hlavních rizikových faktorů, přičemž prevalence ve vyspělých zemích přesahuje 60 % a stále narůstá [4]. Od roku 2018 došlo k několika změnám v terminologii a přístupu k NAFLD. V červnu 2023 došlo na Delphi panelu ke konsenzu více odborných společností pod vedením Americké asociace pro studium jater (American Association for the Study of Liver Diseases, AASLD) a pro NAFLD bylo doporučeno nové označení, na konci roku 2024 odsouhlasené výborem České hepatologické společnosti ČLS JEP: metabolickou dysfunkcí podmíněné steatotické onemocnění jater (metabolic dysfunction‑associated steatotic liver disease, MASLD) [5]. Novou nomenklaturu steatotických onemocnění jater shrnuje obrázek 1. V roce 2024 Evropská asociace pro studium jater (European Association for the Study of the Liver, EASL) spolu s Evropskou asociací pro studium diabetu (European Association for the Study of Diabetes, EASD) a Evropskou asociací pro studium obezity (European Association for the Study of Obesity, EASO) publikovala doporučené postupy k managementu MASLD [6].
Stěžejním bodem v diagnostice MASLD je průkaz jaterní steatózy, nicméně k potvrzení diagnózy je zároveň nezbytná přítomnost alespoň jednoho z kardiometabolických rizikových faktorů, mezi které patří [6]:
- nadváha nebo obezita – index tělesné hmotnosti (body mass index, BMI) > 25 kg/m2 signalizující nadměrné ukládání tuku v těle, především ve viscerální oblasti. Pro Asiaty je hranicí BMI 23 nebo obvod pasu ≥ 94 cm (muži) a ≥ 80 cm (ženy);
- (pre)diabetes – porucha metabolismu glukózy zahrnující prediabetický stav (zvýšená glykemie nalačno nebo porucha glukózové tolerance) nebo diagnostikovaný diabetes mellitus 2. typu (T2DM) nebo lačná glykemie ≥ 5,6 mmol/l nebo postprandiální (2 h) glykemie ≥ 7,8 mmol/l nebo hodnota glykovaného hemoglobinu (HbA1c) ≥ 5,7 %;
- arteriální hypertenze – přetrvávající zvýšený krevní tlak (TK), který zatěžuje kardiovaskulární (KV) systém a může přispívat k poškození jaterních cév. TK ≥ 130/85 mm Hg nebo již zavedená antihypertenzní léčba;
- dyslipidemie – zvýšená hodnota LDL cholesterolu, snížená hodnota HDL cholesterolu nebo zvýšené hodnoty triglyceridů. HDL‑C ≤ 1,0 mmol/l (muži) a ≤ 1,3 mmol/l (ženy) nebo již zavedená hypolipidemická terapie.
MASLD zahrnuje spektrum stavů od benigní steatózy jater po závažnější formu – steatohepatitidu – spojenou s metabolickou dysfunkcí (MASH), dříve označovanou jako nealkoholická steatohepatitida (NASH). Zatímco u MASLD je přítomna tuková infiltrace jater bez zánětlivých změn, MASH se vyznačuje zánětem a apoptózou, což může vést k fibróze a cirhóze [2,5,6]. Patogeneze MASLD není zcela objasněna, ale klíčovou roli hraje inzulinová rezistence, nerovnováha mezi příjmem energie a metabolickými potřebami a systémový zánět. Nejčastěji zmiňovanou teorií je klíčová role inzulinové rezistence, která vede k jaterní steatóze a potenciálně i ke steatohepatitidě. Další hypotézy naznačují potřebu tzv. druhého zásahu (second hit), tedy dalšího oxidačního poškození, které přispívá ke vzniku nekroinflamatorní složky steatohepatitidy. Mezi možné faktory patogeneze se řadí rovněž dysbalance hormonů gastrointestinálního traktu (GIT) a hormonů tukové tkáně (gastrin, sekretin, GIP, VIP, leptin, resistin, adiponektin), deficit antioxidantů a vliv střevního mikrobiomu. Z genetických faktorů jsou to především jednonukleotidové polymorfismy PNPLA3, TM6SF2, GCKR, MBOAT7 a HSD17B13 [7]. Genetické faktory mohou tak zvyšovat riziko progrese do fibrózní formy onemocnění. Většina pacientů s MASLD je asymptomatická a onemocnění je často odhaleno náhodně při laboratorních testech (zvýšené hodnoty aminotransferáz s vyloučením ostatních příčin) nebo zobrazovacími metodami. Pacienti s MASH mohou pociťovat únavu, malátnost nebo bolesti v pravém horním kvadrantu břicha. Pokročilé stadium může vést k dekompenzované cirhóze. Diagnostika MASLD zahrnuje vyloučení jiných příčin jaterních onemocnění a potvrzení steatózy pomocí zobrazovacích metod a biochemických vyšetření. V některých případech je nezbytné provedení jaterní biopsie k posouzení závažnosti onemocnění [6,8]. Recentní přehled věnovaný MASLD byl nedávno publikován autory doporučených postupů České hepatologické společnosti ČLS JEP [1].
 Diagnostika MASLD se opírá nejen o průkaz steatózy, ale i o komplexní hodnocení metabolického zdraví pacienta. Pro screening MASLD může být použit jednoduchý nástroj – tzv. FIB‑4 skóre, které bylo původně vyvinuto pro predikci jaterní fibrózy u pacientů s koinfekcí virem lidské imunodeficience/virem hepatitidy C (HIV/HCV) [1,6,9,10]. FIB‑4 se začalo během posledních dvou let rutinně stanovovat v mnoha českých biochemických laboratořích. Sestává z běžně stanovovaných a snadno dostupných parametrů: alaninaminotransferáza (ALT), aspartátaminotransferáza (AST), věk, a počet trombocytů (obr. 2). Jeho použití v rutinní praxi pro screening a diagnostiku jaterních onemocnění je doporučeno téměř všemi odbornými organizacemi (doporučené postupy České hepatologické společnosti ČLS JEP, EASL, AASLD) a také některými diabetologickými společnostmi. FIB‑4 skóre může být také použito jako jeden z nástrojů pro monitoring terapie [11].
Diagnostika MASLD se opírá nejen o průkaz steatózy, ale i o komplexní hodnocení metabolického zdraví pacienta. Pro screening MASLD může být použit jednoduchý nástroj – tzv. FIB‑4 skóre, které bylo původně vyvinuto pro predikci jaterní fibrózy u pacientů s koinfekcí virem lidské imunodeficience/virem hepatitidy C (HIV/HCV) [1,6,9,10]. FIB‑4 se začalo během posledních dvou let rutinně stanovovat v mnoha českých biochemických laboratořích. Sestává z běžně stanovovaných a snadno dostupných parametrů: alaninaminotransferáza (ALT), aspartátaminotransferáza (AST), věk, a počet trombocytů (obr. 2). Jeho použití v rutinní praxi pro screening a diagnostiku jaterních onemocnění je doporučeno téměř všemi odbornými organizacemi (doporučené postupy České hepatologické společnosti ČLS JEP, EASL, AASLD) a také některými diabetologickými společnostmi. FIB‑4 skóre může být také použito jako jeden z nástrojů pro monitoring terapie [11].
MASLD není v obecné populaci spojeno se zvýšeným rizikem jaterních komplikací [12], ale zvyšuje riziko extrahepatálních onemocnění, zejména s rostoucím počtem kardiometabolických rizikových faktorů. MASLD je spojeno s vyšším rizikem KV onemocnění [13,14] a zvyšuje riziko chronického onemocnění ledvin [15]. Překvapivě MASLD není spojeno se zvýšenou celkovou mortalitou na nádorová onemocnění [15], ale je asociováno s vyšším rizikem vzniku hepatocelulárního karcinomu (HCC) a některých extrahepatálních nádorů, především štítné žlázy a GIT, zejména karcinomu kolorekta [16].
Terapie MASLD
Nefarmakologická léčba (režimová a dietní opatření) představuje základní pilíř terapie MASLD a je doporučována všem pacientům bez ohledu na závažnost onemocnění [6]. Cílem je nejen zlepšení jaterních parametrů, ale také snížení KV rizika. Dosažení úbytku hmotnosti alespoň o 5 % výrazně snižuje jaterní steatózu, zatímco redukce o 7–10 % je spojena s ústupem jaterního zánětu a zlepšením histologického obrazu [2,6]. Důležitá je dlouhodobá udržitelnost hmotnostního úbytku v kombinaci se změnou životního stylu [6]. Ta zahrnuje abstinenci od pití alkoholu snižující riziko progrese onemocnění [8,9] a pravidelnou fyzickou aktivitu (nejlépe více než 150 minut týdně středně intenzivní nebo 75 minut týdně intenzivní fyzické aktivity) [6]. Dalším krokem je optimalizace rizikových faktorů, jako jsou dyslipidemie, hypertenze a T2DM, a zajištění očkování proti hepatitidě A a B u rizikových pacientů. V případech, kdy změny životního stylu nestačí, lze zvážit bariatrickou chirurgii, která prokázala příznivý vliv na jaterní histologii u pacientů s pokročilou fibrózou [2,17]. V několika observačních studiích různé kvality byla překvapivě nalezena jako protektivní faktor konzumace kávy, ať už s kofeinem, nebo bez něj [18,19]. Riziko MASLD a fibrózy bylo nižší u osob, které pily kávu, ve srovnání s těmi, kteří kávu nepili. Výsledky byly silnější a konzistentnější pro fibrózu než pro steatózu [6,18,19].
Farmakologická léčba MASLD je vyhrazena pro pacienty s biopsií potvrzenou steatohepatitidou (MASH) a fibrózou stupně ≥ 2, kteří nedosáhli zlepšení pomocí nefarmakologických opatření. Prvním a jediným léčivem s indikací MASLD (resp. NAFLD) je resmetirom, schválený americkým Úřadem pro kontrolu potravin a léčiv (FDA) v březnu 2024, avšak v EU zatím registrován nebyl. Resmetirom je parciální agonista receptoru pro hormony štítné žlázy beta (THR‑β) (dominantní receptor pro hormony štítné žlázy v játrech) [6,20]. Stimulace THR‑β v játrech zvyšuje metabolismus jaterních lipidů/snižuje hromadění tuku v játrech. Všechna další léčiva jsou tedy v indikaci MASLD užívána sice lege artis a na základě doporučení odborných společností, nicméně off‑label. Bohužel resmetirom zatím nebyl registrován v České republice, a tak v současnosti nejsou v ČR k dispozici žádná specifická léčiva schválená přímo pro MASLD. Některá léčiva však vykazují potenciál pro cílenou terapii tohoto onemocnění. Proto je terapie zaměřena na kontrolu komorbidit, jako jsou T2DM, dyslipidemie a obezita, s individuálním zhodnocením rizik a přínosů terapie.
U pacientů s T2DM nebo obezitou prokázali agonisté receptoru pro glukagonu podobný peptid 1 (GLP‑1 RA) liraglutid a semaglutid snížení aktivit jaterních enzymů a lipidů, což podporuje racionální využití těchto léků u MASH [21]. Největší dostupná studie se semaglutidem u pacientů s MASH prokázala remisi steatohepatitidy, ale bez významné redukce fibrózy [22]. Ve velkých, dobře provedených studiích fáze III nebylo dosaženo podáváním GLP‑1RA zlepšení histologického nálezu, a tak tyto přípravky nejsou doporučovány v terapii MASH. Pioglitazon omezuje fibrózu, steatózu a zánět u pacientů s necirhotickou MASH, zejména u pacientů s T2DM. Přesto není doporučován jako primární terapie MASLD (nedostatečně robustní průkaz přínosů ve 3. fázi klinického hodnocení), navíc má známé nežádoucí účinky: zvyšování hmotnosti, srdeční selhání, osteoporóza, vzácně případy akutního jaterního selhání) [2,6]. Bohužel ani další nadějná léčiva ze skupiny antidiabetik (inhibitory SGLT2 a metformin) alespoň prozatím nemají dostatečnou evidenci, na jejímž základě by byla doporučena k terapii MASH (v rámci progrese MASLD). Nicméně tato léčiva jsou v případě MASLD bezpečná a měla by být používána v rámci svých indikací (T2DM, srdeční selhání a chronické onemocnění ledvin) [6]. Pro použití jiných antidiabetik jako cílené terapie MASH nejsou dostatečné důkazy [6].
Vitamin E je antioxidant s protizánětlivými a antiapoptotickými účinky, který snižuje novotvorbu lipidů a jeho vyšší sérové koncentrace jsou asociovány s nižší pravděpodobností rozvoje MASLD [23]. Ačkoliv suplementace vitaminu E zmírnila steatózu a aktivitu onemocnění u pacientů s MASH bez diabetu [24], vliv na fibrózu a KV mortalitu zůstává neprůkazný [6]. Kyselina ursodeoxycholová (UDCA) má hepatoprotektivní účinky s antioxidačními, imunomodulačními, protizánětlivými a antiapoptotickými vlastnostmi [6]. Ačkoliv studie prokázaly snížení aktivity ALT, AST, GGT (gama‑glutamyltransferázy), ALP (alkalické fosfatázy), hodnot bilirubinu [25] a dobrý bezpečnostní profil, nebyl potvrzen významný histologický přínos u MASH [6,26,27]. Statiny jsou často indikovány u pacientů s MASLD k prevenci KV příhod a jsou považovány za bezpečné. Přestože snižují riziko MASLD, MASH a jaterní fibrózy [28], pro průkaz jejich účinnosti specificky pro léčbu MASH doposud chybějí velké studie [6]. Podobný kardioprotektivní efekt prokázala i kyselina acetylsalicylová, která údajně brání progresi fibrózy [29]. Silymarin, extrakt z ostropestřce mariánského, může zlepšit laboratorní ukazatele MASLD (pokles aktivit jaterních transferáz), avšak dostupné malé randomizované kontrolované studie (RCT) neprokázaly histologické zlepšení u MASH [6,30,31].
Jaká je evidence účinnosti hepatoprotektiv dostupných v ČR v terapii MASLD?
V České republice máme aktuálně dostupná pouze dvě léčiva ve skupině Hepatoprotektiva (ATCA05BA). Jedná se o silymarin (standardizovaný extrakt ostropestřce mariánského, Silybum marianum) a esenciální fosfolipidy (EPL). Protože jsou (měřeno celkovou spotřebou v ČR) obě léčiva velmi oblíbená v různých indikacích (často off‑label), s ohledem na prevalenci MASLD bylo cílem tohoto přehledového článku zhodnotit jejich přínos v terapii MASLD dle principů medicíny založené na důkazech (EBM).
Preklinické nebo in vitro studie by neměly přímo ovlivňovat klinická doporučení. Komplexní povaha lidské fyziologie a multifaktoriální etiologie MASLD znamenají, že výsledky pozorované v laboratorních podmínkách nemusejí být přenositelné do klinické praxe. Historie medicíny nabízí varovné příklady předčasného klinického přijetí na základě preklinických důkazů. Významným příkladem je užívání některých antiarytmik v 80. letech 20. století (enkainid, flekainid, moricizin), která byla předepisována na základě jejich schopnosti potlačit ventrikulární ektopii v preklinických modelech. Později (v r. 1991) však studie CAST odhalila, že tato léčiva ve skutečnosti zvyšovala úmrtnost u pacientů po infarktu myokardu, což vedlo k tisícům potenciálně preventabilních úmrtí [32,33]. Přestože problematika hepatoprotektiv je diametrálně odlišná a současná hepatoprotektiva mají vcelku dobře prověřenou bezpečnost, tento historický precedens slouží jako důrazné varování před možnými důsledky implementace léčby bez dostatečných klinických důkazů pouze na základě „expert opinion“.
Pro ověření klinické evidence účinku hepatoprotektiv u MASLD bylo provedeno vyhledání klinických studií v databázi Web of Science (WOS). Přestože jsou k nalezení různá review a metaanalýzy, při bližším prozkoumání některých těchto zdrojů (např. Dajani, et al., 2020 [34]) vyjde najevo, že zařazené „studie“ jsou např. konferenčními abstrakty, neuvádějí dávky EPL, popř. EPL jsou podávány současně s jinou terapií, jejíž efekt vzhledem k uspořádání studie nelze odlišit nebo je efekt porovnáván s tradiční čínskou medicínou nebo směsí extraktů léčivých rostlin [35]. Proto nelze bezmezně spoléhat na autory a redakční recenzní řízení, které v některých časopisech probíhá zvláštním a v poslední době široce kritizovaným způsobem. Z toho důvodu bylo provedeno vlastní vyhledání klinických studií dle níže uvedeného postupu a závěry porovnány s klinickými doporučeními. Pro posouzení současného stavu poznání byly systematicky vyhledány dostupné publikace sledující použití EPL a silymarinu v prevenci a/nebo terapii steatotického onemocnění jater. Aby nebyly vyloučeny studie s hraniční problematikou, byly v databázi WOS klíčovými slovy pro vyhledávání řetězce: ALL = (hepatoprotective OR liver failure OR drug induced liver injury OR DILI OR hepatic failure OR hepatopathy OR MASLD OR NAFLD OR MASH) AND ALL = (EPL OR essential phospholipid* OR polyenylphosphatidylcholine OR polyene phosphatidylcholine) v případě esenciálních fosfolipidů a ALL = (MASLD OR NAFLD OR ALD OR MASH OR NASH OR steatotic liver OR fatty liver OR steatohepatitis OR hepatoprotective OR liver failure OR drug induced liver injury OR DILI OR hepatic failure OR hepatopathy) AND ALL = (sylimarin* OR milk thistle OR silybum marianum OR silybin* OR silybini*) v případě silymarinu.
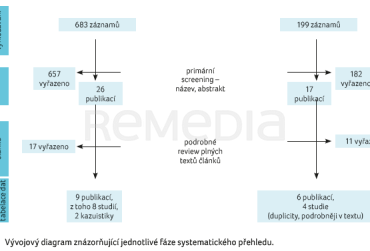 Vyhledání proběhlo k datu 15. 1. 2025 a další zpracování probíhalo dle diagramu na obrázku 3. Vstupní kritéria: 1. hodnocené léčivo (EPL/silymarin, resp. extrakt z ostropestřce mariánského), 2. klinické hodnocení efektu u pacientů se steatotickým onemocněním jater (nealkoholovým – MASLD/NAFLD/NASH/MASH). Vylučovací kritéria: 1. preklinické studie, 2. nebylo možno hodnotit efekt samotného léčiva (kombinace, nejasná dávka), 3. nebylo možno identifikovat cílovou podskupinu pacientů v rámci hodnoceného souboru, 4. review, systematický/narativní přehled. Nalezené studie jsou pro obě látky níže prezentovány v tabulkách a komentovány dle EBM [35].
Vyhledání proběhlo k datu 15. 1. 2025 a další zpracování probíhalo dle diagramu na obrázku 3. Vstupní kritéria: 1. hodnocené léčivo (EPL/silymarin, resp. extrakt z ostropestřce mariánského), 2. klinické hodnocení efektu u pacientů se steatotickým onemocněním jater (nealkoholovým – MASLD/NAFLD/NASH/MASH). Vylučovací kritéria: 1. preklinické studie, 2. nebylo možno hodnotit efekt samotného léčiva (kombinace, nejasná dávka), 3. nebylo možno identifikovat cílovou podskupinu pacientů v rámci hodnoceného souboru, 4. review, systematický/narativní přehled. Nalezené studie jsou pro obě látky níže prezentovány v tabulkách a komentovány dle EBM [35].
Esenciální fosfolipidy
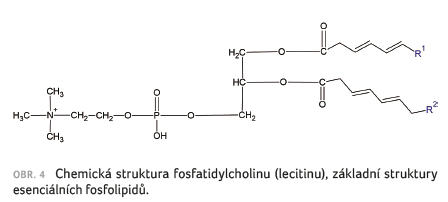 Esenciální fosfolipidy jsou přírodní látky získané ze sójových bobů, jde o diglyceridové estery kyseliny cholinfosforečné s vysokým podílem nenasycených mastných kyselin, jako jsou kyselina linolová, linolenová a olejová [36], obr. 4. Mají podobnou strukturu jako endogenní fosfolipidy, ale s vyšším obsahem nenasycených mastných kyselin. Registrované léčivé přípravky s obsahem EPL mají schválené indikace k podpoře léčby toxicko‑metabolického poškození jater a hepatitid, přičemž zmírňují příznaky, jako je ztráta chuti k jídlu nebo tlak v pravém podžebří u dospělých a mladistvých starších 12 let [37]. Nežádoucí účinky jsou relativně vzácné a zahrnují alergické reakce, průjem, závratě nebo palpitace. Více než 90 % účinné látky je absorbováno v tenkém střevě a následně distribuováno do jater, kde se začleňuje do buněčných membrán hepatocytů, čímž má podporovat regeneraci jaterní tkáně a zlepšovat metabolismus lipidů blíže neurčeným mechanismem. Přípravek může interagovat s antikoagulancii a jeho užívání během těhotenství a kojení se nedoporučuje kvůli nedostatku údajů o bezpečnosti. Souhrn údajů o přípravku (SPC) uvádí, že nemůže zabránit poškození jater způsobenému alkoholem nebo léky a měl by být používán pouze jako doplňková léčba v rámci komplexního léčebného přístupu. Terapie je opodstatněná pouze tehdy, pokud je při léčbě pozorováno zlepšení subjektivních známek stavu [36]. O to více zarážejí některé webové reklamní kampaně, které lze přinejmenším v některých případech považovat za eticky sporné. Kupříkladu osvětová kampaň „Suchej únor“ proložená reklamou na hepatoprotektivní léčivo, jehož SPC ovšem výslovně uvádí, že nemůže zabránit poškození jater v důsledku užívání škodlivých látek (např. alkoholu), může být nepoučeným laikem pochopena zcela opačně.
Esenciální fosfolipidy jsou přírodní látky získané ze sójových bobů, jde o diglyceridové estery kyseliny cholinfosforečné s vysokým podílem nenasycených mastných kyselin, jako jsou kyselina linolová, linolenová a olejová [36], obr. 4. Mají podobnou strukturu jako endogenní fosfolipidy, ale s vyšším obsahem nenasycených mastných kyselin. Registrované léčivé přípravky s obsahem EPL mají schválené indikace k podpoře léčby toxicko‑metabolického poškození jater a hepatitid, přičemž zmírňují příznaky, jako je ztráta chuti k jídlu nebo tlak v pravém podžebří u dospělých a mladistvých starších 12 let [37]. Nežádoucí účinky jsou relativně vzácné a zahrnují alergické reakce, průjem, závratě nebo palpitace. Více než 90 % účinné látky je absorbováno v tenkém střevě a následně distribuováno do jater, kde se začleňuje do buněčných membrán hepatocytů, čímž má podporovat regeneraci jaterní tkáně a zlepšovat metabolismus lipidů blíže neurčeným mechanismem. Přípravek může interagovat s antikoagulancii a jeho užívání během těhotenství a kojení se nedoporučuje kvůli nedostatku údajů o bezpečnosti. Souhrn údajů o přípravku (SPC) uvádí, že nemůže zabránit poškození jater způsobenému alkoholem nebo léky a měl by být používán pouze jako doplňková léčba v rámci komplexního léčebného přístupu. Terapie je opodstatněná pouze tehdy, pokud je při léčbě pozorováno zlepšení subjektivních známek stavu [36]. O to více zarážejí některé webové reklamní kampaně, které lze přinejmenším v některých případech považovat za eticky sporné. Kupříkladu osvětová kampaň „Suchej únor“ proložená reklamou na hepatoprotektivní léčivo, jehož SPC ovšem výslovně uvádí, že nemůže zabránit poškození jater v důsledku užívání škodlivých látek (např. alkoholu), může být nepoučeným laikem pochopena zcela opačně.
 V rámci systematického vyhledávání bylo nalezeno pouze šest publikací, ve kterých byl sledován klinický efekt EPL u populace se steatotickým onemocněním jater. Čtyři z těchto šesti studií publikoval stejný nebo velmi podobný autorský kolektiv, přičemž u tří studií se jednalo o identický kolektiv a o tutéž studii. Přehled studií uvádí tabulka 1; komentáře k jednotlivým studiím jsou uvedeny níže. Otevřená, nekontrolovaná studie Dajaniho a kol. [38] sledovala účinky EPL u pacientů s MASLD a T2DM, dyslipidemií nebo s prostým MASLD (dříve NAFLD). Studie sice uváděla signifikantní pokles aktivity ALT a AST a pravděpodobně nesignifikantní posuny (autoři uvádějí pouze graficky, statisticky nehodnotili) v rámci kategorií jaterní steatózy hodnocené ultrasonograficky, ale byla omezena malým vzorkem hodnocených osob a relativně krátkým trváním. Elastografie navíc neprokázala významné změny ani po 72 týdnech terapie. Otevřené uspořádání a absence kontrolní skupiny představují další podstatnou limitaci [38].
V rámci systematického vyhledávání bylo nalezeno pouze šest publikací, ve kterých byl sledován klinický efekt EPL u populace se steatotickým onemocněním jater. Čtyři z těchto šesti studií publikoval stejný nebo velmi podobný autorský kolektiv, přičemž u tří studií se jednalo o identický kolektiv a o tutéž studii. Přehled studií uvádí tabulka 1; komentáře k jednotlivým studiím jsou uvedeny níže. Otevřená, nekontrolovaná studie Dajaniho a kol. [38] sledovala účinky EPL u pacientů s MASLD a T2DM, dyslipidemií nebo s prostým MASLD (dříve NAFLD). Studie sice uváděla signifikantní pokles aktivity ALT a AST a pravděpodobně nesignifikantní posuny (autoři uvádějí pouze graficky, statisticky nehodnotili) v rámci kategorií jaterní steatózy hodnocené ultrasonograficky, ale byla omezena malým vzorkem hodnocených osob a relativně krátkým trváním. Elastografie navíc neprokázala významné změny ani po 72 týdnech terapie. Otevřené uspořádání a absence kontrolní skupiny představují další podstatnou limitaci [38].
Otevřená, nekontrolovaná studie Ivashkina a kol. [39] sledovala bezpečnost, pacientem hodnocenou symptomatologii a adherenci k léčbě novou formou pasty obsahující EPL u pacientů s NAFLD (n = 106) a virovou hepatitidou B nebo C (n = 41). Pacienti byli léčeni po dobu 12 týdnů (600 mg EPL třikrát denně). Autoři uvádějí signifikantní zlepšení celkových symptomatických skóre (Global Overall Symptom scale a Gastrointestinal Symptom score) ve srovnání s výchozím stavem, přičemž adherence k léčbě dosahovala 99 %. I tato studie má zásadní limitace: otevřené uspořádání, absence kontrolní skupiny. Dále chybějí objektivní parametry hodnocení jaterního postižení, jako jsou histologická data nebo pokročilé zobrazovací metody (např. elastografie), což snižuje výpovědní hodnotu ohledně vlivu EPL na jaterní strukturu. Krátká doba sledování (12 týdnů) je dalším limitem; změny ve fibróze a dlouhodobém jaterním zdraví vyžadují delší hodnocení.
Otevřená, randomizovaná studie Tana a kol. [40] hodnotila účinek EPL u 15 čínských pacientů s biopsií potvrzenou NASH. Pacienti byli randomizováni k užívání EPL (1 800 mg/den) po dobu šesti měsíců (10 subjektů) v kombinaci s dietními a pohybovými doporučeními, nebo pouze k dietním a pohybovým doporučením (5 subjektů). Studie neprokázala žádné signifikantní rozdíly mezi skupinami v parametrech, jako jsou BMI, obvod pasu, aktivita jaterních enzymů, výsledky elastografického vyšetření, ani histologické skóre NAS (non‑alcoholic fatty liver disease activity score) na konci sledování. U pacientů léčených EPL došlo k nevýznamnému poklesu aktivity ALT a AST a k mírným změnám v histologii, nicméně výsledky nebyly statisticky významné. Hlavní limitací studie je malý vzorek pacientů, krátká doba sledování. Autoři sami uzavírají, že přínosy EPL pozorované u alkoholového poškození jater se v této populaci s časným stadiem NASH nepotvrdily [40].
Observační ruská studie Maeva a kol. [41] hodnotila účinek polyenylfosfatidylcholinu (PPC) jako adjuvantní terapie u 2 843 ruských pacientů s nově diagnostikovaným NAFLD a přidruženými metabolickými komorbiditami (nadváha/obezita, hypertenze, T2DM, hypercholesterolemie). Autoři studii publikovali hned ve třech článcích, z nichž se každý věnuje jiným cílovým ukazatelům. Pacienti byli léčeni PPC (1,8 g/den) podávaným po dobu 24 týdnů jako doplněk standardní péče. Výsledky ukázaly statisticky významné snížení aktivit jaterních enzymů (ALT, AST, GGT) po 24 týdnech léčby ve všech podskupinách pacientů s různým počtem komorbidit (p < 0,001). Stejní autoři prezentovali data ze stejné studie v dalším článku [42], tentokrát prezentovali zlepšení ultrasonografických nálezů. Do třetice autoři sledovali adherenci a nežádoucí účinky a uzavírají, že adherence a spokojenost s léčbou byly dobré a nežádoucí účinky mírné [43]. Hlavní limitací studie je její observační uspořádání bez kontrolní skupiny, což znemožňuje stanovit kauzální vztah mezi PPC a zlepšením jaterních funkcí. Navíc autoři hodnotili PPC, který může být součástí EPL, avšak procentuální zastoupení v přípravcích dostupných v ČR je neznámé. Dále chybí hodnocení histologických změn nebo neinvazivních markerů fibrózy. Výsledky je proto třeba interpretovat s opatrností a potvrdit je RCT.
Od roku 2022 probíhá mezinárodní multicentrická dvojitě zaslepená, randomizovaná, placebem kontrolovaná studie fáze IV s plánovanými 190 pacienty s MASLD a přidruženým T2DM, hyperlipidemií nebo obezitou. Studie má dvě ramena: skupina s EPL (1 800 mg/den) + standardní léčba a skupina s placebem + standardní léčba. Hlavním cílem je zhodnotit účinnost EPL na jaterní steatózu pomocí elastografie během šesti měsíců, sekundární cíle zahrnují změnu kvality života (QoL) a hodnocení symptomů (astenie, deprese, bolest břicha, únava) [44]. Vedle toho byl publikován protokol pro Cochrane review, které by mělo skutečně poskytnout validní odpověď na otázku ohledně účinnosti EPL v terapii MASLD [45].
Silymarin
 Silymarin se získává extrakcí z plodů ostropestřce mariánského (Silybum marianum). Jedná se o směs flavolignanů (obr. 5) a detailní složení závisí na způsobu extrakce, přičemž se může zásadně lišit. Vliv změn složení na účinnost a bezpečnost přitom není dostatečně prozkoumán [46]. Další otázkou bezpečnosti je případný obsah mykotoxinů, které se v rostlinných doplňcích stravy mohou vyskytovat a v důsledku spíše zdraví poškozovat [47]. Nejinak je tomu bohužel i u doplňků stravy se semínky ostropestřce mariánského nebo s jeho extrakty, kde byly mykotoxiny opakovaně nalezeny [48–50].
Silymarin se získává extrakcí z plodů ostropestřce mariánského (Silybum marianum). Jedná se o směs flavolignanů (obr. 5) a detailní složení závisí na způsobu extrakce, přičemž se může zásadně lišit. Vliv změn složení na účinnost a bezpečnost přitom není dostatečně prozkoumán [46]. Další otázkou bezpečnosti je případný obsah mykotoxinů, které se v rostlinných doplňcích stravy mohou vyskytovat a v důsledku spíše zdraví poškozovat [47]. Nejinak je tomu bohužel i u doplňků stravy se semínky ostropestřce mariánského nebo s jeho extrakty, kde byly mykotoxiny opakovaně nalezeny [48–50].
Dle SPC přípravků se silymarinem [37] je hepatoprotektivní účinek silymarinu zprostředkován blíže nespecifikovanou stabilizací buněčných membrán hepatocytů (doslova „zpevňuje strukturu buněčné membrány hepatocytu“), podporou regenerace jaterních buněk, inhibicí lipidové peroxidace a antioxidační aktivitou. Dále pak silymarin stimuluje aktivitu (patrně ribozomální) polymerázy A v jádru, a tím následně zvýšenou syntézu ribozomálních bílkovin, což má také přispívat ke zvýšené regenerační schopnosti jater. Silymarin, resp. suchý extrakt z ostropestřce mariánského, se používá k léčbě toxických poškození jater a jako podpůrná terapie při chronických zánětlivých onemocněních jater a jaterní cirhóze. Mezi nežádoucí účinky patří mírný projímavý účinek nebo kožní vyrážky. V případě předávkování může dojít k zesílení projímavého účinku. Samotná SPC přípravků se silymarinem, resp. extrakty ostropestřce mariánského jsou v porovnání s nově registrovanými přípravky až neuvěřitelně stručná (některá jen 5 stran), což ilustruje současnou (ne)znalost molekulárních mechanismů působení a evidenci účinků těchto látek.
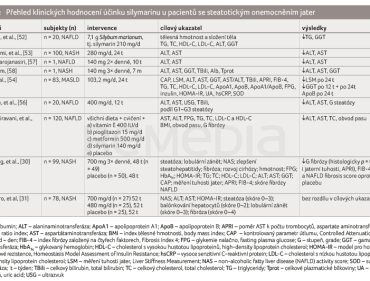 V rámci systematického vyhledávání bylo nalezeno pouze devět publikací, ve kterých byl sledován klinický efekt silymarinu u populace se steatotickým onemocněním jater. Ve dvou případech se jednalo o kazuistiky o jednom pacientovi. V rámci vyhledávání byl nalezen obrovský podíl přehledových článků (více než čtvrtina celkového počtu nalezených publikací). Přehled studií představuje tabulka 2; komentáře k jednotlivým studiím jsou uvedeny níže.
V rámci systematického vyhledávání bylo nalezeno pouze devět publikací, ve kterých byl sledován klinický efekt silymarinu u populace se steatotickým onemocněním jater. Ve dvou případech se jednalo o kazuistiky o jednom pacientovi. V rámci vyhledávání byl nalezen obrovský podíl přehledových článků (více než čtvrtina celkového počtu nalezených publikací). Přehled studií představuje tabulka 2; komentáře k jednotlivým studiím jsou uvedeny níže.
Otevřená intervenční studie (Kolota, et al., [52]) sledovala účinek tříměsíčního podávání ostropestřce mariánského (7,1 g denně jako zdroj 210 mg silymarinu) v kombinaci s dietními a pohybovými doporučeními u 20 pacientů s NAFLD. Navzdory absenci změn v dietním režimu a fyzické aktivitě pacientů během sledovaného období došlo k signifikantnímu poklesu sérových koncentrací triglyceridů (p = 0,0017) a aktivity GGT (p = 0,0008). Tato zjištění naznačují možný příznivý efekt silymarinu nezávisle na změnách životního stylu. Hlavními limitacemi studie však byly malý vzorek pacientů, absence kontrolní skupiny a neschopnost zajistit dodržování intervenčních doporučení a jejich kontrolu.
Randomizovaná, placebem kontrolovaná studie autorů Hashemi a kol. [53] hodnotila účinnost silymarinu (280 mg denně) u 100 pacientů s NASH během 24 týdnů. Silymarin vedl k signifikantnímu snížení aktivity ALT (p = 0,001) a k vyšší míře normalizace ALT (p = 0,001) i AST (62 % vs. 20 %, p = 0,0001) ve srovnání s placebem. Studie byla omezena krátkým trváním a zaměřením pouze na biochemické parametry bez hodnocení histologických změn. Absence závažných nežádoucích účinků podporuje dobrou toleranci silymarinu. Sami autoři uzavírají, že pro potvrzení jeho účinnosti je třeba dalších studií s delším sledováním a histologickým hodnocením.
Terminologický přehled:
NAFLD (non‑alcoholic fatty liver disease): Starší termín pro „nealkoholické ztukovatění jater“ (stav, kdy je v játrech nadměrně ukládán tuk bez známek zánětu). Termín NAFLD se postupně přestal používat, protože nová nomenklatura upřednostňuje označení, která lépe reflektují různé aspekty onemocnění jater.
NASH (non‑alcoholic steatohepatitis): Chronický zánět jater spojený s nealkoholickým ztukovatěním, který může vést k fibróze a progreduje k dalším stadiím onemocnění. Tento termín je stále používán, zejména pro označení specifického stadia onemocnění jater s přítomností zánětu.
MASH (metabolic associated steatohepatitis): Aktualizovaný termín pro NASH, který zdůrazňuje spojení s metabolickým syndromem.
MASLD (metabolic dysfunction‑associated steatotic liver disease): Nový a aktuální termín, který nahrazuje dřívější označení NAFLD. MASLD lépe popisuje spektrum jaterních onemocnění spojených s metabolickou dysfunkcí a zahrnuje jak mírné ztukovatění jater, tak i závažnější stadia se zánětem.
HCC (hepatocellular carcinoma): Hepatocelulární karcinom, může vzniknout jako komplikace dlouhodobého zánětu a fibrózy jater, obzvláště u pacientů s MASH/MASLD. HCC je často konečnou fází jaterního onemocnění a jedním z nejvážnějších důsledků nealkoholických onemocnění jater.
Randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie (Jin, et al.) [54] hodnotila účinky silymarinu (103,2 mg/den) podávaného po dobu 24 týdnů u 83 pacientů s MASLD. Suplementace silymarinu vedla k signifikantnímu snížení jaterní tuhosti (p = 0,015), aktivity GGT (p = 0,042) a hodnoty apolipoproteinu B (p = 0,023), avšak bez významného vlivu na steatózu (CAP – kontrolovaný parametr útlumu, controlled attenuation parameter), aminotransferázy, glykemické a lipidové parametry, zánětlivé markery i na skóre APRI a FIB‑4. Analýza střevního mikrobiomu ukázala zvýšení druhové diverzity a obohacení rodu Oscillospiraceae u skupiny se silymarinem [54]. Hlavními limitacemi jsou malý vzorek a krátké trvání studie, přičemž výsledky vyžadují potvrzení v rozsáhlejších klinických hodnoceních.
Další randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie autorů Anushiravani a kol. [55] hodnotila účinnost silymarinu (140 mg/den), metforminu, pioglitazonu a vitaminu E u 150 pacientů s NAFLD během tří měsíců. Ve skupinách s metforminem, pioglitazonem a silymarinem došlo k významnému poklesu aktivity ALT a AST, u silymarinu pak i ke snížení obvodu pasu [55].
Randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie autorů Kheong a kol. [30] hodnotila účinnost silymarinu (ve vysoké dávce 700 mg 3× denně) po dobu 48 týdnů u 99 pacientů s histologicky potvrzeným NASH. Primární cíl, tedy snížení NAFLD activity score (NAS) o ≥ 30 %, nebyl mezi skupinami signifikantně odlišný (32,7 % vs. 26,0 %, p = 0,467). Naopak bylo zaznamenáno signifikantní zmírnění fibrózy ve skupině se silymarinem, a to jak histologicky (p = 0,023), tak pomocí měření jaterní tuhosti (p = 0,002). Rovněž došlo k poklesu indexů APRI (p = 0,011), FIB‑4 (p = 0,041) a NAFLD fibrosis score (p < 0,001) ve skupině se silymarinem. Studie byla limitována relativně malým vzorkem pacientů a absencí signifikantního efektu na NAS.
Randomizovaná, dvojitě zaslepená, placebem kontrolovaná multicentrická studie fáze II autorů Navarro a kol. [31] hodnotila bezpečnost a účinnost vysokých dávek silymarinu 420 mg a 700 mg 3× denně u 78 pacientů s NASH bez cirhózy. Primárního cíle, tedy zlepšení NAS o ≥ 2 body, bylo dosaženo u 15 % pacientů ve skupině silymarinu 700 mg, u 19 % pacientů ve skupině 420 mg a u 12 % pacientů ve skupině s placebem, rozdíly nebyly statisticky významné (p = 0,79). Zajímavé je, že největší zmírnění fibrózy bylo pozorováno ve skupině s placebem, i když bez statistické významnosti u pacientů s NASH bez cirhózy. Přestože byla studie metodologicky robustní, výsledky neprokázaly signifikantní zlepšení NAS oproti placebu (p = 0,79) [31].
Studie případů a kontrol (Shaikh, et al., [56]) hodnotila účinnost silymarinu (200 mg 2× denně po dobu 12 týdnů) u 200 pacientů s NAFLD. Silymarin významně snížil aktivitu ALT a AST oproti placebu (p = 0,0001). Studie však měla několik limitací: krátké trvání (12 týdnů), které neumožňuje posoudit dlouhodobý efekt; absence hodnocení histologických změn v játrech; malý počet pacientů s pokročilou steatózou (grade 3) [56].
Byla publikována také dvě kazuistická sdělení se zaměřením na silymarin a steatotické onemocnění jater. Kazuistiky popisují případy dvou pacientů s NAFLD/NASH a nadváhou/obezitou, u nichž podávání silymarinu (140 mg 2× denně/3× denně) vedlo ke snížení aktivity jaterních enzymů (ALT, AST, GGT) po 6 a 10 týdnech a 4 a 7 měsících bez zaznamenaných nežádoucích účinků [57, 58].
Solidně provedená metaanalýza [60] z roku 2017 věnující se silymarinu a jeho účinku u MASLD identifikovala 10 904 publikací, z nichž bylo do systematického přehledu zařazeno 17 studií a do metaanalýzy 6 studií podle stanovených kritérií. Výsledky ukázaly statisticky významné snížení aktivity ALT o 0,26 IU/ml (95% interval spolehlivosti [CI] –0,46 až –0,07; p = 0,007) a AST o 0,53 IU/ml (95% CI –0,74 až –0,32; p = 0,000) vlivem užívání silymarinu, avšak bez klinického významu. Aktivita GGT se významně nezměnila. Analýza podskupin (silymarin samostatně vs. v kombinaci s dalšími látkami, délka intervence ≥ 6 měsíců vs. < 6 měsíců) neprokázala významné rozdíly. Hodnocené studie vykazovaly vysokou heterogenitu a nízkou metodologickou kvalitu. Silymarin tedy minimálně snižoval aktivitu ALT a AST, ale bez klinického významu [59].
Závěr
V kontextu výše uvedeného lze shrnout, že současná evidence pro doporučení EPL a silymarinu v terapii MASLD je slabá a je charakterizována nedostatkem kvalitních klinických studií a metodologickými slabinami. Mezi tyto slabiny patří zejména absence kontrolních skupin, absence zaslepení, hodnocení pouze laboratorních parametrů, krátká doba sledování, nedostatečně kontrolované vnější vlivy (především komedikace) a v některých případech i nehomogenní studijní populace. Celkově tedy současná evidence o účinnosti EPL a silymarinu trpí nedostatkem přesvědčivých důkazů pro jejich rutinní klinické využití. To se nakonec odráží i v aktuálních klinických doporučeních [6], kde nejsou tradiční hepatoprotektiva v terapii MASLD doporučována. Jak již bylo uvedeno, v tomto článku nebyly zvláště hodnoceny dříve publikované přehledy, nicméně i tyto zpravidla uvádějí, že přestože testované látky (jak EPL, tak i silymarin) ukazují potenciální přínosy, především směrem k laboratorním ukazatelům MASLD, pro doporučení jejich rutinního využití v terapii MASLD alespoň prozatím nemáme dostatečnou úroveň evidence jejich účinnosti. Situace se silymarinem je obdobná. Rozdíl oproti EPL je v tom, že relevantní klinická doporučení EASL, EASD a EASO k diagnostice a terapii MASLD z roku 2024 silymarin sice zmiňují, avšak na základě několika málo RCT uzavírají, že ač může zlepšit biochemické ukazatele MASLD, k potvrzení jeho krátkodobé a dlouhodobé účinnosti jsou nutné rozsáhlejší klinické studie a nové studie založené na důkazech [6]. Pro potvrzení nebo vyvrácení účinku těchto látek tedy musíme počkat na závěry dobře designovaných zaslepených kontrolovaných klinických studií s dostatečně dlouhou dobou sledování a klinicky validními cílovými ukazateli. Jedna taková studie v současné době dokonce probíhá (EudraCT, 2021–006069-39).
Práce vznikla za podpory specifického vysokoškolského výzkumu (MUNI/A/1722/2024), kterou poskytlo MŠMT.
Doc. PharmDr. Jan Juřica, Ph.D.
Farmakologický ústav
Kamenice 5, 625 00 Brno
e‑mail: jurica@med.muni.cz
Literatura
[1] Šmíd V, Dvořák K. Jaterní manifestace metabolického syndromu se nyní jmenuje MASLD – aktuální pohled na nejčastější onemocnění jater současnosti. Vnitřní lékařství 2024; 70: E8–E14.
[2] Chopra S, Lai M. Management of metabolic dysfunction‑associated steatotic liver disease (nonalcoholic fatty liver disease) in adults. UpToDate 2025; 1–58.
[3] Riazi K, Azhari H, Charette JH, et al. The prevalence and incidence of NAFLD worldwide: a systematic review and meta‑analysis. Lancet Gastroenterol Hepatol 2022; 7: 851–861.
[4] Mahase E. Obesity: No European country is on track to halt rising levels by 2025, WHO warns. BMJ 2022; 377: o1107.
[5] Hagström H, Adams LA, Allen AM, et al. The future of International Classification of Diseases coding in steatotic liver disease: An expert panel Delphi consensus statement. Hepatol Commun 2024; 8: doi:10.1097/HC9.0000000000000386.
[6] (EASL), E.A.f.t.S.o.t.L.; (EASD), E.A.f.t.S.o.D.; (EASO), E.A.f.t.S.o.O. EASL‑EASD‑EASO Clinical Practice Guidelines on the management of metabolic dysfunction‑associated steatotic liver disease (MASLD). J Hepatol 2024; 81: 492–542.
[7] Pei Y, GB‑B Goh. Genetic Risk Factors for Metabolic Dysfunction‑Associated Steatotic Liver Disease. Gut Liver 2025; 19: 8–18.
[8] Sheth SG, Chopra S. Clinical features and diagnosis of metabolic dysfunction‑associated steatotic liver disease (nonalcoholic fatty liver disease) in adults. UpToDate 2024.
[9] Šmíd V, Dvořák K. Doplnění Doporučeného postupu České hepatologické společnosti ČLS JEP pro diagnostiku a léčbu NAFLD: FIB‑4 index – interpretace získaného výsledku a doporučení dalšího postupu. 2024, 1–4.
[10] Sterling RK, Lissen E, Clumeck N, et al. Development of a simple noninvasive index to predict significant fibrosis in patients with HIV/HCV coinfection. Hepatology 2006; 43: 1317–1325.
[11] Albert SG, Wood EM. FIB‑4 as a screening and disease monitoring method in pre‑fibrotic stages of metabolic dysfunction‑associated fatty liver disease (MASLD). J Diabetes Complications 2024; 38: 108777.
[12] Golabi P, Paik JM, Kumar A, et al. Nonalcoholic fatty liver disease (NAFLD) and associated mortality in individuals with type 2 diabetes, pre‑diabetes, metabolically unhealthy, and metabolically healthy individuals in the United States. Metabolism 2023; 146: 155642.
[13] Fu CE, Ng CH, Yong JN, et al. A Meta‑analysis on Associated Risk of Mortality in Nonalcoholic Fatty Liver Disease. Endocr Pract 2023; 29: 33–39.
[14] Quek J, Ng CH, Tang ASP, et al. Metabolic Associated Fatty Liver Disease Increases the Risk of Systemic Complications and Mortality. A Meta‑Analysis and Systematic Review of 12 620 736 Individuals. Endocr Pract 2022; 28: 667–672.
[15] Xiao J, Ng CH, Chan KE, et al. Hepatic, Extra‑hepatic Outcomes and Causes of Mortality in NAFLD – An Umbrella Overview of Systematic Review of Meta‑Analysis. J Clin Exp Hepatol 2023; 13: 656–665.
[16] Kimura T, Tamaki N, Wakabayashi SI, et al. Colorectal cancer incidence in steatotic liver disease (MASLD, MetALD, and ALD). Clin Gastroenterol Hepatol 2025; doi:10.1016/j.cgh.2024.12.018.
[17] Koutoukidis DA, Koshiaris C, Henry JA, et al. The effect of the magnitude of weight loss on non‑alcoholic fatty liver disease: A systematic review and meta‑analysis. Metabolism 2021; 115: 154455.
[18] Hayat U, Siddiqui AA, Okut H, et al. The effect of coffee consumption on the non‑alcoholic fatty liver disease and liver fibrosis: A meta‑analysis of 11 epidemiological studies. Ann Hepatol 2021; 20: 100254.
[19] Chen YP, Lu FB, Hu YB, et al. A systematic review and a dose–response meta‑analysis of coffee dose and nonalcoholic fatty liver disease. Clin Nutr 2019; 38: 2552–2557.
[20] UpToDate. Resmetirom: Drug information. 2025. Online databáze; citováno 10. 2. 2025; URL:. https://www.uptodate.com/contents/resmetirom‑drug‑information?search=resmetirom&source=panel_search_result&selectedTitle=1%7E4&usage_type=panel&kp_tab=drug_general&display_rank=1
[21] Newsome PN, Ambery P. Incretins (GLP‑1 receptor agonists and dual/triple agonists) and the liver. J Hepatol 2023; 79: 1557–1565.
[22] Newsome PN, Buchholtz K, Cusi K, et al. A Placebo‑Controlled Trial of Subcutaneous Semaglutide in Nonalcoholic Steatohepatitis. N Engl J Med 2021; 384: 1113–1124.
[23] Scorletti E, Creasy KT, Vujkovic M, et al. Dietary Vitamin E Intake Is Associated With a Reduced Risk of Developing Digestive Diseases and Nonalcoholic Fatty Liver Disease. Am J Gastroenterol 2022; 117: 927–930.
[24] Sanyal AJ, Chalasani N, Kowdley KV, et al. Pioglitazone, vitamin E, or placebo for nonalcoholic steatohepatitis. N Engl J Med 2010; 362: 1675–1685.
[25] Simental‑Mendía M, Sánchez‑García A, Simental‑Mendía LE. Effect of ursodeoxycholic acid on liver markers: A systematic review and meta‑analysis of randomized placebo‑controlled clinical trials. Br J Clin Pharmacol 2020; 86: 1476–1488.
[26] Lindor KD, Kowdley KV, Heathcote EJ, et al. Ursodeoxycholic acid for treatment of nonalcoholic steatohepatitis: results of a randomized trial. Hepatology 2004; 39: 770–778.
[27] Ratziu V. Treatment of NASH with ursodeoxycholic acid: Pro. Clin Res Hepatol Gastroenterol 2012; 36: S41–S45.
[28] Ayada I, van Kleef LA, Zhang H, et al. Dissecting the multifaceted impact of statin use on fatty liver disease: a multidimensional study. EBioMedicine 2023; 87: 104392.
[29] Severo MD. Daily Aspirin Use Associated With Reduced Risk for Fibrosis Progression in Patients With Nonalcoholic Fatty Liver Disease. Clin Gastroenterol Hepatol 2020; 18: 523.
[30] Kheong CW, Mustapha NRN, Mahadeva S. A Randomized Trial of Silymarin for the Treatment of Nonalcoholic Steatohepatitis. Clin Gastroenterol Hepatol 2017; 15: 1940–1949.e1948.
[31] Navarro VJ, Belle SH, D’Amato M, et al. Silymarin in non‑cirrhotics with non‑alcoholic steatohepatitis: A randomized, double‑blind, placebo controlled trial. PLoS One 2019; 14: e0221683.
[32] Anderson JL, Platia EV, Hallstrom A, et al. Interaction of baseline characteristics with the hazard of encainide, flecainide, and moricizine therapy in patients with myocardial infarction. A possible explanation for increased mortality in the Cardiac Arrhythmia Suppression Trial (CAST). Circulation 1994; 90: 2843–2852.
[33] Echt DS, Liebson PR, Mitchell LB, et al. Mortality and morbidity in patients receiving encainide, flecainide, or placebo. The Cardiac Arrhythmia Suppression Trial. N Engl J Med 1991; 324: 781–788.
[34] Dajani AI, Popovic B. Essential phospholipids for nonalcoholic fatty liver disease associated with metabolic syndrome: A systematic review and network meta‑analysis. World J Clin Cases 2020; 8: 5235–5249.
[35] Durieux N, Vandenput S, Pasleau F. Médecine Factuelle: na hierarchiation des preuves par le Centre for evidence‑based medicine d´Oxford [OCEBM levels of evidence system]. Rev Med Liege 2013; 68: 644–649.
[36] SUKL. SmPC: Essentiale forte 600 mg tvrdé tobolky. 2025.
[37] InfoPharm. AISLP. 2022.
[38] Dajani A, Abu Hammour A, Zakaria M, et al. Essential phospholipids as a supportive adjunct in the management of patients with NAFLD. Arab J Gastroenterol 2015; 16: 99–104.
[39] Ivashkin V, Maev I, Pavlov C, et al. Safety and Effectiveness of Essential Phospholipids Paste in Patients with Non‑alcoholic Fatty Liver Disease or Viral Hepatitis. Turk J Gastroenterol 2021; 32: 750–757.
[40] Tan H, Low A, Lim K, et al. A randomized, unblinded pilot trial of essential phospholipids in Chinese subjects with non‑alcoholic fatty liver disease (NASH). J Gastroenterol Hepatol 2011; 26: 162–162.
[41] Maev IV, Samsonov AA, Palgova LK, et al. Effectiveness of phosphatidylcholine as adjunctive therapy in improving liver function tests in patients with non‑alcoholic fatty liver disease and metabolic comorbidities: real‑life observational study from Russia. BMJ Open Gastroenterol 2020; 7: e000368.
[42] Maev I, Samsonov A, Palgova L, et al. Effectiveness of phosphatidylcholine in alleviating steatosis in patients with non‑alcoholic fatty liver disease and cardiometabolic comorbidities (MANPOWER study). BMJ Open Gastroenterol 2020; 7: doi:10.1136/bmjgast‑2019‑000341.
[43] Maev IV, Samsonov AA, Palgova LK, et al. Real‑world comorbidities and treatment patterns among patients with non‑alcoholic fatty liver disease receiving phosphatidylcholine as adjunctive therapy in Russia. BMJ Open Gastroenterol 2019; 6: e000307.
[44] Stefan N, Hartleb M, Popovic B, Varona R. Effect of essential phospholipids on hepatic steatosis in metabolic dysfunction‑associated steatotic liver disease associated with type 2 diabetes mellitus and/or hyperlipidemia and/or obesity: study protocol of a randomized, double‑blind, phase IV clinical trial. Trials 2024; 25: doi:10.1186/s13063‑024‑08208‑4.
[45] Varganova DL, Pavlov CS, Casazza G, et al. Essential phospholipids for people with non‐alcoholic fatty liver disease. The Cochrane Database of Systematic Reviews 2019; 2019.
[46] Chambers CS, Holečková V, Petrásková L, et al. The silymarin composition… and why does it matter??? Food Res Int 2017; 100: 339–353.
[47] Pleadin J, Frece J, Markov K. Mycotoxins in food and feed. Adv Food Nutr Res 2019; 89: 297–345.
[48] Bosko R, Pernica M, Beláková S, et al. Determination of T‑2 and HT‑2 Toxins in Seed of Milk Thistle [Silybum marianum (L.) Gaertn.] Using Immunoaffinity Column by UPLC‑MS/MS. Toxins 2022; 14: doi:10.3390/toxins14040258.
[49] Boško R, Pluháčková H, Martiník J, et al. Occurrence of mycotoxins in milk thistle: to be included in legislation or not? Mycotoxin Res 2024; 41: 199–206.
[50] Pickova D, Ostry V, Toman J, Malir F. Presence of Mycotoxins in Milk Thistle (Toxins (Basel) 2020; 12: doi:10.3390/toxins12120782.
[51] Anthony K, Subramanya G, Uprichard S, et al. Antioxidant and Anti‑Hepatitis C Viral Activities of Commercial Milk Thistle Food Supplements. Antioxidants (Basel) 2013; 2: 23–36.
[52] Kołota A, Głąbska D. Dietary intake of milk thistle seeds as a source of silymarin and its influence on the lipid parameters in nonalcoholic fatty liver disease patients. Applied Sciences 2021; 11: 5836.
[53] Hashemi SJ, Hajiani E, Heydari SE. A placebo‑controlled trial of silymarin in patients with nonalcoholic fatty liver disease. Hepatitis Monthly 2009; 9: 265–270.
[54] Jin Y, Wang X, Chen K, et al. Silymarin decreases liver stiffness associated with gut microbiota in patients with metabolic dysfunction‑associated steatotic liver disease: a randomized, double‑blind, placebo‑controlled trial. Lipids Health Dis 2024; 23: 239.
[55] Anushiravani A, Haddadi N, Pourfarmanbar M, Mohammadkarimi V. Treatment options for nonalcoholic fatty liver disease: a double‑blinded randomized placebo‑controlled trial. Eur J Gastroenterol Hepatol 2019; 31: 613–617.
[56] Shaikh KR, Shaikh S, Ata MA, et al. Therapeutic efficacy of Silymarin on liver aminotransferases in patients with nonalcoholic fatty liver disease. RMJ 2021; 46: 761–761.
[57] Chantarojanasiri T. Silymarin treatment and reduction of liver enzyme levels in non‑alcoholic fatty liver disease: a case report. Drugs Context 2023; 12: 2023‑1‑4.
[58] Hashem A. Silymarin and management of liver function in non‑alcoholic steatohepatitis: a case report. Drugs Context 2023; 12: 2023‑2‑9.
[59] de Avelar CR, Pereira EM, de Farias Costa PR, et al. Effect of silymarin on biochemical indicators in patients with liver disease: Systematic review with meta‑analysis. World J Gastroenterol 2017; 23: 5004–5017.