Alergie na včelí a vosí jed
Souhrn:
Vachová M. Alergie na včelí a vosí jed. Remedia 2020; 30: 68–71.
Alergie na včelí a vosí jed je u dospělých Evropanů jednou z nejčastějších příčin anafylaxe. Pro léčbu pacientů s diagnostikovanou alergií na hmyzí jed je určena vysoce efektivní specifická imunoterapie včelím/vosím jedem, která velmi výrazně snižuje riziko opakování alergické reakce po dalším bodnutí tímto hmyzem. Tato léčba je jednoznačně indikována dětem a dospělým, kteří po bodnutí prodělali těžkou či středně těžkou systémovou alergickou reakci. Navíc je určena i dospělým, kteří po bodnutí prodělali pouze generalizovanou kožní alergickou systémovou reakci, a to v případě vysokého rizika reexpozice hmyzímu bodnutí a/nebo narušení kvality života.
Summary:
Vachova M. Hymenoptera venom allergy. Remedia 2020; 30: 68–71.
Hymenoptera venom allergy (HVA) is one of the most common causes of anaphylaxis in European adults. Highly effective bee/wasp venom immunotherapy (VIT) is available for the treatment of patients diagnosed with HVA. VIT significantly reduces the risk of another allergic sting reaction. VIT is indicated in children and adults with clinical history of moderate to severe systemic allergic sting reaction. Moreover, VIT is recommended also in adults with history of only generalized skin systemic allergic sting reaction, if risk of re‑exposition is high or quality of life is impaired.
Key words: Hymenoptera venom allergy – anaphylaxis – venom immunotherapy.
Úvod
Bodnutí hmyzem je velmi běžné,
alespoň jedenkrát za život se s ním setká až 94,5 %
populace [1]. Normální reakcí po bodnutí hmyzem je lokální
otok, bolestivost, svědění a zčervenání v okolí
místa vpichu odeznívající zpravidla do několika hodin.
Alergie na hmyzí jed se nejčastěji projevuje jako tzv. velká
lokální reakce po bodnutí, při které otok v okolí
místa vpichu přesahuje 10 cm v průměru a trvá déle
než 24 hodin. K těmto mnohdy pacienta velmi obtěžujícím
reakcím dochází u 2,4–26,4 % populace [2]. Méně častým,
avšak klinicky závažnějším projevem alergie na hmyzí jed
jsou tzv. systémové reakce (SR) po bodnutí, které kolísají
od lehčích SR manifestovaných generalizovanými kožními
projevy až po závažné život ohrožující SR charakteru
anafylaktického šoku s poruchou vědomí, zástavou srdce
a apnoí (tab. 1).
Systémové reakce jsou naštěstí méně časté než velké
lokální reakce, postihují 0,3–7,5 % dospělých a 3,4 %
dětí [3]. Nejčastějšími původci uvedených alergických reakcí
po bodnutí jsou v našich geografických podmínkách
včely, vosy, případně sršně. Závažnější alergické reakce
po bodnutí jinými druhy blanokřídlého hmyzu jsou v našich
končinách vzácné.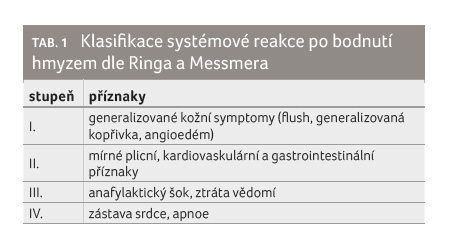
Diagnostika
Diagnostika alergie na hmyzí jed
vychází z doporučení Evropské akademie pro alergologii
a klinickou imunologii (EAACI) [4]. Na základě tohoto
doporučení je k provedení diagnostických testů jednoznačně
indikován pouze pacient s anamnézou proběhlé systémové
reakce po bodnutí hmyzem. Prvním diagnostickým krokem je
provedení kožních testů s extrakty včelího a vosího
jedu a/nebo stanovení specifických IgE protilátek k extraktům
těchto jedů. V klinické praxi se obvykle tato vyšetření
provádějí současně, což výrazně zvyšuje jejich senzitivitu.
Pro pacienty, kterým je prokázána „single“ pozitivita na včelí
nebo vosí jed, jsou tato vyšetření plně dostačující. Pro
nemocné s „double“ pozitivitou výsledků (včela i vosa)
těchto rutinních vyšetření jsou pro upřesnění diagnózy
určeny ještě další laboratorní metody, a to molekulární
diagnostika a test aktivace bazofilů [5]. Molekulární
diagnostika je založena na stanovení specifických IgE
protilátek cílených přímo k jednotlivým alergenovým
složkám obsaženým v extraktech včelího a vosího
jedu. V současné době můžeme stanovit IgE protilátky
ke dvěma hlavním složkám vosího jedu (Ves v 1 a Ves
v 5) a k pěti složkám včelího jedu (Api m 1,
Api m 2, Api m 3, Api m 5, Api m 10),
které jsou běžně komerčně dostupné (tab. 2).
Pokud jsou IgE protilátky k oběma dostupným vosím molekulám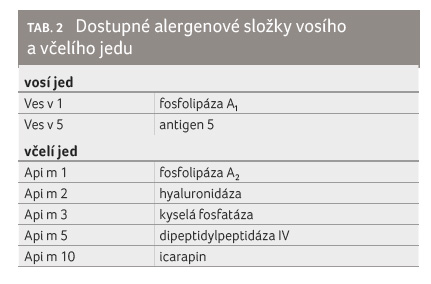 negativní, je alergie na vosí jed nepravděpodobná [6,7].
V případě negativity IgE protilátek ke všem pěti
dostupným alergenovým složkám včelího jedu však alergii
na tento jed s jistotou vyloučit nelze. Je to dáno tím,
že bohužel ne všechny relevantní molekuly obsažené ve včelím
jedu jsou dostupné a senzitivita stávajícího panelu není
optimální [8,9]. Další přínosnou metodou k upřesnění
diagnózy v nejednoznačných případech je test aktivace
bazofilů (BAT). Ten, podobně jako molekulární diagnostika, pomáhá
rozlišit mezi alergií na včelí a vosí jed v případě
„double“ pozitivity standardních, rutinně prováděných testů
uvedených výše [10]. Navíc by tento test měl být nepochybně
doplněn i u pacientů s přesvědčivou anamnézou
systémové reakce po bodnutí a s negativitou
ostatních testů [5,11]. Vyšetření alergie na hmyzí jed
spadá plně do kompetence alergologa a lze konstatovat, že
při použití všech uvedených metod se alergie na včelí
a/nebo vosí jed daří v naprosté většině případů
správně diagnostikovat.
negativní, je alergie na vosí jed nepravděpodobná [6,7].
V případě negativity IgE protilátek ke všem pěti
dostupným alergenovým složkám včelího jedu však alergii
na tento jed s jistotou vyloučit nelze. Je to dáno tím,
že bohužel ne všechny relevantní molekuly obsažené ve včelím
jedu jsou dostupné a senzitivita stávajícího panelu není
optimální [8,9]. Další přínosnou metodou k upřesnění
diagnózy v nejednoznačných případech je test aktivace
bazofilů (BAT). Ten, podobně jako molekulární diagnostika, pomáhá
rozlišit mezi alergií na včelí a vosí jed v případě
„double“ pozitivity standardních, rutinně prováděných testů
uvedených výše [10]. Navíc by tento test měl být nepochybně
doplněn i u pacientů s přesvědčivou anamnézou
systémové reakce po bodnutí a s negativitou
ostatních testů [5,11]. Vyšetření alergie na hmyzí jed
spadá plně do kompetence alergologa a lze konstatovat, že
při použití všech uvedených metod se alergie na včelí
a/nebo vosí jed daří v naprosté většině případů
správně diagnostikovat.
Léčba
Léčba pacienta s prokázanou
alergií na hmyzí jed manifestovanou předchozí SR zahrnuje
jeho edukaci, vybavení pohotovostní protialergickou medikací pro
případ recidivy SR po dalším bodnutí hmyzem a v neposlední
řadě také léčbu specifickou imunoterapií hmyzím jedem (VIT,
venom immunotherapy). Předně musí být nemocný poučen
o opatřeních, která snižují riziko bodnutí hmyzem (tab. 3). Další důležitou součástí edukace je seznámení
s použitím pohotovostních léků, včetně praktického
nácviku aplikace adrenalinu pomocí autoinjektoru s využitím
cvičného pera. Autoinjektor s adrenalinem je nepochybně
hlavním a nezbytným pohotovostním medikamentem, kromě něj
jsou pacienti navíc vybaveni i tabletami nesedativního
antihistaminika a kortikoidu [12].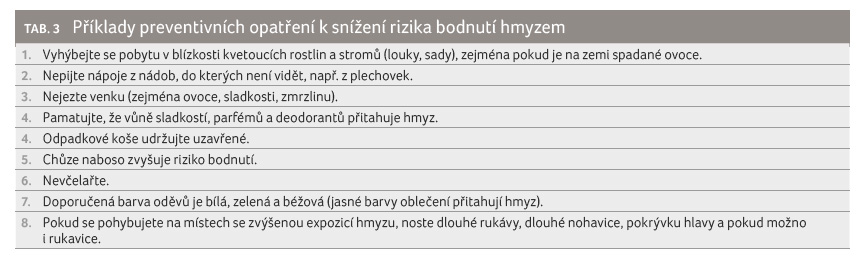
Profylaktickou léčbu, která jako jediná významně snižuje riziko opakování SR po dalším bodnutí hmyzem, představuje specifická imunoterapie hmyzím (včelím/vosím) jedem (VIT). Účinnost této léčby je velmi vysoká, dosahuje až 96 % u pacientů léčených specifickou imunoterapií vosím jedem a 84 % u nemocných léčených imunoterapií včelím jedem [13]. O indikaci rozhoduje pouze alergolog, a to na základě posouzení anamnézy a zhodnocení výsledků cíleného alergologického vyšetření. Specifická imunoterapie hmyzím jedem je jednoznačně indikována dětem a dospělým s anamnézou těžké či středně těžké systémové reakce (stupeň II–IV dle Ringa a Messmera) po bodnutí hmyzem. Navíc je určena i dospělým, kteří po bodnutí prodělali pouze generalizovanou kožní systémovou reakci (stupeň I dle Ringa a Messmera), a to v případě, hrozí li vysoké riziko reexpozice hmyzímu bodnutí a/nebo je kvalita života nemocného narušená.
Kromě anamnézy SR po bodnutí je nezbytnou podmínkou pro zahájení VIT jednoznačně potvrzená alergie k příslušnému hmyzímu jedu dostupnými diagnostickými metodami. Pokud se nám alergii na hmyzí jed nepodaří prokázat, pak imunoterapie není indikována bez ohledu na charakter reakce po bodnutí [13]. Absolutních kontraindikací k zahájení VIT je málo. Léčba se nezahajuje v těhotenství, u malých dětí (věk do 2–5 let), u pacientů s nekontrolovaným astmatem či s aktivním autoimunitním onemocněním. Další stavy (kardiovaskulární choroby, malignity, imunodeficience atd.) posuzuje alergolog individuálně u každého nemocného na základě platných mezinárodních doporučení [13,14]. Obecně platí, že pokud je přidružené onemocnění stabilizované, pak kontraindikaci k zahájení VIT nepředstavuje.
Zahájení a vedení VIT probíhá na pracovišti se zkušenostmi s vedením specifické imunoterapie, tedy v ambulanci alergologa. V České republice máme pro VIT k dispozici depotní přípravek obsahující standardizované extrakty včelího nebo vosího jedu určený k podkožnímu injekčnímu podání. Léčba má dvě fáze, úvodní a udržovací. V úvodní části terapie se injekce podávají jedenkrát týdně. Aplikace se zahajuje velmi nízkou dávkou alergenu, která se postupně navyšuje až do dosažení udržovací či maximální tolerované dávky. Standardně se v jednom sezení aplikuje jedna injekce, po které následuje 30minutová observace. Dle doporučení výrobce však lze aplikovat i 2–3 injekce v jeden den, opět v 30minutových intervalech. Při použití standardního schématu s navyšováním dávek po jedné injekci týdně dosáhneme udržovací dávky za zhruba 15 týdnů. Výhodou navyšování dávek po skupinách 2–3 injekcí v jednom sezení jedenkrát týdně je výrazné zkrácení iniciální fáze na pouhých šest týdnů. Po dosažení udržovací dávky alergenu se postupně prodlužuje interval mezi injekcemi až na 6–8 týdnů. V tomto rozmezí pak pacient dochází na injekce obvykle po dobu pěti let.
Naprostá většina pacientů podstupuje imunoterapii pouze jedním hmyzím jedem (včelím nebo vosím), v indikovaných případech však lze vést léčbu i oběma jedy. Případné obavy z VIT nejsou namístě. Bylo potvrzeno, že se jedná o léčbu bezpečnou, v souvislosti s její aplikací nebyly zaznamenány žádné letální komplikace. Přínosy imunoterapie jednoznačně vysoce převyšují možná rizika. Pokud k alergické reakci po VIT dojde, pak nejčastěji vídáme lokální otok a bolestivosti v místě podání, systémové reakce po aplikaci jsou málo časté a dobře reagují na protialergickou medikaci [13].
Závěr
Pacienti s alergií na včelí
a vosí jed mají díky léčbě specifickou imunoterapií
příslušným hmyzím jedem naději vést kvalitní život bez obav
z dalšího bodnutí. Specifická imunoterapie totiž významně
snižuje riziko opakování závažné život ohrožující alergické
reakce po dalším bodnutí a poskytuje tak ochranu
naprosté většině léčených pacientů
.
Seznam použité literatury
- [1] Antonicelli L, Bilo MB, Bonifazi F. Epidemiology of Hymenoptera allergy. Curr Opin Allergy Clin Immunol 2002; 2: 341–346.
- [2] Bilò MB, Bonifazi F. The natural history and epidemiology of insect venom allergy: clinical implications. Clin Exp Allergy 2009; 39: 1467–1476.
- [3] Bilò BM, Bonifazi F. Epidemiology of insect‑venom anaphylaxis. Curr Opin Allergy Clin Immunol 2008; 8: 330–337.
- [4] Bilò BM, Rueff F, Mosbech H, et al., EAACI Interest Group on Insect Venom Hypersensitivity. Diagnosis of Hymenoptera venom allergy. Allergy 2005; 60: 1339–1349.
- [5] Sturm GJ, Arzt‑Gradwohl L, Varga EM. Medical Algorithms: Diagnosis and treatment of Hymenoptera venom allergy. Allergy 2019; 74: 2016–2018.
- [6] Korosec P, Valenta R, Mittermann I, et al. High sensitivity of CAP‑FEIA rVes v 5 and rVes v 1 for diagnosis of Vespula venom allergy. J Allergy Clin Immunol 2012; 129: 1406–1408.
- [7] Vachova M, Panzner P, Malkusova I, et al. Utility of laboratory testing for the diagnosis of Hymenoptera venom allergy. Allergy Asthma Proc 2016; 37: 248–255.
- [8] Arzt L, Bokanovic D, Schrautzer C, et al. Questionable diagnostic benefit of the commercially available panel of bee venom components. Allergy 2017; 72: 1419–1422.
- [9] Vachová M, Panzner P, Kopač P, et al. Routine clinical utility of honeybee venom allergen components. J Allergy Clin Immunol Pract 2018; 6: 2121–2123.
- [10] Eberlein B, Krischan L, Darsow U, et al. Double positivity to bee and wasp venom: improved diagnostic procedure by recombinant allergen‑based IgE testing and basophil activation test including data about cross‑reactive carbohydrate determinants. J Allergy Clin Immunol 2012; 130: 155–161.
- [11] Korosec P, Erzen R, Silar M, et al. Basophil responsiveness in patients with insect sting allergies and negative venom‑specific immunoglobulin E and skin prick test results. Clin Exp Allergy 2009; 39: 1730–1737.
- [12] Bilò MB, Cichocka‑Jarosz E, Pumphrey R, et al. Self‑medication of anaphylactic reactions due to Hymenoptera stings‑an EAACI Task Force Consensus Statement. Allergy 2016; 71: 931–943.
- [13] Sturm GJ, Varga EM, Roberts G, et al. EAACI guidelines on allergen immunotherapy: Hymenoptera venom allergy. Allergy 2018; 73: 744–764.
- [14] Pitsios C, Demoly P, Bilò MB, et al. Clinical contraindications to allergen immunotherapy: an EAACI position paper. Allergy 2015; 70: 897–909.