Algoritmus léčby hyperglykemie u nemocných s diabetem 2. typu
Léčba hyperglykemie je základní součástí komplexní péče o nemocného s diabetem 2. typu. Významně redukuje riziko rozvoje a progrese mikrovaskulárních komplikací diabetu, a to v kterémkoli stadiu choroby a nezávisle na volbě léčebného prostředku. Význam léčby hyperglykemie z hlediska redukce kardiovaskulárního (KV) rizika je stále předmětem diskusí, stejně jako její vliv na redukci nádorových onemocnění a možnost ovlivnění progresivního úbytku sekrece inzulinu. Intervenční studie zveřejněné během let ukazují na nutnost diferencovaného přístupu k nemocným. Významně příznivý efekt na redukci KV rizika má těsná kompenzace diabetu zejména u osob časně po záchytu cukrovky v primární KV prevenci. Uplatňuje se tzv. metabolická paměť. Naopak příliš agresivní léčba hyperglykemie u diabetiků s pokročilými komplikacemi a již manifestním KV onemocněním riziko KV úmrtí zvyšuje, pravděpodobně v souvislosti s výskytem hypoglykemií. Pro léčbu hyperglykemie stanovujeme individuální léčebné cíle. Cílové hodnoty HbA1c u osob s nízkým KV rizikem jsou < 4,5 %. U nemocných v sekundární prevenci jsme méně přísní (HbA1c < 6 %) a zásadním požadavkem je bezpečnost léčby (nepřítomnost hypoglykemií). Přednost dáváme pozvolnému zlepšování kompenzace. Základem léčby hyperglykemie jsou režimová opatření a podávání farmak s antidiabetickým účinkem. Lékem 1. volby u diabetiků 2. typu je metformin, jehož podávání zahajujeme ihned po záchytu diabetu spolu s režimovými opatřeními. Pokud monoterapie nezajistí uspokojivou kompenzaci, přidáváme do kombinace další farmaka (glitazony, glinidy, gliptiny, inkretinová mimetika, deriváty sulfonylurey, akarbózu, inzulin). Protože není jasné, které hypoglykemizující prostředky jsou výhodné z hlediska dlouhodobé prognózy nemocného, je postup liberální. Inzulin zůstává zatím lékem 2. volby. U nemocných s diabetem 2. typu není potvrzeno, jaký inzulinový režim je nejvýhodnější z hlediska dlouhodobé prognózy nemocných, proto léčbu zahajujeme obvykle jednodušším schématem. Pokud nejsou přítomny kontraindikace, inzulin podávaný v jakémkoli režimu vždy kombinujeme s metforminem. Součástí komplexní péče je edukace nemocného a pravidelný screening případných komplikací diabetu.
Úvod
Diabetes mellitus 2. typu (DM2T) je jedním z projevů metabolického syndromu. DM2T se často manifestuje až jako pozdní klinická abnormita. Nemocný je obvykle obézní nebo má nadváhu (centrální obezi-ta), postupně se u něj objevují dyslipidemie a hypertenze a často má již za sebou kardiovaskulární (KV) příhodu. Hyperglykemie proto bývá označována jako špička ledovce. Dalšími projevy metabolického syndromu jsou endoteliální dysfunkce, subklinický zánět a zvýšené riziko trombózy. Kromě uvedených je metabolický syndrom asociován s nealkoholickou jaterní stea-tózou, syndromem polycystických ovarií, zvyšuje riziko celkové mortality a riziko některých nádorů. Jednotlivé komponenty metabolického syndromu jsou riziko-vými faktory KV onemocnění a například hypertenze je zároveň nepochybným rizikovým faktorem rozvoje mikrovaskulárních komplikací diabetu.
Proto jako terapii DM2T chápeme nejen léčbu hyperglykemie, ale rozumíme jí soubor komplexních opatření, která zahrnují zároveň léčbu dalších projevů metabolického syndromu. Jde zejména o ovlivnění hypertenze, dyslipidemie, centrální obezity a o antiagregační léčbu.
Základní patogenetickou odchylkou při rozvoji hyperglykemie je inzulinová rezistence, ale rozhodujícím faktorem, který podmiňuje progresi glukoregulační poruchy a stojí v pozadí typického „zhoršování“ klinického obrazu DM2T, je progresivní selhání B-buněk. V současné době neexistuje způsob, jak postupující selhání sekrece inzulinu zastavit.
Cíle léčby nemocného s DM2T, jimž se snažíme přiblížit, jsou:
- co nejlepší kvalita života;
- redukce celkové mortality a morbidity;
- redukce kardiovaskulární mortality a morbidity;
- prevence a léčba mikrovaskulárních komplikací;
- redukce výskytu nádorových onemocnění;
- prevence progresivního úbytku sekrece inzulinu.
Hyperglykemie a riziko cévních komplikací
Léčba hyperglykemie významně redukuje riziko rozvoje a progrese mikrovas-kulárních komplikací diabetu 2. typu, a to v kterémkoli stadiu choroby a nezávisle na volbě léčebného prostředku [1, 2].
Význam léčby hyperglykemie z hlediska redukce KV rizika je stále předmětem diskusí. Je jednoznačně dokumentován v experimentálních [3] a epidemiologických studiích, v nichž je hyperglykemie jasným nezávislým rizikovým faktorem KV mortality a morbidity [4, 5]. KV riziko se extrémně zvyšuje, pokud jsou splněna kritéria diabetu, který s sebou navíc přináší rizika mikrovaskulárních komplikací (diabetická nefropatie, retinopatie a neuropatie). Pro glykemii nebyla v epidemiologických studiích nalezena prahová hodnota, každé snížení glykemie a HbA1c, dokonce i v rozmezí normálních hodnot [4], je provázeno další redukcí KV rizika.
Intervenční studie u diabetiků nevyznívají tak jednoznačně; efekt léčby na redukci KV mortality nebyl ve studiích staršího data významný nebo se pohyboval na hranici významnosti [1, 6, 7]. Důležité je, že pouze 10–40 % nemocných ve studiích publikovaných v minulých letech dosahovalo cílových hodnot HbA1c. V roce 2008 a 2009 byly zveřejněny výsledky velkých randomizovaných, multicentrických intervenčních studií VADT [8], ACCORD [9], ADVANCE [2] a RECORD [10]. Ani ony neprokazují v celých souborech významný pozitivní vliv intenzivní léčby hyperglykemie na KV mortalitu, a studie ACCORD [9] dokonce poukázala na vyšší úmrtnost v intenzivně léčené skupině diabetiků s vy-sokým KV rizikem. Významný posun však přineslo prodloužené sledování nemocných zařazených do UKPDS [11]; ukázalo, že za deset let po ukončení studie je zaznamenávána významně nižší KV mortalita u původně intenzivně léčených nemocných s DM2T, přestože kompenzace byla již bez rozdílů.
Uvedené intervenční studie přinesly nové poznatky s konkrétními dopady na léčbu diabetiků. Doložily, že agresivními způsoby léčby je možné dosáhnout cílových hodnot glykemie s koncentrací HbA1c nižší než 5,3 % (53 mmol/mol) u 70–80 % nemocných, ale že zlepšení kompenzace je provázeno zvýšenou frekvencí hypoglykemických příhod. Hypoglykemie jsou nepochybným rizikovým faktorem KV příhod a mohou tak smazat případné pozitivní vlivy těsné kompenzace. Studie také upozorňují na poměrně dlouhou dobu latence, po které se může příznivý efekt normoglykemie projevit, a na nutnost diferencovaného přístupu k nemocným. Významně příznivý efekt na redukci KV rizika má těsná kompenzace diabetu zejména u osob časně po záchytu cukrovky v primární KV prevenci. Uplatňuje se tzv. metabolická paměť. Na-opak příliš agresivní léčba hyperglykemie u diabetiků s pokročilými komplikacemi a již manifestním KV onemocněním může KV riziko úmrtí dokonce zvýšit, pravděpodobně v souvislosti s výskytem hypoglykemií.
V současné době nemáme jasné doklady pro rozdíly mezi používanými hypoglykemizujícími prostředky, které by z hlediska prevence cévních komplikací odůvodnily jejich přednostní užití. Určité výhody z hlediska KV rizika má podávání metforminu [11], akarbózy u osob s poruchou glukózové tolerance [12] a pioglitazonu u diabetiků s vysokým KV rizikem [6]. Relativně bezpečná je také léčba deriváty sulfonylurey (SU) [1, 2] nebo inzulinem [1, 7]. Definitivní doklady pro KV bezpečnost zatím logicky chybí u novějších látek s inkretinovým účinkem.
Hyperglykemie a riziko nádorových onemocnění
Diabetes zvyšuje v epidemiologických sledováních riziko vzniku nádorových onemocnění, například riziko karcinomu (ca) prsu 1,2krát, ca pankreatu 1,8krát, ca endometria 2krát, kolorektálního ca 1,3krát, ca močového měchýře 1,2krát. V intervenčních studiích však léčba hyperglykemie nevede k významné redukci rizika nádorových onemocnění [13, 14].
Z hlediska volby jednotlivých hypoglykemizujících prostředků a rizika nádorových onemocnění jsou výsledky epidemiologických observačních studií a metaanalýz dostupných intervenčních studií následující: inzulin je hormon, který má prokazatelný mitogenní a proliferační efekt. Léčba inzulinem (bez ohledu na typ) zvyšuje riziko vzniku ca. Toto riziko se zvyšuje úměrně s celkovou dávkou inzulinu (dobou expozice). Při izolované léčbě inzulinem trvající déle než 15 let se riziko ca zvyšuje až 5krát. Zatím dostupná klinická data, byť operující s malými čísly, nesignalizují vyšší riziko vzniku nádorů při léčbě inzulinovými analogy (ultrakrátká analoga a dlouze působící analoga detemir a glargin) oproti humánnímu inzulinu. Deriváty SU jako stimulátory sekrece endogenního inzulinu pravděpodobně také zvyšují riziko karcinogeneze, a to dle epidemiologických analýz asi 1,3krát. Naproti tomu metformin riziko vzniku ca snižuje (RR-0,8) a při současném podávání s inzulinem snižuje inzulinem indukovaný vzestup rizika na polovinu [15, 16]. Existují také doklady o tom, že léčba metforminem zlepšuje odpověď ca prsu na chemoterapii, blokuje růst tumoru a prodlužuje remisi. Podobně nadějně se do loňského roku jevily i glitazony. V loňském roce se objevily určité pochybnosti a diskutuje se na téma pioglitazon a riziko karcinomů močového měchýře. Pioglitazon je v současné době v tomto směru pečlivě sledovaným lékem jak v Americe (FDA), tak v Evropě (EMA). Pro farmaka ze skupiny inkretinů zatím chybí dostatečně průkazná data, vzhledem k relativně krátké době jejich používání [13, 14].Hyperglykemie a progresivní úbytek sekrece inzulinu
V průběhu DM2T dochází k progresivnímu úbytku v sekreci inzulinu v důsledku poklesu masy B-buněk. Uplatnit se může řada různých mechanismů (glukotoxicita, lipotoxicita, oxidační stres, humorální mechanismy včetně poruch sekrece inkretinů, stres endoplazmatického retikula, dysfunkce mitochondrií, inzulinová rezistence B-buněk a další). Určitý ochranný vliv na B-buňky má normoglykemie bez ohledu na použitý léčebný prostředek. V klinických studiích zaměřených na prevenci diabetu byl prokázán příznivý účinek režimových opatření, podávání metforminu, glitazonů, orlistatu, akarbózy, a účinek blokády RAS. Z dlouhodobého hlediska však v současné době nemáme k dispozici žádné léčebné prostředky, kterými bychom mohli postupující úbytek sekrece inzulinu zastavit. Naděje se vkládají do inkretinové léčby, byť definitivní potvrzení její efektivity v klinické praxi zatím chybí [17].Výběr farmak v léčbě hyperglykemie
V léčbě hyperglykemie tradičně využíváme perorální antidiabetika (metformin, glitazony – thiazolidindiony, akarbózu, deriváty SU, glinidy), inzulin a nejnověji léky na bázi inkretinů (inkretinová mimetika či inhibi-tory dipeptidylpeptidázy-4, DPP-4 – gliptiny). V posledních letech se objevily na far-maceutickém trhu některé nové molekuly, zatím posledním registrovaným antidiabetikem je linagliptin. Jsme svědky postupného rozšiřování jejich indikací k užití v monoterapii či v kombinační léčbě s inzulinem a jejich postupného uvolnění například pro nemocné se srdečním selháním či selháním ledvin.
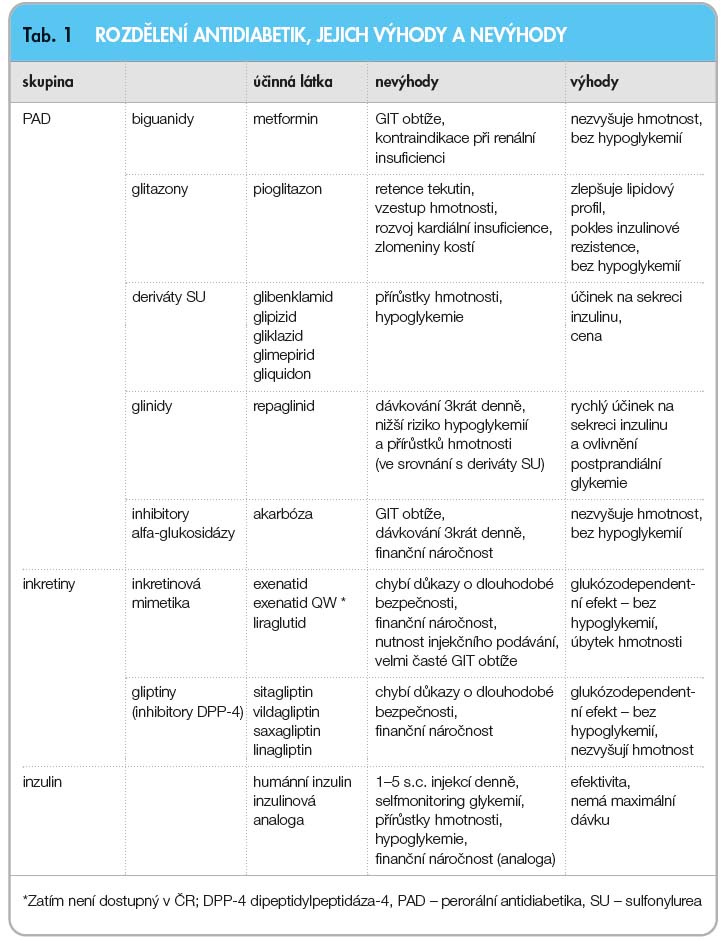 Rozdělení farmak, která jsou v současné době registrována a jsou k dispozici v našich lékárnách, jejich výhody a nevýhody shrnuje tab. 1.
Rozdělení farmak, která jsou v současné době registrována a jsou k dispozici v našich lékárnách, jejich výhody a nevýhody shrnuje tab. 1.
V současné době chybí přesvědčivé klinické důkazy pro výhodnost některého z po-užívaných farmak z hlediska dlouhodobé prognózy nemocného (KV mortalita, riziko nádorových onemocnění, progrese mikrovaskulárních komplikací) a ochrany B-buněk.
Účinek na pokles glykemie a zlepšení kompenzace je u všech jmenovaných farmak s výjimkou inzulinu velmi podobný, náš výběr se obvykle řídí nežádoucími účinky a kontraindikacemi jednotlivých lékových skupin a roli hraje i cena.
Protože hlavní překážkou v dosažení těsné kompenzace jsou hypoglykemie, o nichž je také známo, že zvyšují KV mortalitu, je logické, že přednost by měla mít farmaka, při jejichž podávání je riziko hypoglykemií nízké. Riziko hypoglykemií přináší léčba inzulinem a deriváty SU, mírně ho zvyšuje také léčba repaglinidem. Druhým problémem při léčbě DM2T jsou přírůstky hmotnosti. Nejvyšší hmotnostní přírůstky pozorujeme při léčbě inzulinem, pioglitazonem, deriváty SU, mírné až žádné v závislosti na intenzitě edukace při léčbě metforminem, hmotnostně neutrální jsou gliptiny a jedinými zástupci antidiabetik, která redukují hmotnost, jsou inkretinová mimetika.
Předpokládá se, že asi polovina nemocných s DM2T má určitý stupeň funkčního postižení ledvin. Redukce funkčního parenchymu ledviny a pokles renálních funkcí je obvykle provázen vyšším rizikem těžkých hypoglykemií a nutností redukovat dávky inzulinu, eventuálně inzulinových sekretagog. Výběr farmak k léčbě hyperglykemie ve fázi renálního selhání je ovlivněn farmakologickými vlastnostmi jednotlivých farmak s ohledem na podíl ledvin na jejich metabolismu a vylučování. Během posledních několika měsíců došlo v souvislosti s ukončením klinických hodnocení, která testovala účinnost a bezpečnost některých novějších farmak v různých fázích chronické renální i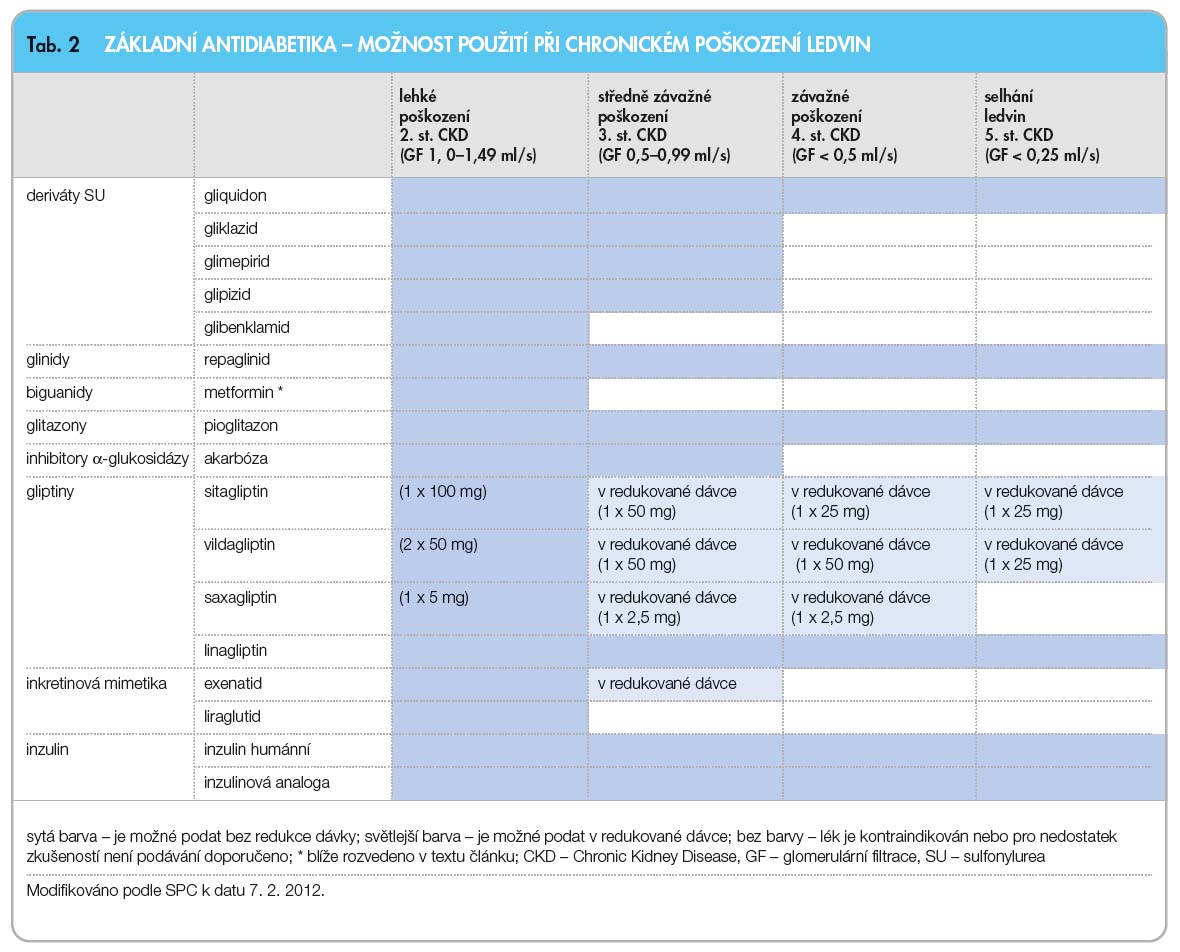 nsuficience, k uvolnění jejich použití v této indikaci. Ve fázi terminálního selhání ledvin (chronic kidney disease, CKD 5. stupně, odhadovaná glomerulární filtrace – eGF < 0,25 ml/s) můžeme bezpečně podávat inzulin, pioglitazon a linagliptin; možné je podávání gliquidonu a repaglinidu, u nichž je však třeba pamatovat na riziko hypoglykemií a v případě potřeby upravit dávky. Nově je v redukované dávce použitelný i vildagliptin a sitagliptin. U osob s těžkou renální insuficiencí (CKD 4. stupně, eGF 0,25–0,5 ml/s) můžeme podat v redukované dávce také saxagliptin. Indikace a dávkování antidiabetik při snížené funkci ledvin uvádí tab. 2, která je převzata ze společných doporučení pro léčbu diabetického onemocnění ledvin České diabetologické společnosti (ČDS) České lékařské společnosti Jana Evangelisty Purkyně a České nefrologické společnosti (ČNS) [18].
nsuficience, k uvolnění jejich použití v této indikaci. Ve fázi terminálního selhání ledvin (chronic kidney disease, CKD 5. stupně, odhadovaná glomerulární filtrace – eGF < 0,25 ml/s) můžeme bezpečně podávat inzulin, pioglitazon a linagliptin; možné je podávání gliquidonu a repaglinidu, u nichž je však třeba pamatovat na riziko hypoglykemií a v případě potřeby upravit dávky. Nově je v redukované dávce použitelný i vildagliptin a sitagliptin. U osob s těžkou renální insuficiencí (CKD 4. stupně, eGF 0,25–0,5 ml/s) můžeme podat v redukované dávce také saxagliptin. Indikace a dávkování antidiabetik při snížené funkci ledvin uvádí tab. 2, která je převzata ze společných doporučení pro léčbu diabetického onemocnění ledvin České diabetologické společnosti (ČDS) České lékařské společnosti Jana Evangelisty Purkyně a České nefrologické společnosti (ČNS) [18].
Lékem volby u diabetiků 2. typu zůstává v současné době metformin [19, 20]. Výhodou metforminu je, že nezvyšuje riziko hypoglykemií a hmotnostních přírůstků a jeho postavení podporují data o KV bezpečnosti [21] a epidemiologické analýzy dokumentující nízké riziko nádorových onemocnění [15, 16]. Podávání metforminu je klasicky spojováno s rizikem laktátové acidózy a kvůli tomuto riziku byl donedávna kontraindikován u srdečního selhání. Hladina metforminu však nekoreluje s hladinou laktátu a frekvence laktátové acidózy je stejná u nemocných léčených metforminem jako u nemocných bez metforminu [22]. Kauzalita mezi podáváním metforminu a laktátovou acidózou byla proto v posledních letech přehodnocena, stejně jako kontraindikace léčby metforminem při srdečním selhání. Podle řady registrů totiž metformin snižuje mortalitu nemocných s chronickým srdečním selháním a jeho po-dávání bylo v Evropě doporučeno u všech nemocných se stabilním chronickým srdečním selháním, pokud mají glomerulární fil-traci převyšující 0,5 ml/s [23].
Hlavní praktickou kontraindikací podávání metforminu zůstává podle platného SPC renální insuficience, jejíž závažnost však není specifikována. Konkrétní doporučení evropských i amerických odborných společností se různí [24]. Podle recentních společných doporučení ČDS a ČNS [18] je metformin kontraindikován při těžké renální insuficienci (eGF < 0,5 ml/s). Při eGF 0,5–1 ml/s (CKD 3. stupně) léčbu metforminem nově nezahajujeme, u již léčených nemocných snižujeme dávku metforminu na polovinu. Při eGF > 1 ml/s podáváme metformin bez omezení dávky. Obvyklá dávka metforminu je 2krát denně 1000 mg (maximální denní dávka 3000 mg). Podmínkou je kontrola hladiny kreatininu v séru a kontrola renálních funkcí – minimálně 1krát za rok u osob s normální eGF a 4krát za rok u osob s poruchou renálních funkcí.
Protože zatím nebyly doloženy žádné výhody inzulinu oproti perorálním antidiabetikům, je inzulin u nemocného s DM2T využíván z praktických důvodů jako prostředek 2. volby v období po selhání per-orálních antidiabetik, eventuálně inkretinové léčby. U diabetiků 2. typu je však možné k léčbě inzulinem sáhnout v kterémkoli stadiu choroby, včetně období ihned po manifestaci cukrovky. V současné době dokončená studie ORIGIN [25], která testuje vliv časného podání glarginu u osob s poruchou glukózové homeostázy či s nově zjištěným DM2T na KV mortalitu, možná přinese změny v zavedené strategii. Její výsledky budou poprvé představeny v červnu 2012 na kongresu Americké diabetické asociace. Pokud je u nemocného s DM2T indikována léčba inzulinem, pak vždy, pokud není kontraindikace, kombinujeme inzulin s metforminem. Byť neexistují intervenční studie, které by pro-kázaly, že kombinovaná léčba inzulinem a perorálními antidiabetiky (PAD) má oproti monoterapii inzulinem jasné výhody z hlediska mortality a morbidity diabetiků či z hlediska přirozeného průběhu choroby, podpořily v poslední době tuto strategii poznatky výše uvedených epidemiologických studií, které dokládají příznivý účinek léčby metforminem na redukci mortality na nádorová onemocnění [16].
Nedořešenou otázkou také zůstává, jaký inzulinový režim je u nemocných s DM2T výhodnější z hlediska KV mortality, dlouhodobé prognózy a z hlediska ovlivnění přirozeného průběhu choroby. HEART2D byla první randomizovanou intervenční studií, která řešila, zda je z dlouhodobého hlediska výhodnější ovlivňovat bazální glykemii, nebo postprandiální vzestupy glykemie. Ukázala, že po 5 letech léčby není patrný rozdíl v KV mortalitě u skupiny léčené jednou dávkou bazálního inzulinu či 3 dávkami prandiálního inzulinu [26]. Studie 4T navíc doložila menší výskyt hypo-glykemií a nižší hmotnostní přírůstky při iniciaci inzulinu formou jedné dávky bazálního inzulinu proti intenzifikované léčbě, byť po jednom roce léčby bylo nutné u dvou třetin nemocných intenzifikovat režim a přidávat další dávky inzulinu [27].
Praktické postupy
Podle posledních doporučení ČDS z roku 2012 [20], která jsou v souladu s evropskými [28] a americkými standardy [29], je prevence a léčba chronických cévních komplikací, včetně makrovaskulárních, samozřejmou součástí komplexních opatření, která následují po vyšetření diabetika a stanovení diagnózy. Kromě léčby hyperglykemie zahrnují snahu o ovlivnění všech ovlivnitelných rizikových faktorů, tj. zanechání kouření, léčbu hypertenze, dyslipidemie a obezity a eventuálně anti-agregační terapii [30].
Při léčbě hyperglykemie platí následující zásady – uplatňuje se diferencovaný přístup k nemocným: cílové hodnoty HbA1c u osob s nízkým KV rizikem jsou < 4,5 % (méně než 45 mmol/mol). U nemocných v sekundární prevenci jsme méně přísní (HbA1c < 6 %; 60 mmol/mol). Hodnota HbA1c kolem 5,3 % (53 mmol/mol) je obvyk-le považována za určitou hranici, která nutí k revizi stávající léčby, nicméně cílové hodno-ty u konkrétního pacienta vždy volíme individuálně. Zásadním požadavkem je bezpečnost léčby (nepřítomnost hypoglykemií). Přednost dáváme pozvolnému zlepšování kompenzace a větší důraz je kladen na edukaci nemocného a selfmonitoring. Základním kamenem léčby jsou režimová opatření.
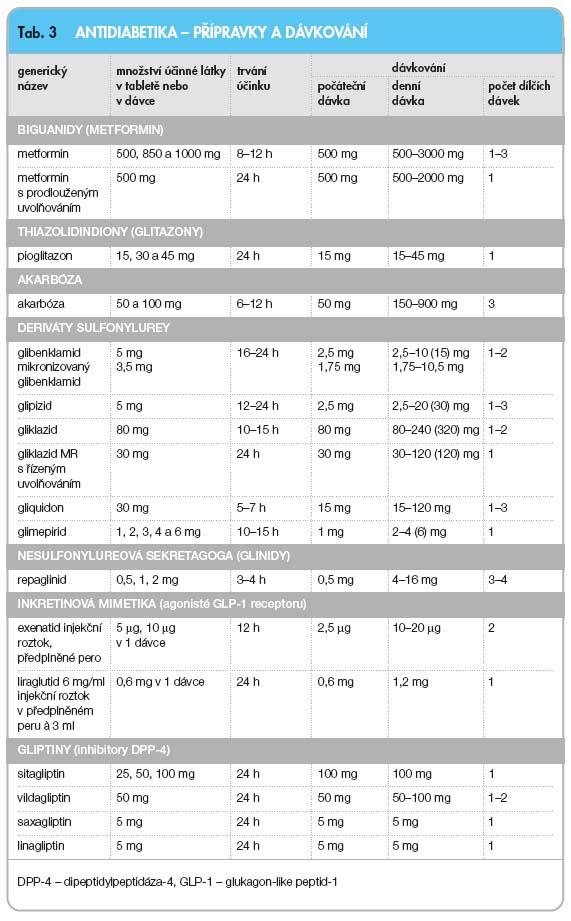 Lékem 1. volby je metformin, jehož podávání zahajujeme ihned po záchytu diabetu, nezávisle na hmotnosti pacienta, spolu s režimovými opatřeními. Pokud monoterapie nezajistí uspokojivou kompenzaci, přidáváme do kombinace další perorální antidiabetika, léky s inkretinovým účinkem nebo inzulin. Léčiva dostupná na českém trhu a jejich dávkování uvádí tab. 3. Výčet dostupných kombinovaných farmak shrnuje tab. 4. Protože není jasné, které hypoglykemizující prostředky jsou výhodné z hlediska dlouhodobé prognózy nemocného, je postup při jejich volbě liberální [20].
Lékem 1. volby je metformin, jehož podávání zahajujeme ihned po záchytu diabetu, nezávisle na hmotnosti pacienta, spolu s režimovými opatřeními. Pokud monoterapie nezajistí uspokojivou kompenzaci, přidáváme do kombinace další perorální antidiabetika, léky s inkretinovým účinkem nebo inzulin. Léčiva dostupná na českém trhu a jejich dávkování uvádí tab. 3. Výčet dostupných kombinovaných farmak shrnuje tab. 4. Protože není jasné, které hypoglykemizující prostředky jsou výhodné z hlediska dlouhodobé prognózy nemocného, je postup při jejich volbě liberální [20].
 Poslední revidovaná doporučení NICE z roku 2010 [31] jsou poměrně rezervovaná a staví inkretinová mimetika (exenatid, liraglutid) do pozice farmak, jimiž se snažíme oddálit léčbu inzulinem nebo která použijeme tam, kde nemůžeme podávat jiná PAD. Podle NICE by léčba inkretinovými mimetiky měla být zvážena v následujících případech: a) do trojkombinace s dalšími farmaky, a to především u osob s BMI > 35 kg/m2. U osob s BMI < 35 kg/m2 podporuje jejich indikaci potenciální příznivý vliv na redukci hmotnosti a okolnosti, které brání zahájení léčby inzulinem; b) do dvojkombinace by měla být inkretinová mimetika přidána pouze tehdy, pokud není možné použít z důvodů nesnášenlivosti nebo kontraindikace metformin nebo derivát SU a není-li možné ze stejných důvodů použít pioglitazon či gliptin.
Poslední revidovaná doporučení NICE z roku 2010 [31] jsou poměrně rezervovaná a staví inkretinová mimetika (exenatid, liraglutid) do pozice farmak, jimiž se snažíme oddálit léčbu inzulinem nebo která použijeme tam, kde nemůžeme podávat jiná PAD. Podle NICE by léčba inkretinovými mimetiky měla být zvážena v následujících případech: a) do trojkombinace s dalšími farmaky, a to především u osob s BMI > 35 kg/m2. U osob s BMI < 35 kg/m2 podporuje jejich indikaci potenciální příznivý vliv na redukci hmotnosti a okolnosti, které brání zahájení léčby inzulinem; b) do dvojkombinace by měla být inkretinová mimetika přidána pouze tehdy, pokud není možné použít z důvodů nesnášenlivosti nebo kontraindikace metformin nebo derivát SU a není-li možné ze stejných důvodů použít pioglitazon či gliptin.
Doporučení ČDS z roku 2012 [20] jsou v indikacích inkretinových mimetik v kombinační léčbě poměrně liberální. Hlavní podpůrné kritérium pro podání je BMI > 35 kg/m2. Doporučení umožňují použít agonisty GLP-1R v trojkombinaci i v dvojkombinaci, pokud stávající léčba není uspokojivá, tj. HbA1c je vyšší než 5,3 %.
Inzulin zatím zůstává lékem druhé volby. Při jeho iniciaci volíme jednodušší inzulinová schémata v kombinaci s metforminem, přestože tvrdé důkazy, které by podpořily racionálnost tohoto postupu, zatím chybí.
Součástí léčby je edukace zaměřená na změnu stravovacích zvyklostí a životního stylu, včetně zákazu kouření. Pokud je nemocný léčen PAD či inkretiny, pak musí být seznámen s riziky, jež tato léčba přináší. Při léčbě inzulinem, zvláště intenzifikovaným způsobem, je nutnou podmínkou selfmonitoring glykemií a samostatné úpravy dávek inzulinu.
Nezbytnou součástí péče o nemocného s diabetem je pravidelný screening všech potenciálních cévních komplikací diabetu.
Práce vznikla s podporou grantu IGA MZČR č. NT/ 11238-4.
Seznam použité literatury
- [1] UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonyl-ureas or insulin compared with conventional
- [2] Patel A, MacMahon S, Chalmers J, et al. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl
- [3] Chait A, Bornfeldt KE. Diabetes and atherosclerosis: is there a role for hyperglycemia? J Lipid Res 2009; 50 Suppl: S335–339.
- [4] Selvin E, Steffes MW, Zhu H, et al. Glycated hemoglobin, diabetes, and cardiovascular risk
- [5] Nesto RW. Correlation between cardiovascular disease and diabetes mellitus: current concepts. Am J Med 2004; 116 Suppl 5A: 11S–22S.
- [6] Dormandy JA, Charbonnel B, Eckland DJ, et al. Secondary prevention of macrovascular events in patients with type 2 diabetes in the PROactive Study (PROspective pioglitAzone Clinical
- [7] Malmberg K, Ryden L, Wedel H, et al. Intense metabolic control by means of insulin in patients with diabetes mellitus and acute myocardial infarction (DIGAMI 2): effects on mortality and morbidity. Eur Heart J 2005; 26: 650–661.
- [8] Duckworth W, Abraira C, Moritz T, et al. Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med 2009; 360: 129–139.
- [9] Gerstein HC, Miller ME, Byington RP, et al. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med 2008; 358: 2545–2559.
- [10] Home PD, Pocock SJ, Beck-Nielsen H, et al. Rosiglitazone evaluated for cardiovascular outcomes in oral agent combination therapy for
- [11] Holman RR, Paul SK, Bethel MA, et al. 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med 2008; 359: 1577–1589.
- [12] Chiasson JL, Josse RG, Gomis R, et al. Acarbose treatment and the risk of cardiovascular disease and hypertension in patients with impai-red glucose tolerance: the STOP-NIDDM trial. Jama 2003; 290: 486–494.
- [13] Giovannucci E, Harlan DM, Archer MC, et al. Diabetes and cancer: a consensus report. Diabetes Care 2010; 33: 1674–1685.
- [14] Svačina Š. Existuje vztah mezi léčbou diabetu a vznikem nádorů? Vnitř Lék 2011; 57: 760–763.
- [15] Gallagher EJ, LeRoith D. Diabetes, cancer,
- [16] Landman GW, Kleefstra N, van Hateren KJ,
- [17] Pelikánová T. Přežití beta buněk. Nový aspekt v léčbě diabetu 2. typu. In: Rušavý Z, ed. Technologie v diabetologii. Praha: Galén; 2010, 218–232.
- [18] Bouček P, Kvapil M, Monhart V, et al. Doporučené postupy při diabetickém onemocnění ledvin 2012. Společná doporučení České diabetologické společnosti ČLS JEP a České nefrologické společnosti. 2012: dostupné na www.diab.cz
- [19] Schernthaner G, Barnett AH, Betteridge DJ, et al. Is the ADA/EASD algorithm for the management of type 2 diabetes (January 2009) based on evidence or opinion? A critical analysis. Diabetologia 2010; 53: 1258–1269.
- [20] ČDS. Česká diabetologická společnost. Doporučený postup péče o diabetes mellitus 2. typu – aktualizace 2012, dostupné na www.diab.cz.
- [21] UK Prospective Diabetes Study (UKPDS) Group. Effect of intensive blood-glucose control with metformin on complications in overweight pa-tients with type 2 diabetes (UKPDS 34). Lancet 1998; 352: 854–865.
- [22] Salpeter SR, Greyber E, Pasternak GA, et al. Risk of fatal and nonfatal lactic acidosis with metformin use in type 2 diabetes mellitus. Arch Intern Med 2003; 163: 2594–2602.
- [23] Dickstein K, Cohen-Solal A, Filippatos G, et al. ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2008: the Task Force for the diagnosis and treatment of acute and chronic heart failure 2008 of the European Society of Cardiology. Developed in collabora-tion with the Heart Failure Association of the ESC (HFA) and endorsed by the European Society of Intensive Care Medicine (ESICM). Eur J Heart Fail 2008; 10: 933–989.
- [24] Lipska KJ, Bailey CJ, Inzucchi SE. Use of metformin in the setting of mild-to-moderate renal insufficiency. Diabetes Care 2011; 34: 1431–1437.
- [25] Origin Trial Investigators, Gerstein H, Yusuf S,
- [26] Raz I, Wilson PW, Strojek K, et al. Effects of
- [27] Holman RR, Farmer AJ, Davies MJ, et al. Three-
- [28] Nathan DM, Buse JB, Davidson MB, et al. Me-dical management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initia-tion and adjustment of therapy: a consensus
- [29] Standards of medical care in diabetes – 2012. Diabetes Care 2012; 35 Suppl 1: S11–63.
- [30] Pelikánová T, Bartoš V. Praktická diabetologie, 5. vydání Praha: Maxdorf, 2011.
- [31] NICE technology appraisal guidance 203. Lira-glutide for the treatment of type 2 diabetes mellitus. Issued October 2010: dostupné na: www. nice.org.uk/guidance/TA203.