Co by měl kardiolog vědět o diabetes mellitus 2. typu a léčbě perorálními antidiabetiky
Prevalence diabetes mellitus 2. typu v současné době stoupá ve všech vyspělých zemích světa včetně České republiky. Zároveň se zvyšuje výskyt chronických komplikací, kam patří mikrovaskulární a makrovaskulární komplikace, které jsou u diabetiků hlavní příčinou úmrtí. Pokud jim chceme předcházet, musíme diabetes mellitus včas diagnostikovat a především včas léčit. Základním lékem je metformin, který by měl být podáván prakticky všem pacientům s prediabetem a diabetem 2. typu. Výjimkou jsou gastrointestinální vedlejší účinky nebo zhoršení renálních funkcí. Vzhledem k tomu, že diabetici jsou ohroženi zvýšeným kardiovaskulárním rizikem, je třeba stále připomínat dobře doložené pozitivní kardiovaskulární účinky metforminu.
Úvod
Diabetes mellitus (DM) 2. typu je nejčastější metabolickou chorobou vyznačující se relativním nedostatkem inzulinu; v organismu vede tento stav k nedostatečnému využití glukózy projevujícímu se hyperglykemií. DM 2. typu vzniká při kombinaci porušené sekrece inzulinu a jeho působení v cílových tkáních, přičemž kvantitativní podíl obou poruch může být rozdílný. Nezbytným předpokladem vzniku DM 2. typu je přítomnost obou poruch, na nichž se podílejí jak faktory genetické, tak faktory zevního prostředí. Diabetes 2. typu je obvykle součástí tzv. metabolického syndromu, který se vyznačuje přítomností dalších abnormalit charakteru dyslipidemie, arteriální hypertenze, obezity centrálního typu, endoteliální dysfunkce a vyšší pohotovostí k tvorbě trombů. Kombinace těchto poruch významně zvyšuje kardiovaskulární riziko diabetiků. Kardiovaskulární komplikace jsou pak nejčastější příčinou mortality i morbidity pacientů s diabetem [1].
Prevalence diabetu je vysoká a trvale stoupá v populaci většiny vyspělých zemí světa. Česká republika není v tomto směru výjimkou. Podle epidemiologických údajů Ústavu zdravotnických informací a statistiky České republiky (ÚZIS ČR) bylo v ČR v roce 2011 registrováno 825 382 diabetiků. Vzrůst oproti roku 2010 činil 2,4 % a prevalence tak dosáhla v ČR 8 %. V 92 % případů onemocnění byl klasifikován DM 2. typu. Znamená to, že DM 2. typu se rozhodujícím způsobem podílí i na problémech spojených s komplikacemi provázejícími toto onemocnění. S rostoucím počtem diabetiků 2. typu narůstá i počet cévních komplikací zahrnujících jak mikroangiopatii, tak makroangiopatii. Vedle diagnostikovaných diabetiků 2. typu zůstává v naší populaci ještě značný počet nemocných, u nichž nebylo onemocnění zatím rozpoznáno [2, 3].
Diagnostika diabetu
O diagnóze diabetu svědčí:
a) přítomnost klinické symptomatologie provázené náhodnou glykemií vyšší než 11,0 mmol/l a následně glykemií v žilní plazmě nalačno, která dosahuje hodnoty 7,0 mmol/l nebo vyšší (stačí jedno měření);
b) při nepřítomnosti klinických projevů nález glykemie v žilní plazmě nalačno, která dosahuje hodnoty 7,0 mmol/l nebo vyšší po osmihodinovém lačnění (ověřit dvakrát);
c) nález glykemie za 2 hodiny při orálním glukózovém tolerančním testu (oGTT) vyšší než 11,0 mmol/l [1].
O prediabetu hoříme tehdy, je-li splněno alespoň jedno z následujících kritérií:
- přítomnost hraniční glykemie nalačno definovaná nálezem glykemie nalačno z žilní plazmy v rozmezí 5,6–6,9 mmol/l;
- porušená glukózová tolerance definovaná hodnotami glykemie v žilní plazmě ve 120. minutě oGTT 7,8–11,0 mmol/l;
- jako alternativní, ale nejpřesnější kritérium se do budoucna jeví zvýšení hodnoty glykovaného hemoglobinu (HbA1c) na 3,9–4,7 % (39–47 mmol/mol) dle IFCC.
Klinické projevy diabetu
Typický klinický obraz rozvinutého diabetu zahrnuje žízeň, polyurii, polydipsii a s nimi spojenou únavu. Nechutenství či pokles tělesné hmotnosti mohou a nemusejí být přítomny. Tyto klinické projevy jsou typické především pro pacienty s DM 1. typu, kdy je glykemie obvykle natolik vysoká, že klinické projevy jsou výrazné a pacient si jich brzy povšimne. Naopak vzestup glykemie u diabetiků 2. typu je velmi často pozvolný. U mnoha pacientů typické příznaky zcela chybějí. Jindy je podezření vysloveno při jiných potížích, jako je zánětlivé onemocnění, svědění, zhoršení zraku, nebo při jiném onemocnění, jako je ischemická choroba srdeční, ischemická choroba dolních končetin nebo cévní mozková příhoda. Navíc se tento typ diabetu vyskytuje především u starších pacientů trpících již řadou dalších obtíží a onemocnění. Diagnóza DM 2. typu tak může být zjištěna relativně pozdě, kdy už mohou být přítomny i některé chronické komplikace tohoto onemocnění. Bohužel u řady pacientů je DM 2. typu diagnostikován se zpožděním řady měsíců či let [4].
Cévní komplikace diabetu
Komplikace diabetu můžeme rozdělit na akutní a chronické. Mezi akutní komplikace patří především stavy spojené se závažnou akutně vzniklou hypoglykemií nebo hyperglykemií. Hyperglykemie může vyústit až v ketoacidotické hyperglykemické kóma (vyskytuje se převážně u diabetiků 1. typu), případně v hyperosmolární hyperglykemické kóma nebo laktacidotické kóma (u diabetiků 2. typu). Kardiology budou zajímat především chronické komplikace, které souvisejí jednak s délkou trvání diabetu a jednak se stupněm kompenzace diabetu. Dlouhodobá hyperglykemie je zásadním faktorem v rozvoji cévních komplikací diabetu. V závislosti na velikosti cév dělíme cévní postižení na mikroangiopatii a makroangiopatii.
Mikrovaskulární postižení vede u diabetu k orgánově specifickým komplikacím zahrnujícím diabetickou retinopatii, nefropatii, polyneuropatii a syndrom diabetické nohy. Závažnost mikrovaskulárních komplikací je ovlivněna stavem kompenzace diabetu, krevního tlaku, dyslipidemie, délkou trvání diabetu a genetickou predispozicí. Výskyt mikrovaskulárních komplikací u pacientů s DM 1. typu je relativně vzácný v prvních 5–10 letech trvání onemocnění, ale potom rychle narůstá. Naopak u diabetiků 2. typu jsou mikrovaskulární komplikace často přítomny již při záchytu diabetu vzhledem k jeho častému dlouhodobému latentnímu průběhu [5].
Makroangiopatie je v podstatě akcelerovaná ateroskleróza. Kardiovaskulární riziko u diabetiků 2. typu je dvoj- až čtyřnásobně vyšší ve srovnání s celkovou populací. Toto zvýšené riziko je zvláště patrné u žen s DM, jejichž rizikový profil je pak srovnatelný s muži. Na kardiovaskulární komplikace zemře přibližně 75 % pacientů s DM 2. typu a 35 % pacientů s DM 1. typu. Úspěšná a časná léčba hyperglykemie vede k příznivému ovlivnění rizika rozvoje makrovaskulárních komplikací. DM 2. typu představuje významné riziko pro vznik ischemických mozkových příhod, ischemické choroby srdeční a ischemické choroby dolních končetin [6].
Terapie DM 2. typu
Léčba hyperglykemie je u nemocného s DM 2. typu součástí komplexních opatření, která zahrnují i léčbu hypertenze, dyslipidemie, obezity a dalších projevů metabolického syndromu.
Snahou je dosáhnout cílových hodnot glykemií jakýmkoliv způsobem, ideálně při nepřítomnosti hypoglykemií a bez přírůstků hmotnosti. Léčba by měla být agresivní, s kontrolou HbA1c každé tři měsíce a s opakovanou revizí režimových opatření. U většiny pacientů, u nichž je cílem snížení rizika komplikací – u osob s nízkým rizikem vzniku nežádoucích příhod (tj. bez závažných chorob a zejména u krátce trvajícího diabetu), usilujeme o koncentraci HbA1c nižší než 45 mmol/mol (dle IFCC). U osob s přidruženými závažnými chorobami, u nichž hypoglykemie zvyšuje riziko komplikací, postačí cílová hodnota HbA1c do 60 mmol/mol. Po dosažení cílových hodnot HbA1c je minimální frekvence kontrol jedenkrát za 6 měsíců. Cíle léčby by měly být stanoveny individuálně.
Léčebný plán má být navržen tak, aby se dosáhlo optimální kompenzace diabetu co nejdříve po stanovení diagnózy s přihlédnutím k věku, zaměstnání, fyzické aktivitě, přítomnosti komplikací, přidruženým chorobám.
Nefarmakologická léčba
Nefarmakologická léčba tvoří základ léčby pacienta s DM 2. typu. Zahrnuje volbu individuálně stanovených dietních opatření a fyzické aktivity. Energetický obsah stravy je zvolen s přihlédnutím k tělesné hmotnosti, věku a režimu diabetika. Ošetřující lékař stanoví, zda postačuje dieta diabetická (s příslušným limitem sacharidů), či zda je vhodnější dieta redukční s ohledem na stupeň nadváhy. Cílem režimových opatření je přiblížit se k ideální hmotnosti. U obézních diabetiků se doporučuje dieta redukční [7–9].
Farmakologická léčba
Zahajuje se ihned při stanovení diagnózy diabetu. Lékem první volby je metformin. Jiná antidiabetika se použijí buď při jeho nesnášenlivosti, nebo vyžaduje-li to závažnost poruchy glykoregulace nebo klinický stav pacienta, kdy je třeba použít zpočátku inzulin. Pokud monoterapie nevede k dosažení požadované kompenzace, je třeba zvolit jednu z variant kombinované terapie perorálními antidiabetiky (PAD) nebo též inzulinem. Hodnota HbA1c kolem 53 mmol/mol je obvyklou hranicí, kdy se reviduje léčba, zvyšují se dávky antidiabetik nebo se upravuje jejich k![Obr. 1 Algoritmus léčby diabetes mellitus 2. typu; podle [1] – Standardy ČDS, 2012. GLP-1R – receptor pro glukagonu podobný peptid 1; HbA1c – glykovaný hemoglobin](https://www.remedia.cz/photo-a-29265---.jpg) ombinace, včetně podávání inzulinu. Algoritmus farmakologické léčby vychází z původního konsenzu ADA/EASD (American Diabetes Association/European Association for the Study of Diabetes) z roku 2008 (obr. 1) [1, 10].
ombinace, včetně podávání inzulinu. Algoritmus farmakologické léčby vychází z původního konsenzu ADA/EASD (American Diabetes Association/European Association for the Study of Diabetes) z roku 2008 (obr. 1) [1, 10].
Léčba je vedena tak, aby se výsledky co nejvíce přiblížily cílovým hodnotám, a to vždy s průměrnou dávkou farmak při monoterapii nebo kombinaci léčiv a při respektování všech kontraindikací léčby [1, 11]. Při léčbě se klade důraz na postprandiální glykemie, které významně ovlivňují dlouhodobou kompenzaci diabetu, a vedení léčby tudíž vyžaduje jejich znalost. Zvýšené postprandiální glykemie jsou rizikem rozvoje aterosklerotických komplikací. Cíle léčby však mají být vždy stanoveny individuálně se zřetelem ke stavu pacienta a k přítomnosti přidružených nemocí. Inzulin se přidává k monoterapii či ke kombinaci PAD, ale zpravidla se léčba inzulinem doporučuje tehdy, pokud neuspěje podávání dvojkombinace PAD. Při nepřítomnosti kontraindikací se kombinuje inzulin s metforminem. Přitom se volí některý z konvenčních nebo intenzifikovaných režimů, včetně inzulinové pumpy.
Volba skupiny PAD
Biguanidy – metformin
V současné době je jediným biguanidem užívaným v klinické praxi metformin. Metformin je dnes považován u diabetiků 2. typu za antidiabetikum první volby, které je vhodné i pro pacienty s prediabetem [10]. Podle standardů Americké diabetologické asociace [11, 12] je doporučován i pacientům s porušenou glukózovou tolerancí nebo se zvýšenou glykemií nalačno – pokud mají další alespoň jeden rizikový faktor (věk nižší než 60 let, body mass index – BMI ≥ 35, rodinná anamnéza DM u příbuzných prvního stupně, zvýšená hladina triglyceridů, snížená koncentrace HDL cholesterolu, hypertenze, HbA1c > 6,0 %). Kardiovaskulární riziko je totiž u osob s prediabetem stejné jako u diabetiků, ani onkologické riziko není zanedbatelné (zejména u mužů). U nemocných s DM 2. typu pak metformin používáme nejen jako antidiabetikum první volby, ale zároveň také ve všech dalších kombinacích podle Nathanova schématu (obr. 1). Hypoglykemizující účinek a zlepšení utilizace glukózy při léčbě metforminem nejsou stále zcela objasněny, ale nejpravděpodobnějším vysvětlením se zdá být ovlivnění inzulinové rezistence na úrovni jater, snížení produkce glukózy játry a možné omezení vstřebávání glukózy střevem. Metformin samotný nezvyšuje sekreci inzulinu, a proto nevyvolává hypoglykemie.
Kromě významného antidiabetického efektu jsou významné i další systémové účinky metforminu [13, 14]:
- snížení výskytu nádorů,
- pozitivní kardiovaskulární účinky,
- redukce hmotnosti a obvodu pasu,
- pravděpodobnost snížení výskytu pankreatitidy při inkretinové léčbě,
- pozitivní ovlivnění jaterní steatózy
- stimulace imunity,
- anabolický efekt na kost,
- účinky na ovulaci a syndrom polycystických ovarií.
Velmi důležité použití metforminu je také tam, kde pravděpodobně tlumí nežádoucí účinky antidiabetik. To je při podání společně s inzulinem a inzulinovými sekretagogy, kdy metformin normalizuje zvýšené nádorové riziko, a u pacientů léčených léky na inkretinovém principu, kde se zdá, že může snižovat riziko pankreatitidy. Protože diabetici mají zvýšené kardiovaskulární riziko, je vhodné stále připomínat pozitivní kardiovaskulární účinky metforminu. Toto doporučení vychází zejména ze studie Diabetes prevention program (DPP) [15], kde bylo prokázáno, že metformin má jak efekt na prevenci diabetu, tak další pozitivní kardiovaskulární účinky. Metformin snižuje kardiovaskulární riziko, jak se prokázalo v řadě studií. Ve studii UKPDS snížil metformin riziko vzniku infarktu myokardu více než jiné léky při srovnatelném účinku na glykemii [16, 17]. Efekt na snížení progrese aterosklerózy karotid byl prokázán i u nediabetiků. Ve studii, která trvala dva roky, došlo při podávání metforminu v dávce 500–850 mg/den ke snížení progrese intimomediální tloušťky na karotidách. Tento efekt nesouvisel s poklesem glykemie [18].
Léčba metforminem byla u nás i v dalších zemích kontraindikována u pacientů s chronickým srdečním selháním a dalšími stavy s rizikem hypoxie. Dnes však existuje řada studií, které ukazují, že podání metforminu u srdečního selhání I. a II. stupně je velmi výhodné. Dokonce mortalita na chronické srdeční selhání je za léčby metforminem až o 50 % nižší než při léčbě sulfonylureou a výrazně klesá i počet opakovaných hospitalizací [13]. Metformin významně snižuje mortalitu kardiaků za hospitalizace i v ambulantní péči [19, 20]. Ve studii UKPDS došlo u diabetiků 2. typu k nejmenšímu vzestupu hmotnosti ze všech užívaných antidiabetik právě po léčbě metforminem. Ve studii DPP [14] zaměřené na prevenci diabetu došlo u pacientů s prediabetem léčených metforminem k redukci hmotnosti.
Terapie se u diabetiků 2. typu zahajuje nejnižší dávkou metforminu (500 mg) podanou jednou až dvakrát denně s postupným navýšením dle snášenlivosti pacienta. Chronická udržovací dávka obvykle nepřekračuje 2000 mg denně. Maximální doporučovaná dávka je 3000 mg denně. Při podávání metforminu s prodlouženým účinkem, jehož výhodou je dávkování v jedné večerní dávce a menší nežádoucí účinky, je maximální denní dávka 2000 mg.
Při terapii metforminem je nutné pravidelně kontrolovat renální funkce, používání je bezpečné, pokud glomerulární filtrace (GF) neklesne pod 30 ml/min a nebo hladina sérového kreatininu nevystoupí nad 130 μmol/l. Při plánovaném vyšetření radiokontrastními látkami, v rámci rentgenologického vyšetření, před vyšetřením počítačovou tomografií a magnetickou rezonancí je vhodné léčbu metforminem přerušit v den vyšetření a následujících 48 hodin po výkonu. Po vyšetření je nutné monitorovat renální funkce a zajistit dostatečnou hydrataci pacienta. Kontraindikací léčby biguanidy je gravidita a laktace, přecitlivělost na biguanidy, laktátová acidóza nebo stavy, které zvyšují riziko jejího vzniku. Dále je tato léčba kontraindikována při těžkých a akutních stavech, těžší poruše jaterní funkce a stavech s rizikem lokální nebo celkové hypoxie, jako jsou akutní infarkt myokardu, kardiální insuficience, těžké plicní onemocnění. Uvažuje se o prospěšnosti léčby metforminem u DM 1. typu s obezitou, známkami metabolického syndromu a inzulinovou rezistencí, u nichž by mohl pomoci snížit velkou denní dávku inzulinu.
K nežádoucím účinkům řadíme gastrointestinální účinky metforminu nebo zhoršení renálních funkcí. Opakovaně existují obavy z hepatotoxicity. Nicméně se prokázalo, že pacienti se steatózou jater mají z léčby metforminem výrazný prospěch. Tito pacienti mají často mírnou elevaci hodnot jaterních testů a lékaři se obávají metformin podávat. Je zajímavé, že u prediabetiků snižují obsah tuků v játrech glitazony, ale nikoliv metformin [21].
Pokud se při monoterapii metforminem nedosáhne cílových hodnot kompenzace, je vhodné přidat další antidiabetikum s odlišným mechanismem účinku, a to opět zahájení léčby v co nejnižší dávce.
Inzulinová sekretagoga
Do této skupiny patří léky stimulující sekreci inzulinu – deriváty sulfonylurey a glinidy.
Deriváty sulfonylurey jsou používány v klinické praxi již několik desítek let. Účinné jsou u diabetiků 2. typu se zachovanou reziduální produkcí inzulinu. V současné době se léčí výhradně léčivy 2. generace, která mají kratší dobu účinku, nižší riziko hypoglykemie a méně lékových interakcí. Deriváty sulfonylurey snižují lačnou i post-
prandiální glykemii. K dosažení lepší kompenzace diabetu v kombinaci s metforminem se doporučuje zejména gliklazid nebo glimepirid v nejnižší dávce a při nedostačující kompenzaci po několika týdnech je možno zvýšit na průměrnou denní dávku. Při chronické monoterapii se nedoporučuje překračovat střední dávky PAD (gliklazid 160 mg a pro MR formu 60–120 mg, glimepirid 2–4 mg, glipizid 10 mg). U nemocných s chronickou renální insuficiencí je možno podávat glikvidon. Při glykemiích nad 15 mmol/l nelze očekávat významnější efekt této skupiny léků, a další zvyšování dávek proto není vhodné. Z kardiovaskulárního hlediska se zdají být výhodné svojí selektivní vazbou na β-buňky pankreatu zejména gliklazid a glimepirid. Naopak glibenklamid a glipizid se váží kromě β-buněk pankreatu též na myokard. V porovnání s biguanidy dochází při léčbě deriváty sulfonylurey k vzestupu tělesné hmotnosti. Hypoglykemie jsou častým nepříjemným nežádoucím účinkem. Předmětem diskusí je kardiovaskulární mortalita.
Nesulfonylureová sekretagoga (glinidy) lze alternativně použít místo derivátů sulfonylurey v kombinaci s metforminem a u pacientů se zachovalou sekrecí inzulinu. Používají se těsně před jídlem k ovlivnění postprandiální glykemie. Ke klinickému použití jsou zaregistrovány repaglinid a nateglinid, v ČR pouze repaglinid. Jejich účinek je krátký a rychlý.
Glitazony
Thiazolidindiony (glitazony) se používají ke kombinované léčbě u pacientů s DM 2. typu s vyjádřenou inzulinovou rezistencí. Indikovány jsou v kombinaci se sulfonylureou, kde nelze použít metformin pro jeho nesnášenlivost, jinak v kombinaci s metforminem, kde monoterapie tímto léčivem nedosáhla požadované kompenzace diabetu, přičemž přetrvává neuspokojivá kompenzace a současně hrozí zvýšené riziko vzniku kardiovaskulárních onemocnění (arteriální hypertenze, dyslipidemie a zvýšená albuminurie – s hodnotou nad 20 μmol/min).
Pioglitazon lze výhodně kombinovat s inkretiny, a to jak s blokátory dipeptidylpeptidázy 4 (DPP-4), tak se subkutánně aplikovanými inkretinovými mimetiky. Je doporučen i pro trojkombinaci s metforminem a deriváty sulfonylurey při nedostatečné kompenzaci léčbou dvojkombinací PAD. Pioglitazon je možno použít i v kombinaci s inzulinem. Podávání této kombinace může vést u rizikových pacientů ke vzniku otoků, při vystupňování retence až ke kardiálnímu selhávání. Používá se úvodní dávka 15 mg pioglitazonu. U těchto pacientů musejí být současně respektovány kontraindikace léčby glitazony (chronické srdeční selhání funkční třídy III–IV dle NYHA, u pacientů s anamnézou srdeční ischemie a s ischemickou chorobou srdeční [22], u edémových stavů, těhotenství, poškození jater). V průběhu léčby je třeba kontrolovat klinický stav pacienta se zřetelem na retenci tekutin, včetně známek oběhového selhání. Thiazolidindiony podporují redistribuci tuku z centrální do periferní lokalizace. V souvislosti s touto redistribucí tukové tkáně může dojít ke vzestupu tělesné hmotnosti o 2–4 kg. U žen léčených thiazolidindiony existuje vyšší riziko fraktur na podkladě osteoporózy. V roce 2010 došlo v důsledku zvýšeného rizika kardiovaskulárních komplikací ke stažení rosiglitazonu z klinického používání v Evropě a k jeho téměř úplnému zákazu i v USA. Potenciální riziko, které tato léčba přinášela nemocným, celkově převažovalo nad jejím
přínosem.
Při léčbě DM 2. typu lze rovněž použít kombinované přípravky PAD (např. kombinaci metforminu se sulfonylureou, metformin s pioglitazonem nebo metformin s gliptinem).
Léky ovlivňující GLP-1 receptorovou signalizaci
Tyto léky jsou též označovány jako inkretiny; tzv inkretinový efekt byl popsán jako rozdíl ve stimulaci sekrece inzulinu při podání glukózy per os a intravenózně. Při udržení stejných hodnot glykemie byla při perorálním podání glukózy sekrece inzulinu vyšší než po aplikaci stejné dávky intravenózně. Rozdíl je pak důsledkem aktivace inkretinového systému perorálním příjmem. K přirozeným inkretinům, důležitým u DM 2. typu, patří GLP-1 (glucagon-like peptide 1, glukagonu podobný peptid 1) a GIP (glukózodependentní inzulinotropní peptid). Jsou to peptidy, které se uvolňují z trávicího traktu jako odpověď na podání potravy. Léky s inkretinovým působením zahrnují jednak inkretinová mimetika, jednak gliptiny (inhibitory DPP-4). Používají se v kombinační terapii s metforminem a glitazony, pokud není dosaženo uspokojivé kompenzace. Podmínkou jejich účinného působení je zachovaná sekrece inzulinu, kterou v přítomnosti glukózy stimulují.
Prvním dostupným agonistou GLP-1 receptorů byl exenatid, syntetická verze peptidu izolovaného ve slinách ještěra Gila monster. Výhodou léku je pokles tělesné hmotnosti způsobený sníženou chutí k jídlu. Exenatid prokázal dobrou klinickou účinnost a další vývoj inkretinových agonistů směřuje ke snížení rizika výskytu nežádoucích účinků a ke snížení počtu nutných parenterálních aplikací. Exenatid se aplikuje subkutánně v základní dávce od 5 µg do 10 µg dvakrát denně.
Liraglutid je analog humánního GLP-1, který se aplikuje jednou denně. Poměrně časté jsou nežádoucí účinky – nauzea, zvracení a jsou popsány případy akutní pankreatitidy.
Inhibitory DPP-4 (gliptiny) jsou určeny v prvé řadě k zintenzivnění léčby DM 2. typu. Tato léčiva inhibují enzym DPP-4 odbourávající inkretinové hormony a tím blokují jejich inaktivaci. Nepřímo tak modulují funkci α- i β-buněk a sekreci inzulinu i glukagonu bez rizika hypoglykemie a vzestupu hmotnosti. Patří sem sitagliptin, vildagliptin, saxagliptin, linagliptin a alogliptin (u nás zatím nedostupný). Tyto léky se používají v kombinaci s dalšími PAD u DM 2. typu. V budoucnu lze očekávat průkaz příznivých účinků na kardiovaskulární systém. Ovlivňují glykemii nalačno i postprandiální glykemii. Gliptiny jsou dostupné v tabletové formě a jsou k dispozici i ve fixní kombinaci
s metforminem.
Inhibitory α-glukosidáz
Inhibitory α-glukosidáz (akarbóza, miglitol) se mohou použít ke zlepšení kompenzace u jedinců s vysokým postprandiálním vzestupem glykemií, případně v kombinaci s jiným antidiabetikem, a to v dávce obvykle do 200 mg denně. Tyto léky snižují postprandiální hyperglykemii zpomalením absorpce glukózy v zažívacím traktu. Neovlivňují utilizaci glukózy ani sekreci inzulinu. Podávají se těsně před jídlem. Na našem trhu je pouze akarbóza, která se má podávat na začátku léčby v nízké dávce 50 mg 3krát denně s hlavními jídly. Při dobré toleranci je možné dávku zvyšovat v odstupu alespoň 14 dnů až na maximální dávku, tj. 3krát 300 mg. Nevýhodou jsou časté vedlejší účinky – průjem, flatulence, nadýmání. Kontraindikovány jsou u pacientů s nespecifickými střevními záněty, gastroparézou, středně těžkou a těžkou renální insuficiencí [23].
Inzulinoterapie
V případě, že léčba PAD nebo jejich kombinací nevede k uspokojivým výsledkům nebo je kontraindikována, je třeba zahájit léčbu inzulinem. Také zde platí doporučení volby co nejnižší účinné dávky inzulinu. Obvykle se začíná se středně dlouze působícím přípravkem aplikovaným na noc nebo s dlouhodobě působícím analogem (zejména při vysoké glykemii nalačno), který se často kombinuje s metforminem. Pokud se nedosahuje požadované kompenzace, použijí se krátce působící inzuliny (včetně analog) podané před hlavními jídly, a to především v případě, kdy je zjištěna vysoká postprandiální glykemie. Intenzifikovaná léčba inzulinem včetně léčby inzulinovými analogy by měla vést k co nejlepší kompenzaci diabetu při minimalizaci celkové dávky inzulinu. U části pacientů lze použít premixované inzuliny (včetně analog), nelépe v podání 3krát denně před jídlem napodobujícím inzulinovou sekreci. Není-li dosaženo požadované kompenzace lidským inzulinem, je vhodné využít vlastností inzulinových analog. Při vyšších glykemiích (většinou nad 15 mmol/l) prokázaných při stanovení diagnózy diabetu může být inzulin použit dočasně ke zlepšení kompenzace již na začátku terapie s následným převedením pacienta na léčbu PAD. Zahájení léčby inzulinem, určení formy a zvolení druhu přípravku má provádět diabetolog.
U starších nebo polymorbidních jedinců je nezbytné respektovat kontraindikace PAD s obzvláštní důsledností. Nezbytnou součástí úspěšné léčby DM 2. typu je edukace nemocných s upevňováním návyků nefarmakologické
léčby.
Závěr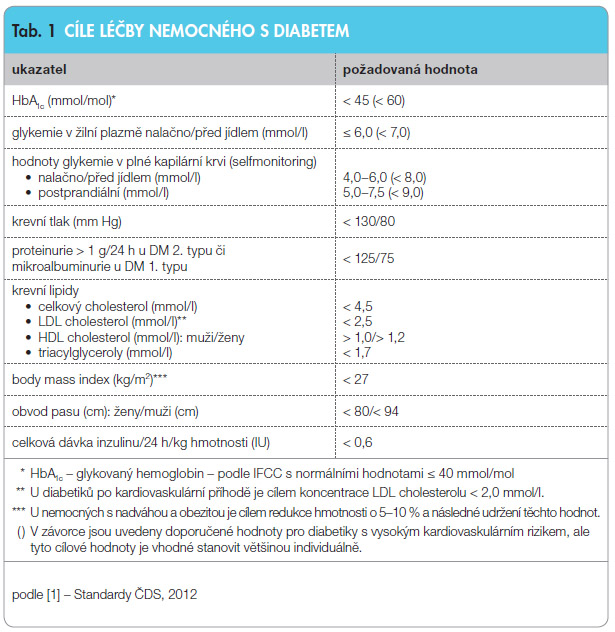
Při diagnóze prediabetu i diabetu je vhodné časné navození normoglykemie – vede totiž k obnově funkce B-buněk a často i k remisi diabetu či prediabetu, čímž je sníženo zejména kardiovaskulární riziko i mortalita. Proto je vhodné neodkládat léčbu a dosahovat v těchto situacích léčebných cílů určených pro nově zjištěné diabetiky. Součástí léčby DM 2. typu má být úspěšné zvládnutí hyperglykemie, obezity, hypertenze, dyslipidemie, zvýšené tendence k agregaci trombocytů a akutních a chronických komplikací diabetu [1] (tab. 1).
Seznam použité literatury
- [1] Standardy péče o diabetes mellitus 2. typu. Standardy České diabetologické společnosti. 2012 (www.diab.cz).
- [2] Haluzík M. Využití moderní diabetologické léčby v ordinaci interního lékaře. Acta medicinae 2012; 5: 8–10.
- [3] Pelikánová T. Léčba diabetu při metabolickém syndromu. Vnitř Lék 2009; 55: 637–645.
- [4] Pelikánová T, Bartoš V a kol. Praktická diabetologie. Praha, Maxdorf 2010, 4. vydání, 743 s.
- [5] Rosolová H, Petrlová B, Šimon J, et al. Makrovaskulární a mikrovaskulární komplikace u diabetiků 2. typu. Vnitř Lék 2008; 54: 229–237.
- [6] Škrha J. Diabetologie. Praha, Galén 2009, 417 s.
- [7] Diabetes Prevention Program. Repeat glucose testing to confirm glucose tolerance status: implications for diagnosing diabetes in high risk adults. Diabetes 2006; 55 (Suppl 1): 894P.
- [8] Tuomilehto J, Lindström J, Ericsson JG, et al. Finnish Diabetes Prevention Study Group. Prevention of type 2 diabetes mellitus by changes in lifestyle among subjects with impaired glucose tolerance. N Engl J Med 2001; 344: 1343–1350.
- [9] Karen I a kol. Prediabetes. Doporučený postup pro praktické lékaře. Praha: SVL ČLS, 2012.
- [10] Perušičová J a kol. Prediabetes, prehypertenze, dyslipidemie a metabolický syndrom. Praha, Maxdorf 2012. 315 s.
- [12] American Diabetes Association Standards of Medical Care in Diabetes – 2012. Diabetes Care 2012; 35: S11–S63.
- [13] Svačina Š. Systémové účinky metforminu. Postgrad Med 2010; 12: 42–45.
- [14] Svačina Š. Postavení metforminu jako antidiabetika první volby. Vnitř Lék 2010; 56: 1225–1227.
- [15] DPP (Diabetes Prevention Program) Role of insulin secretion and sensitivity in the evolution of type 2 diabetes in the diabetes prevention program: effects of lifestyle intervention and metformin. Diabetes 2005; 54: 2404–2414.
- [16] UKPDS (The United Kingdom Prospective Diabetes Study) Holman RR, Paul SK, Betel MA et al. Long-term follow-up after tight control of blood pressure in type 2 diabetes. N Engl J Med 2008; 359: 1565–1576.
- [17] Holman RR, Paul SK, Betel MA, et al. 10-years follow-up of intensive glucose control in type 2 diabetes. N Engl J Med 2008; 359: 1577–1589.
- [18] Matsumoto K, Sera Y, Abe Y et al. Metformin attenuates progression of carotid arterial wall thickness in patients with type 2 diabetes. Diabetes Res Clin Pract 2004; 64: 225–228.
- [19] Anderson C, Olesen JB, Hansen PR, et al. Metformin treatment is associated with a low risk of mortality in diabetic patients with heart failure: a retrospective nation-wide cohort study. Diabetologia 2010; 53: 2546–2553.
- [20] Evans JM, Doney AS, AlZadjali MA, et al. Effect of Metformin on mortality in patients with heart failure and type 2 diabetes mellites. Am J Cardiol 2010; 106: 1006–1010.
- [21] Levri KM, Slaymaker E, Last A, et al. Metformin as treatment for overweight and obese adults: a systematic review. Ann Fam Med 2005; 3: 457–461.
- [22] Nesto RW, Bell D, Bonow RO, et al. Thiazolidinedione use, fluid retention, and congestive heart failure: a consensus statement from the American Heart Association and American Diabetes Association. Circulation 2003; 108: 2941–2948.
- [23] Svačina Š, Šmahelová A, Haluzík M. Perorální antidiabetika. In: Škrha J, et al. Diabetologie. Praha, Galén 2009: 298–324.