HPV infekce není rizikem jen pro ženy
Infekce lidskými papilomaviry způsobuje onemocnění nejen u žen, ale také u mužů. Je příčinou genitálních bradavic, rekurentní respirační papilomatózy a karcinomu penisu. Významně se podílí na rozvoji karcinomu řiti a nádorů oblasti hlavy a krku. Nejnovější data ukazují, že očkování chlapců a mužů kvadrivalentní vakcínou je užitečné v prevenci nemocí spojených s lidskými papilomaviry.
Úvod
Lidský papilomavirus (human papillomavirus, HPV) byl objeven v roce 1907. Od té doby uplynulo přes půl století, než v letech 1974–1984 německý virolog Harald zur Hausen prokázal kauzální spojení mezi HPV infekcí a karcinomem hrdla děložního, za což v roce 2008 získal Nobelovu cenu. Znalost zmíněné kauzální souvislosti byla podkladem nejen k vývoji vakcín proti HPV, které byly v roce 2006 (kvadrivalentní vakcína) a 2007 (bivalentní vakcína) uvedeny do klinického užívání, ale i k doporučení WHO, aby případný nově zakládaný screening karcinomu hrdla děložního byl opřen o detekci přítomnosti HPV.
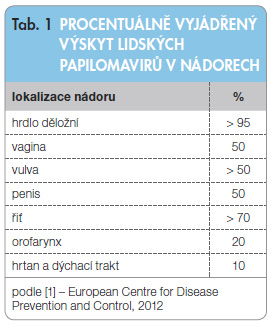 Genitální typy HPV se dle svého onkogenního potenciálu dělí na vysoce rizikové a nízkorizikové. Vysoce rizikové typy (high risk, HR) jsou druhým nejvýznamnějším známým lidským kancerogenem po tabákovém kouři. Ve vysokém procentu je nacházíme i v dalších nádorech, a to nejen u žen (tab. 1).
Genitální typy HPV se dle svého onkogenního potenciálu dělí na vysoce rizikové a nízkorizikové. Vysoce rizikové typy (high risk, HR) jsou druhým nejvýznamnějším známým lidským kancerogenem po tabákovém kouři. Ve vysokém procentu je nacházíme i v dalších nádorech, a to nejen u žen (tab. 1).
Muži nejsou pouze přenašeči této nejčastější pohlavně přenosné infekce, ale i její obětí. Nízkorizikové typy (low risk, LR) stejnou měrou postihují muže i ženy s celkem 30 miliony případů výskytu genitálních bradavic ročně a způsobují také rekurentní respirační papilomatózu. HR typy stojí ročně za jedenácti tisíci případy karcinomů penisu a významně se podílejí i na vzniku karcinomů řiti a karcinomů hlavy a krku [1].
Genitální bradavice
Genitální bradavice (kondylomata) jsou ve více než 90 % způsobovány LR HPV typu 6 a 11. Jejich prevalence v populaci se pohybuje kolem 1 % a trvale mírně roste [2, 3]. Přestože se jedná o benigní onemocnění, má významný vliv na kvalitu života pacientů kvůli značné tendenci k rekurenci. Náklady na léčbu genitálních bradavic [4] jsou považovány za jeden z důvodů změny zvolené vakcíny; v plošném očkování proti HPV ve Velké Británii byla v roce 2012 změněna vakcína bivalentní na kvadrivalentní.
![Graf 1 Vývoj incidence genitálních bradavic dle výzkumu v Melbourne Sexual Health Centre; podle [7] – Gertig , et al., 2011.](https://www.remedia.cz/photo-a-29214---.jpg) Kvadrivalentní vakcína je určena k aplikaci dívkám a ženám ve věku 9–45 let a chlapcům a mužům ve věku 9–26 let. Při dodržení očkovacího protokolu vykazuje 100% účinnost (95% CI: 92–100) proti kondylomatům způsobeným typy HPV 6 a 11 v HPV-naivní populaci (jedinci, kteří se dosud s HPV infekcí nesetkali) a 76% účinnost (95% CI: 61–86) v běžné populaci [5].
Kvadrivalentní vakcína je určena k aplikaci dívkám a ženám ve věku 9–45 let a chlapcům a mužům ve věku 9–26 let. Při dodržení očkovacího protokolu vykazuje 100% účinnost (95% CI: 92–100) proti kondylomatům způsobeným typy HPV 6 a 11 v HPV-naivní populaci (jedinci, kteří se dosud s HPV infekcí nesetkali) a 76% účinnost (95% CI: 61–86) v běžné populaci [5].
Při dostatečném pokrytí cílové populace dívek je toto očkování samozřejmě přínosem i pro heterosexuální muže, jak ukazují data z Austrálie [6]. V Austrálii byl v roce 2007 zahájen školní očkovací program pro dívky ve věku 12–13 let, do konce roku 2009 se mohly zdarma očkovat kvadrivalentní vakcínou také dívky ve věku 13–18 let a v komunitním systému i ženy ve věku 18–26 let. Bylo 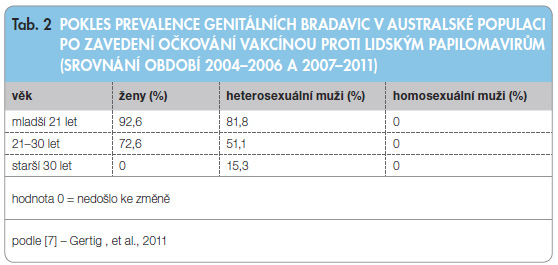 dosaženo pokrytí 83 % cílové populace. Již po roce od zahájení očkování byl zaznamenán významný pokles případů výskytu genitálních bradavic nejen u dívek, ale i u heterosexuálních mužů (graf 1), vedoucí až k praktickému vymizení genitálních bradavic u očkovaných žen po třech letech od zahájení očkování (tab. 2) [7].
dosaženo pokrytí 83 % cílové populace. Již po roce od zahájení očkování byl zaznamenán významný pokles případů výskytu genitálních bradavic nejen u dívek, ale i u heterosexuálních mužů (graf 1), vedoucí až k praktickému vymizení genitálních bradavic u očkovaných žen po třech letech od zahájení očkování (tab. 2) [7].
Rekurentní respirační papilomatóza
Benigní papilomy dýchacích cest ve formě rekurentní respirační papilomatózy (RRP) jsou prakticky ve 100 % případů spojovány s infekcí HPV typu 6 a 11. Za důsledek peripartální a perinatální infekce je považována juvenilní forma (juvenilie-onset recurrent respiratory papillomatosis, JORP) s maximem výskytu u dětí ve věku 2–4 roky s incidencí 4,3 případu na 100 000; druhý vrchol výskytu, který je spojován s infekcí při orálním sexu, nacházíme u dospělé formy (adult-onset recurrent respiratory papillomatosis, AORRP) u jedinců ve věku 20–40 let [8]. U dětí se onemocnění projevuje stridorem, dušností, poruchami polykání a kašlem, u dospělých dominuje chrapot. Léčbou volby je chirurgické odstranění. Adjuvantně jsou podávána antivirotika a interferony. Tendence k rekurenci je vysoká.
Vzhledem k neuspokojivému spektru léčby doporučují někteří autoři očkování proti HPV 6 a 11 v prevenci RRP, a to i po ošetření lézí [9].
Nádory hlavy a krku
V těchto nádorech sice představuje zastoupení HPV, zejména typu 16, již jen asi 20 %, přesto však je očkování proti HPV jednou z mála možných cest primární prevence. Ostatně recentní studie prokazují přítomnost HPV v daleko vyšším procentu. Incidence nádorů hlavy a krku u mužů je 19 případů na 100 000, zatímco u žen představuje tento poměr jen 6/100 000. Nejčastěji se vyskytují nádory hlasivek (25 %) a tonzil (10 %).
Vysoký počet sexuálních partnerů pro sex vaginální (26 a více, odds ratio – OR = 3,1) i orální (více než 6, OR = 3,4) významně zvyšuje riziko orofaryngeálních karcinomů (p = 0,002, resp. 0,009). Infekce HPV typu 16 ve spojení s kouřením a abúzem alkoholu zvyšuje přidané riziko na 19,4 (OR = 19,4), nicméně tyto faktory se jeví jako nezávislé [10]. Prevalence HPV v orální oblasti je vyšší u mužů než u žen a stále se zvyšuje [11].
Karcinom penisu
Incidence karcinomu penisu je nižší než 1 na 100 000 mužů a z toho 47 % případů je HPV pozitivních. Tvoří tak 0,5 % karcinomů v mužské populaci.
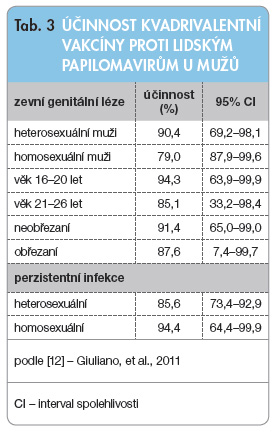 Ve dvojitě slepé randomizované intervenční studii týkající se účinnosti kvadrivalentní HPV vakcíny bylo během 2,9 roku sledováno 4065 zdravých mužů ve věku 16–26 let. V tzv. intention-to-treat (ITT) populaci bylo zjištěno 36 výskytů genitálních lézí (genitální bradavice, penilní intraepiteliální neoplazie – PIN) v očkované skupině a 89 výskytů ve skupině léčené placebem, což ukazuje na snížení o 60,2 % (95% CI: 40,8–73,8), při sledování lézí způsobených očkovacími typy HPV dokonce o 65,5 % (95% CI: 45,8–78,6). V populaci léčené per protocol (per-protocol efficacy, PPE), tedy v populaci HPV naivní, bylo zjištěno 6 lézí v očkované skupině a 36 lézí ve skupině léčené placebem, což znamená účinnost 90,4 % (95% CI: 69,2–98,1). Záleží však také na sexuální orientaci probandů (tab. 3). V PPE populaci nebyla zaznamenána žádná PIN jako přednádorová léze penisu, ale ve skupině léčené placebem se vyskytly tři případy. To jsou příliš malá čísla k ověření signifikantní ochrany [12].
Ve dvojitě slepé randomizované intervenční studii týkající se účinnosti kvadrivalentní HPV vakcíny bylo během 2,9 roku sledováno 4065 zdravých mužů ve věku 16–26 let. V tzv. intention-to-treat (ITT) populaci bylo zjištěno 36 výskytů genitálních lézí (genitální bradavice, penilní intraepiteliální neoplazie – PIN) v očkované skupině a 89 výskytů ve skupině léčené placebem, což ukazuje na snížení o 60,2 % (95% CI: 40,8–73,8), při sledování lézí způsobených očkovacími typy HPV dokonce o 65,5 % (95% CI: 45,8–78,6). V populaci léčené per protocol (per-protocol efficacy, PPE), tedy v populaci HPV naivní, bylo zjištěno 6 lézí v očkované skupině a 36 lézí ve skupině léčené placebem, což znamená účinnost 90,4 % (95% CI: 69,2–98,1). Záleží však také na sexuální orientaci probandů (tab. 3). V PPE populaci nebyla zaznamenána žádná PIN jako přednádorová léze penisu, ale ve skupině léčené placebem se vyskytly tři případy. To jsou příliš malá čísla k ověření signifikantní ochrany [12].
Anální karcinom
Incidence análního karcinomu (karcinomu řiti) je v populaci 1,2 na 100 000. V 71 % je tento karcinom spojen s HPV infekcí. Výskyt neznamená automaticky anamnézu análního styku, faktem ale zůstává, že tato sexuální praktika, vzhledem ke snadné zranitelnosti sliznice anu – vstupní brány infekce – při této aktivitě, významně zvyšuje riziko nákazy HPV. U homosexuálních mužů je incidence 5,1/100 000 a u HIV pozitivních homosexuálních mužů dokonce 45,9/100 000. Prekurzorem análního karcinomu je anální intraepiteliální neoplazie (AIN).
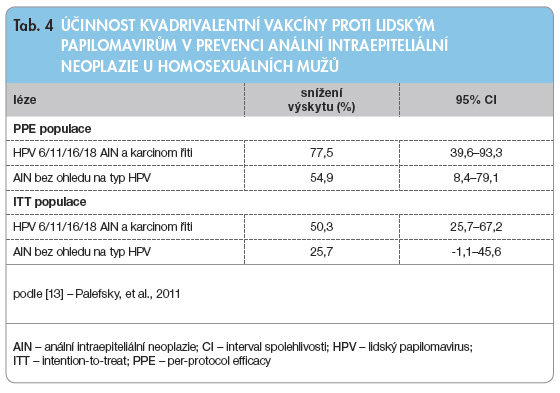 V podskupině výše uvedené studie účinnosti kvadrivalentní vakcíny u mužů bylo sledováno 602 homosexuálních mužů ve věku 16–26 let. Ochrana před perzistentní anální infekcí HPV typu 6, 11, 16 a 18 dosáhla 59,4 % (95% CI: 43,0–71,4) v ITT skupině, a dokonce 94,9 % (95% CI: 80,4–99,4) ve skupině léčené dle protokolu (tab. 4). Po dobu studie nebyla hlášena žádná zdravotní nežádoucí událost [13].
V podskupině výše uvedené studie účinnosti kvadrivalentní vakcíny u mužů bylo sledováno 602 homosexuálních mužů ve věku 16–26 let. Ochrana před perzistentní anální infekcí HPV typu 6, 11, 16 a 18 dosáhla 59,4 % (95% CI: 43,0–71,4) v ITT skupině, a dokonce 94,9 % (95% CI: 80,4–99,4) ve skupině léčené dle protokolu (tab. 4). Po dobu studie nebyla hlášena žádná zdravotní nežádoucí událost [13].
Závěr
Lze tedy shrnout, že také muži jsou ohroženi projevy HPV infekce. Očkování kvadrivalentní vakcínou významně snižuje výskyt těchto nemocí, jak bylo prokázáno u zevních genitálních lézí i análního karcinomu. Očkování by měli podstoupit zejména homosexuální muži. Nicméně z očkování mají přínos prakticky všichni chlapci a muži ve věku 9–26 let bez ohledu na sexuální orientaci. Vakcinace mužů je výrazným přínosem i pro jejich sexuální partnerky či partnery.
Seznam použité literatury
- [1] European Centre for Disease Prevention and Control: Introduction of HPV vaccines in EU countries – an update. Stockholm. ECDC 2012, 40 p.
- [2] Fait T, Dvořák V, Skřivánek A, et al. Epidemiologie genitálních bradavic mezi ženami v České republice. Čes Gynek 2012; 77: 360–363.
- [3] Fenton KA, Lowndes CM. Recent trends in the epidemiology of STI in the European Union. Sex Trans Infect 2004; 80: 255–263.
- [4] Desai S, Wetten S, Woodhall SC, et al. Genital warts and cost of care in England. SecTrans Infect 2011; 87: 464–468.
- [5] Garland SM, Hernandez-Avila M, Wheeler CM, et al. Quadrivalent Vaccine against Human Papillomavirus to Prevent Anogenital Disease. NEJM 2007; 356: 1928–1943.
- [6] Fairley CK, Hocking JS, Gurrin LC, et al. Rapid decline in presentation of genital warts after the implementation of a national quadrivalent human papillomavirus vaccination programme for young women. Sex Transm Infect 2009; 85: 499–502.
- [7] Gertig DM, Brotherton JM, Savile M. Measuring human papillomavirus (HPV) vaccination coverage and the role of the National HPV Vaccination Program Register, Australia. Sex Health 2011; 8: 171–178.
- [8] Gallagher TQ, Derkay CS. Recurrent respiratory papillomatosis. Curr Opin Otolaryngol Head Neck Surg 2008; 16: 645–655.
- [9] Dubová J, Vydrová J, Bendová O, et al. Výsledky vakcinace proti HPV u pacientů s rekurentní papilomatózou hrtanu. Postgrad Med 2012; 13: 921–923.
- [10] D´Sousa G, Kreimer A, Viscidi R, et al. Case-Control Study of Human Papillomavirus and Oropharyngeal Cancer. NEJM 2007; 356: 1944–1956.
- [11] Gillison ML, Broutian T, Pickard RK, et al. Prevalence of oral HPV infection in the United States, 2009–2010. JAMA 2012; 307: 693–703.
- [12] Giuliano AR, Palefsky JM, Goldstone S, et al. Efficacy of quadrivalent HPV vaccine against HPV Infection and disease in males. N Engl J Med 2011; 364: 401–411.
- [13] Palefsky JM, Giuiliano AR, Goldstone S, et al. HPV valine against anal HPV infection and anal intraepithelial neoplasia. N Engl J Med 2011; 365: 1567–1585.