Inhibitory ACE a antagonisté receptorů AT1 pro angiotenzin II (sartany) využitelné v rámci sekundární prevence kardiovaskulárních příhod, porovnání z
Článek shrnuje nejvýznamnější farmakologická a klinická data týkající se léčiv ovlivňujících systém renin-angiotenzin-aldosteron, která lze použít při sekundární prevenci kardiovaskulárních příhod. Příznivý vliv na prognózu nemocných byl prokázán velkými randomizovanými studiemi u ramiprilu, perindoprilu, trandolaprilu a telmisartanu.
Léčiva ovlivňující systém renin-angiotenzin-aldosteron (RAAS) patří v současné době k základním farmakoterapeutickým intervencím nejen u pacientů s hypertenzí či srdeční nedostatečností. Zejména u specifických skupin nemocných (pacienti s ischemickou chorobou srdeční, ischemickou chorobou dolních končetin, s diabetem mellitem provázeným orgánovými změnami nebo po prodělané cévní mozkové příhodě) náleží účinné látky ovlivňující RAAS k léčivům používaným k redukci mortality a morbidity, a to bez ohledu na jejich hodnoty krevního tlaku či případnou přítomnost srdeční nedostatečnosti nebo dysfunkce levé komory srdeční .
Spotřeba léčiv ovlivňujících RAAS je v ČR značná. V roce 2009 činila celková spotřeba léčiv ATC skupiny C09 (tj. léků ovlivňujících RAAS) ve finančním vyjádření 3 792 105 929 Kč a ve hmotných jednotkách dosáhla hodnoty 163,47 DDD/1000 obyvatel a den [1]. Struktura této spotřeby ve hmotných 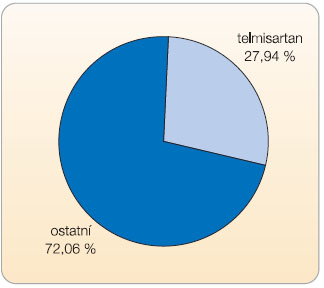 jednotkách byla v roce 2009 vcelku
jednotkách byla v roce 2009 vcelku 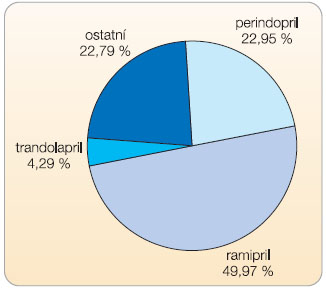 výmluvná: více než tři čtvrtiny spotřeby inhibitorů angiotenzin konvertujícího enzymu (ACE) tvořily léčivé přípravky obsahující tři léčivé látky – ramipril (49,97 %), perindopril (22,95 %) a trandolapril (4,29 %), viz graf 1 . Více než jednu čtvrtinu spotřeby antagonistů angiotenzinu na AT 1 -receptorech (tzv. sartanů) tvořil telmisartan (27,94 %), viz graf 2 .
výmluvná: více než tři čtvrtiny spotřeby inhibitorů angiotenzin konvertujícího enzymu (ACE) tvořily léčivé přípravky obsahující tři léčivé látky – ramipril (49,97 %), perindopril (22,95 %) a trandolapril (4,29 %), viz graf 1 . Více než jednu čtvrtinu spotřeby antagonistů angiotenzinu na AT 1 -receptorech (tzv. sartanů) tvořil telmisartan (27,94 %), viz graf 2 .
Důvodem výše uvedeného výsadního postavení zmíněných čtyř léčivých látek je s největší pravděpodobností jejich prokázaný příznivý vliv na prognózu nemocných v rámci sekundární prevence kardiovaskulárních příhod. Pozitivní vliv ramiprilu je velmi dobře doložen výsledky studie HOPE [2] (20% snížení IM, snížení počtu úmrtí o 22 % a CMP o 32 %), přínos perindoprilu dokumentují výsledky studie EUROPA [3] (23% snížení IM, 6% CMP, úmrtí o 14 %) či studie PROGRESS (v kombinaci s indapamidem, snížení počtu IM, CMP, úmrtí o 26 %), o příznivém účinku trandolaprilu vypovídají výsledky studie PEACE [4] (snížení počtu CMP o 24 % a úmrtí o 11 %) a dále výsledky studií INVEST a TRACE. Pozitivní vliv telmisartanu je pak opět velmi dobře doložen výsledky studie ONTARGET [5], v níž přímé srovnání telmisartanu a ramiprilu vedlo ke shodnému snížení výskytu sledovaných kardiovaskulárních příhod.
Skutečnost, že se jednotlivé inhibitory ACE liší v efektu léčby a v ovlivnění prognózy nemocných, byla dále dokumentována v retrospektivní kohortové studii, jejímž cílem bylo porovnat mortalitu starších pacientů ( ≥ 65 let), kteří byli hospitalizováni pro akutní infarkt myokardu (AIM) a byli léčeni inhibitory ACE [6]. Bylo sledováno celkem 18 ![Graf 3 Srovnání efektu ramiprilu s ostatními inhibitory angiotenzin konvertujícího enzymu na prognózu nemocných po infarktu myokardu; podle [6] – Pilote, et al., 2004.](https://www.remedia.cz/photo-a-27951---.jpg) 453 pacientů z kanadské provincie Quebec, přičemž hodnoceno bylo 7512 z nich; právě tito pacienti totiž naplnili kritérium terapie inhibitorem ACE trvající alespoň 1 rok, přičemž tato terapie byla zahájena do 30 dnů po ukončení hospitalizace. Mortalita pacientů léčených kaptoprilem, enalaprilem, fosinoprilem nebo quinaprilem byla statisticky významně vyšší než mortalita pacientů léčených ramiprilem (referenční lék) nebo perindoprilem ( graf 3 ). Výsledky této kohortové studie se staly předmětem polemiky a byly podrobeny kritice pro různé metodologické a další nedostatky (např. odlišná skladba komedikace pacientů léčených jednotlivými inhibitory ACE).
453 pacientů z kanadské provincie Quebec, přičemž hodnoceno bylo 7512 z nich; právě tito pacienti totiž naplnili kritérium terapie inhibitorem ACE trvající alespoň 1 rok, přičemž tato terapie byla zahájena do 30 dnů po ukončení hospitalizace. Mortalita pacientů léčených kaptoprilem, enalaprilem, fosinoprilem nebo quinaprilem byla statisticky významně vyšší než mortalita pacientů léčených ramiprilem (referenční lék) nebo perindoprilem ( graf 3 ). Výsledky této kohortové studie se staly předmětem polemiky a byly podrobeny kritice pro různé metodologické a další nedostatky (např. odlišná skladba komedikace pacientů léčených jednotlivými inhibitory ACE).
Stejná autorka následně publikovala další a rozsáhlejší studii [7]; zde bylo zařazeno 43 316 pacientů hospitalizovaných pro chronickou srdeční nedostatečnost, kteří byli léčeni inhibitory ACE alespoň 30 dnů před přijetím k hospitalizaci, ramipril opět sloužil jako referenční lék. I v tomto případě, při srovnávání neadjustovaných ![Graf 4 Srovnání efektu ramiprilu s ostatními inhibitory angiotenzin konvertujícího enzymu na prognózu nemocných se srdečním selháním (založeno na modelu fixní dávky); podle [7] – Pilote, et al., 2008.](https://www.remedia.cz/photo-a-27952---.jpg) hodnot, bylo relativní riziko pro kaptopril (1,13) i enalapril (1,10) zvýšeno. Z modelu, který byl založen na fixním modelu dávky, vyplývá, že až na perindopril a cilazapril byla léčba ostatními sledovanými inhibitory ACE spojena s horší prognózou (
hodnot, bylo relativní riziko pro kaptopril (1,13) i enalapril (1,10) zvýšeno. Z modelu, který byl založen na fixním modelu dávky, vyplývá, že až na perindopril a cilazapril byla léčba ostatními sledovanými inhibitory ACE spojena s horší prognózou (
graf 4 ). Vzestup mortality proti ramiprilu se pohyboval v rozmezí 10–60 %. Nedostatkem analýzy bylo, že v ní nebyly posuzovány další dlouhodobě účinkující inhibitory ACE – trandolapril, moexipril a spirapril (obdobně jako ve výše uvedené studii publikované v roce 2004); důvod je prostý, v době analýzy nebyly v Kanadě tyto léky užívány. Obě nezávislé analýzy tak docházejí ke stejnému závěru – existují významné rozdíly v účinku inhibitorů ACE. Výsledky druhé analýzy jsou cennější, neboť důkladná preskripční analýza nezjistila významné rozdíly mezi skupinami.
Obdobný prospektivní multicentrický registr pacientů po AIM ze SRN byl popsán ve studii MITRA PLUS [8]. Cílem bylo porovnat mortalitu pacientů léčených ramiprilem ve srovnání s pacienty léčenými jinými inhibitory ACE nebo s těmi, kteří inhibitory ACE léčeni nebyli. Bylo sledováno celkem 14 608 pacientů s AIM s ST elevací, z nichž 40,7 % užívalo ramipril, 39 % užívalo jiné inhibitory ACE a 56,3 % nebylo léčeno žádným inhibitorem ACE. Podávání ramiprilu bylo provázeno nejnižší hospitalizační mortalitou (relativní riziko 0,54 s 95% hladinou spolehlivosti 0,32–0,90), nejnižším výskytem závažných kardiovaskulárních příhod (relativní riziko 0,65 s 95% hladinou spolehlivosti 0,46–0,93), nikoli však snížením výskytu rozvoje srdeční nedostatečnosti při ukončení hospitalizace (relativní riziko 0,79 s 95% hladinou spolehlivosti 0,50–1,27), vše ve srovnání s podáváním jiných inhibitorů ACE.
Ve studii ONTARGET [5] byl porovnáván dopad léčby 80 mg telmisartanu či 10 mg ramiprilu přidaných ke stávající léčbě nebo kombinace obou léků na mortalitu a morbiditu. Ve studii byl sledován vliv telmisartanu a/nebo ramiprilu na pokles výskytu závažných kardiovaskulárních příhod, na 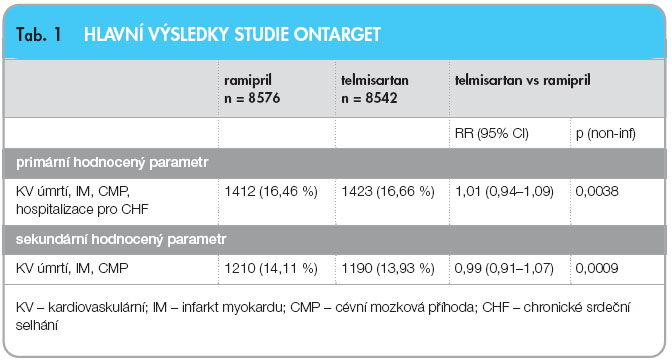 kardiovaskulární
kardiovaskulární 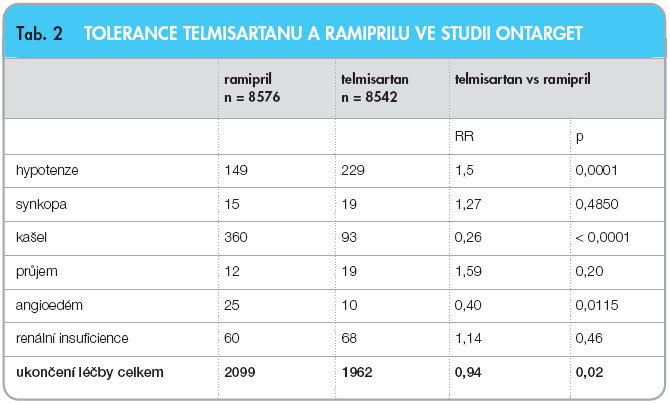 mortalitu, výskyt infarktu myokardu, iktu či na hospitalizaci pro srdeční selhání. Do studie ONTARGET bylo zařazeno více než 25 tisíc nemocných, medián sledování byl 56 měsíců. Nebyly zjištěny rozdíly ve výši krevního tlaku u pacientů léčených telmisartanem nebo ramiprilem. Při sledování primárního cíle (kardiovaskulární mortalita, výskyt infarktu myokardu, iktu či hospitalizace pro srdeční selhání) se jednotlivé větve nelišily, tedy léčba telmisartanem byla v sekundární prevenci stejně účinná jako léčba ramiprilem, kombinace obou léků (telmisartanu a ramiprilu), tedy duální blokáda systému RAA, nevedla k dalšímu snížení kardiovaskulární mortality či morbidity ( tab. 1 a 2 ).
mortalitu, výskyt infarktu myokardu, iktu či na hospitalizaci pro srdeční selhání. Do studie ONTARGET bylo zařazeno více než 25 tisíc nemocných, medián sledování byl 56 měsíců. Nebyly zjištěny rozdíly ve výši krevního tlaku u pacientů léčených telmisartanem nebo ramiprilem. Při sledování primárního cíle (kardiovaskulární mortalita, výskyt infarktu myokardu, iktu či hospitalizace pro srdeční selhání) se jednotlivé větve nelišily, tedy léčba telmisartanem byla v sekundární prevenci stejně účinná jako léčba ramiprilem, kombinace obou léků (telmisartanu a ramiprilu), tedy duální blokáda systému RAA, nevedla k dalšímu snížení kardiovaskulární mortality či morbidity ( tab. 1 a 2 ).
Je zřejmé, že v České republice, v podmínkách běžné klinické praxe, dávají lékaři přednost léčivým přípravkům, které redukují nejen hodnoty surrogate (jako je výše krevního tlaku), ale které zejména redukují riziko vzniku další kardiovaskulární příhody, případně upřednostňují léčivý přípravek, jehož podávání „respektuje“ metabolickou homeostázu a prakticky vždy přidružené komorbidity. Je jen škoda, že si tyto skutečnosti ne zcela uvědomuje regulátor tuzemských úhrad – Státní ústav pro kontrolu léčiv a Ministerstvo zdravotnictví ČR.
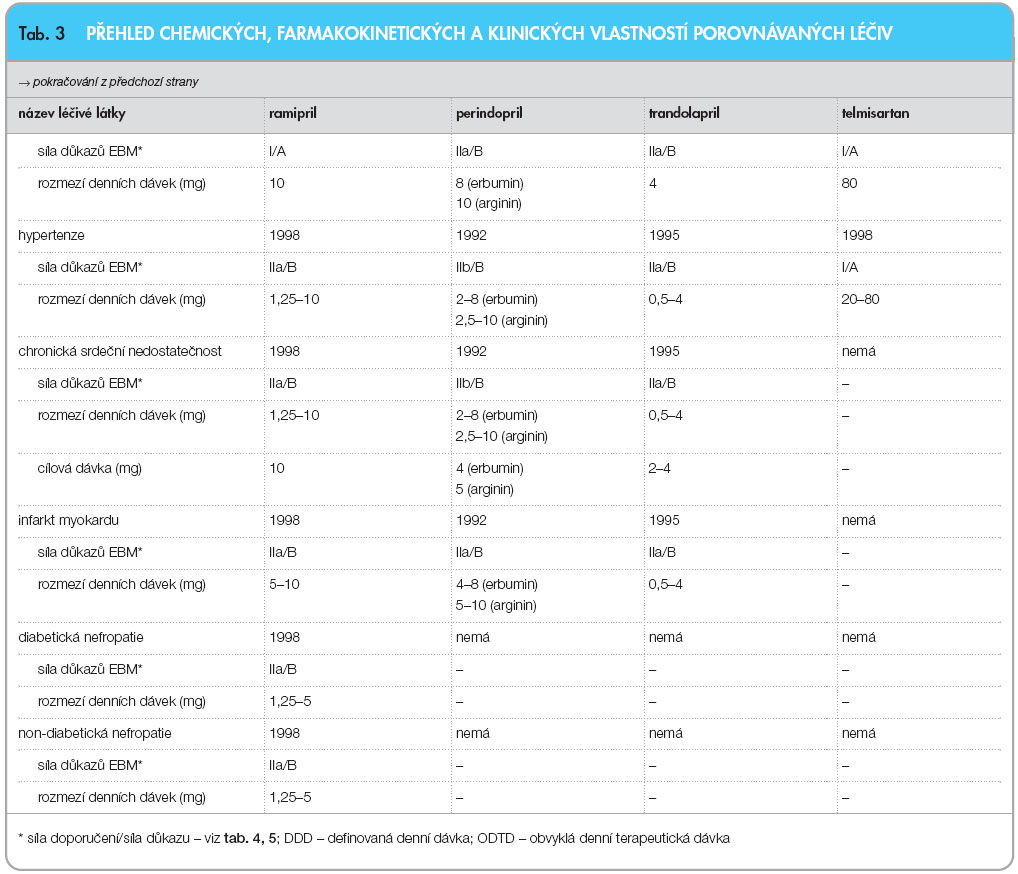
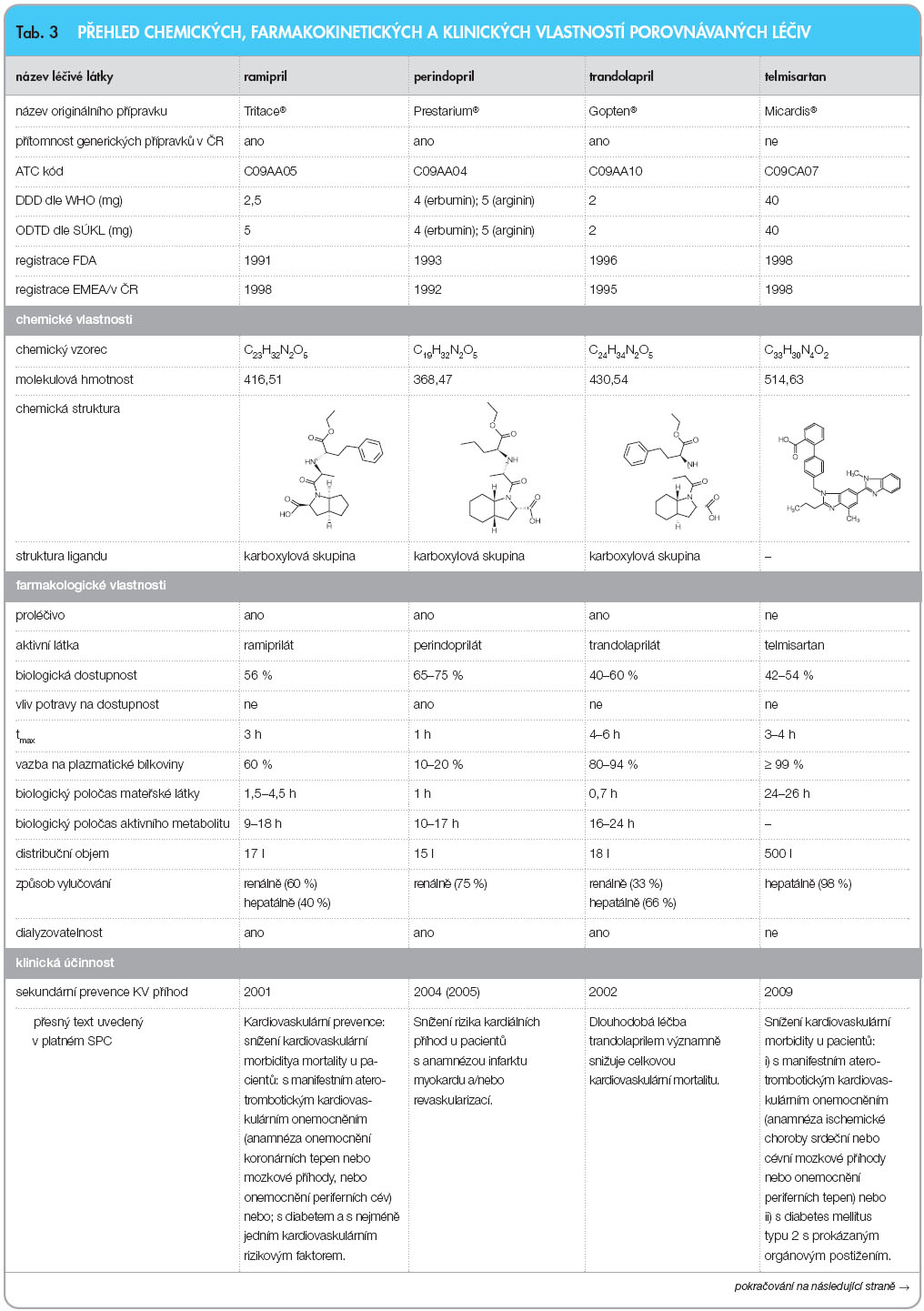 Předkládaný přehled, uvedený v tab. 3 , se snaží hutnou formou uvést nejvýznamnější farmakokinetická a klinická data týkající se těch léčiv ovlivňujících systém renin-angiotenzin-aldosteron, která lze použít při sekundární prevenci kardiovaskulárních příhod. Navazuje tak na obdobné přehledy týkající se porovnání vlastností inhibitorů ACE [9] nebo antagonistů receptorů AT 1 pro angiotenzin II [10] publikované v časopise Remedia. Údaje v tab. 3a3b vycházejí zejména z platných Souhrnů údajů o přípravcích (www.sukl.cz nebo www.emea. europa.eu) a z databáze Thomson Micromedex [11].
Předkládaný přehled, uvedený v tab. 3 , se snaží hutnou formou uvést nejvýznamnější farmakokinetická a klinická data týkající se těch léčiv ovlivňujících systém renin-angiotenzin-aldosteron, která lze použít při sekundární prevenci kardiovaskulárních příhod. Navazuje tak na obdobné přehledy týkající se porovnání vlastností inhibitorů ACE [9] nebo antagonistů receptorů AT 1 pro angiotenzin II [10] publikované v časopise Remedia. Údaje v tab. 3a3b vycházejí zejména z platných Souhrnů údajů o přípravcích (www.sukl.cz nebo www.emea. europa.eu) a z databáze Thomson Micromedex [11].
V tabelárním přehledu nejsou uvedeny vlastnosti jednotlivých léčiv z hlediska bezpečnosti. Důvodem je velmi dobrá tolerance jak inhibitorů ACE (ramipril, perindopril a trandolapril), tak sartanů (telmisartan). Je však zřejmé, že zejména telmisartan patří k nejlépe tolerovaným kardiovaskulárním léčivům, protože jeho podávání je spojeno s výrazně nižším výskytem kašle ve srovnání s inhibitory ACE a s nižším výskytem hypokalemií, zejména závažných, ve srovnání s léčbou inhibitory angiotenzin konvertujícího enzymu (i když i v jejich případě je incidence klinicky závažných hypokalemií nízká). Jeho podávání je ale provázeno vyšším rizikem hypotenze. Též z hlediska výskytu klinicky závažných lékových interakcí nejsou mezi jednotlivými léčivy významnější rozdíly, zejména proto, že takových lékových interakcí je minimum. 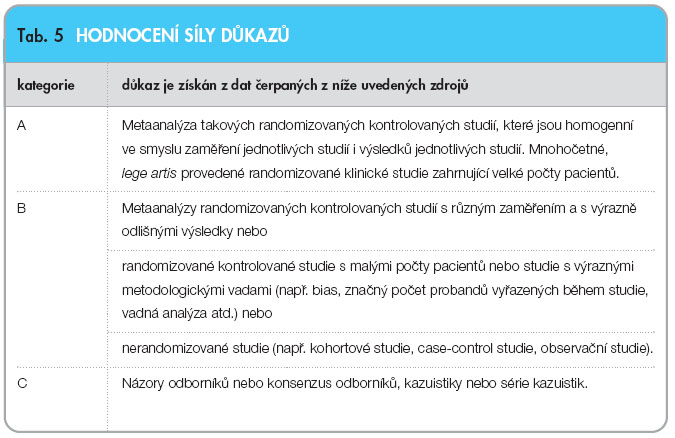
Seznam použité literatury
- [1] Údaje uveřejněné Státním ústavem pro kontrolu léčiv v Praze, 2010.
- [2] Yusuf S, Sleight P, Pogue J, et al. Effects of an angiotensin-converting-enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients. The Heart Outcomes Prevention Evaluation Study Investigators. N Engl J Med 2000; 342: 145–153.
- [3] Fox KM. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomised, double-blind, placebo-controlled, multicentre trial (the EUROPA study). Lancet 2003; 362 (9386): 782–788.
- [4] Braunwald E, Domanski MJ, Fowler SE, et al. Angiotensin-converting-enzyme inhibition in stable coronary artery disease. N Engl J Med 2004; 351: 2058–2068.
- [5] Yusuf S, Teo KK, Pogue J, et al. Telmisartan, ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008; 358: 1547–1559.
- [6] Pilote L, Abrahamowicz M, Rodrigues E, et al. Mortality rates in elderly patients who take different angiotensin-converting enzyme inhibitors after acute myocardial infarction: a class effect? Ann Intern Med 2004; 141: 102–112.
- [7] Pilote L, Abrahamowicz M, Eisenberg M, et al. Effect of different angiotensin-converting-enzyme inhibitors on mortality among elderly patients with congestive heart failure. CMAJ 2008; 178: 1303–1311.
- [8] Wienbergen H, Schiele R, Gitt AK, et al. MITRA PLUS Study Group: Impact of ramipril versus other angiotensin-converting enzyme inhibitors on outcome of unselected patients with ST-elevation acute myocardial infarction. Am J Cardiol 2002; 90: 1045–1049.
- [9] Červený P, Koblihová H. Inhibitory angiotenzin konvertujícího enzymu: přehled a porovnání základních údajů. Remedia 2009; 19: 215–219.
- [10] Suchopár J. Antagonisté receptorů AT1 pro angiotenzin II (sartany), porovnání základních údajů. Remedia 2007; 17: 295–299.
- [11] Thomson Micromedex® HealthCare Series vol. 135.