Jak rozlišit chřipku od COVID‑19 a jakou roli v léčbě hraje erdostein?
Součástí XIV. jarní interaktivní konference, kterou Společnost všeobecného lékařství ČLS JEP pořádala v náhradním termínu 18.‒20. září 2020 na virtuální platformě, bylo mimo jiné sympozium společnosti Angelini. Jeho dva přednášející – profesor Pierachille Santus z katedry biologických a klinických věd milánské univerzity a profesor František Kopřiva z Dětské kliniky FN a LF UP v Olomouci – vystoupili s příspěvky týkajícími se aktuální situace kolem pandemie nemoci COVID‑19. Přednášky byly prezentovány na základě prací dostupných v době konání odborné akce.
Profesor Santus věnoval první část
prezentace stručnému přehledu dosavadních poznatků o tom,
jak klinicky zvládat chorobu COVID 19 a jaké jsou
klinické charakteristiky pacientů s touto nemocí. Nejprve
zmínil dvě real world čínské práce z počátku
pandemie (Guan, et al., N Engl J Med 2020; Ai, et al.,
Radiology 2020), z nichž především druhou věnovanou
korelaci mezi CT vyšetřením hrudníku a RT PCR
testováním (polymerázová řetězová reakce spojená s reverzní
transkripcí) lze považovat za velmi důležitou z hlediska
vysoké senzitivity tohoto vyšetření. Pro pacienty s těžším
průběhem COVID 19 jsou na radiologickém zobrazení
typické prezentace opacit mléčného skla a závažnější
plicní příznaky v podobě intersticiální pneumonie.
Italská studie z lombardského regionu (Grasselli, et al., J Am Med Assoc 2020), která zahrnula 1 591 osob, přinesla první klinické charakteristiky pacientů, kteří byli hospitalizováni na jednotce intenzivní péče (JIP). Podle ní činila zaznamenaná mortalita nemocných na JIP 26 % a nejdůležitější komorbiditou, která souvisela s úmrtím na COVID 19, byla hypertenze. Novější zkušenosti s pacienty na JIP zachytila práce sledující nemocné v čínském Wu chanu (Yu, et al., Crit Care 2020). Pouze asi u 40 % těchto pacientů byla použita invazivní plicní ventilace, u 25 % neinvazivní plicní ventilace a u zbytku nemocných jen kyslíková maska nebo nosní kanyla s kyslíkem. Otázkou zůstává, zda měli být pacienti z poslední skupiny skutečně léčeni na JIP, zmínil přednášející.
Britská studie se stovkou pacientů hodnotila stav nemocných z hlediska klinického výsledku po provedené tracheostomii (McGrath, et al., Br J Anaesth 2020). Zaznamenané třicetidenní přežití a délka hospitalizace se u těchto nemocných odvíjely od závažnosti onemocnění COVID 19. Podle výsledků práce se zdá, že tracheostomie může pacientům s těžkým průběhem choroby zachránit život. „Podle mého názoru je to správný postup, neboť víme o řadě pacientů, kteří mohou mít z tracheostomie prospěch,“ komentoval profesor Salus.
Často citovanou práci, která přispěla k řešení otázky, kdy a jak používat neinvazivní plicní ventilaci, představuje prospektivní studie z počátku pandemie (Radovanovic, et al., J Clin Med 2020).
Aktuálně publikovaná práce italských intenzivistů (Grasselli, et al., Lancet 2020) zdůrazňuje význam onemocnění plic ve spojení s vaskulární komponentou, což je důležité z hlediska klinických projevů a přežití. Prostřednictvím kontrol bylo zjištěno, že antikoagulační terapie může zajistit zlepšení stavu pacientů bez nutnosti zavedení plicní ventilace.
Předběžná zpráva o používání dexametazonu u hospitalizovaných pacientů (RECOVERY Collaborative Group, N Engl J Med 2020) potvrdila prospěch z jeho užívání, větší efekt je patrný u nemocných, u nichž byla použita invazivní plicní ventilace. Zkušenosti s prodlouženým podáváním nízkodávkovaného metylprednisolonu představila studie, na níž se podílel také profesor Santus (Salton, et al., Open Forum Infectious Diseases 2020). Prospěch byl doložen u pacientů se závažnou pneumonií spojenou s infekcí SARS CoV 2. Snížil se počet nemocných, u nichž bylo nutné používat na JIP invazivní plicní ventilaci. U pacientů léčených metylprednisolonem byla potvrzena 75% pravděpodobnost přežití v porovnání se standardní léčbou.
Také používání rekonvalescentní plazmy má u pacientů se závažným průběhem onemocnění významný účinek na kumulativní zlepšení klinického výsledku (Li, et al., J Am Med 2020). V případě podávání hydroxychlorochinu s azitromycinem nebo bez něj u pacientů s mírným až středně závažným průběhem onemocnění nebyl zaznamenán významný rozdíl během patnáctidenního sledování (Cavalcanti, et al., N Engl J Med 2020).
Profesor Santus se v první části prezentace dotkl také významného tématu vakcíny proti onemocnění COVID 19. Poukázal na studii, do níž bylo zařazeno 50 000 pacientů a v níž testovaná vakcína prokazuje po 28 dnech dobrou bezpečnost a tolerabilitu (Zhu, et al., Lancet 2020), nebo na mRNA vakcínu, u níž byla třetí fáze zkoušení zahájena v červenci (Jackson, et al., N Engl J Med 2020).
COVID 19 versus chřipka
Z pohledu praktického pediatra prezentoval rozdíly mezi chřipkou a nemocí COVID 19 profesor Kopřiva. „Jako lidstvo disponujeme mnoha obrannými mechanismy,“ uvedl svoji přednášku. „Viry jsou v podstatě parazité, kteří nesou určitou genetickou informaci a snaží se využít schopnosti napadené buňky ke svému přežití a množení. Fylogeneze virů je diskutabilně zachytitelná a víme o nich velmi málo. Náš imunitní systém však vznikl pod tlakem virů, bez tohoto procesu bychom nebyli schopni se bránit.“
Lidstvo překonalo ve své historii několik velkých pandemií, například španělskou chřipku v letech 1918‒1920, která si vyžádala až 100 milionů obětí. Koronaviry, na něž se nyní soustředí pozornost, jsou RNA viry, které se v naší populaci vyskytují běžně. Vyvolávají mírné až středně těžké infekce horních cest dýchacích a nejčastěji se vyskytují na podzim a v zimě. Původně to byly infekce zvířecí. V roce 2002 se rozvinula epidemie SARS (z angl. Severe Acute Respiratory Syndrome), následně epidemie MERS (Middle East Respiratory Syndrome), kdy byl virus zpočátku nebezpečný, avšak během roku zmutoval. Aktuálně čelíme viru SARS CoV 2.
Naproti tomu chřipka (influenza) původně znamenala termín označující víru v nepříznivé astrologické vlivy coby příčiny nemocí. Je to RNA virus čeledi Orthomyxoviridae. Chřipkové viry typu A infikují savce a ptáky, chřipkové viry typu B převážně pouze lidi a chřipkové viry typu C lidi a prasata.
Pro diagnostiku onemocnění dýchacích cest máme k dispozici PCR testování, které zahrnuje viry chřipky, respirační syncytiální virus (RSV), metapneumovirus (MPV), adenovirus (ADV), viry parainfluenzy (PIV), běžné lidské koronaviry, enteroviry/rinoviry (EV/hRV), bokaviry, Mycoplasma pneumoniae a Chlamydia pneumoniae.
Rozdíly mezi chřipkou a COVID 19
Chřipka má míru infekčnosti (tzv. reprodukční číslo, R0) 1,5 a k hospitalizaci kvůli tomuto onemocnění dochází zhruba u 1 % pacientů. Pro nemoc COVID 19 způsobenou SARS CoV 2 je R0 2,5 bez sociálního distancování a hospitalizace pacientů je nutná v 5‒20 %. Jediná osoba s chřipkou může během dvou měsíců infikovat dalších 386 lidí, z nichž jen minimální počet je hospitalizován. Jeden pacient s COVID 19 by za stejné období infikoval 99 000 lidí, z nichž asi 20 000 by muselo být hospitalizováno. Mortalita u chřipky činí 0,1 %. U dětí může infekce až v 70 % případů proběhnout bezpříznakově. Při onemocnění COVID 19 je mortalita asi desetkrát větší, přibližně 1 %. „Naším štěstím je, že evoluční strategií virů je infikovat maximální počet hostitelů, aniž by způsobily jejich úmrtí,“ podotkl profesor Kopřiva.
Ke klasickým příznakům chřipky (flu like syndrom) patří horečka, bolest hlavy, únava, bolest svalů, suchý kašel, bolest hrdla, kýchaní, podrážděné oči, extrémní pocit zimy atd., není však mezi nimi uváděna rýma. Virus napadá dýchací systém, je přenášen kapičkami slin vznikajícími při kašlání, tedy vzduchem. Inkubační doba u chřipky je enormně krátká ‒ 3‒72 hodin.
V případě onemocnění COVID 19 je inkubační doba zhruba týden a projevuje se horečkou, ztrátou chuti, únavou, ztrátou čichu, dušností, kašlem, kašláním hlenu, bolestí svalů. Při závažném průběhu choroby může docházet ke zmatení, potížím s probouzením, výskytu namodralého obličeje či rtů, kašlání krve, trvalé bolesti hrudníku, úbytku bílých krvinek, selhání ledvin, vysoké horečce. Nemocí COVID 19 jsou více ohroženy vyšší věkové skupiny populace.
Co se děje při napadení imunitního
systému SARS CoV 2
Nespecifická (bariérová) imunita přehnaně uvolňuje mediátory a rozvíjí se těžká zánětlivá reakce (tzv. reakce zmatených makrofágů nebo fagocytární syndrom), která chováním připomíná autoimunitní proces a napadá vlastní plicní tkáň (tzv. cytokinová bouře). Dochází k narušení protivirové imunity, při němž jsou T regulační a Th17 lymfocyty zodpovědné za přestup neutrofilů a tvorbu neutrofilního zánětu (Riva, et al., Critical Care 2020). Objevuje se lymfopenie, a je tedy narušena naše obranyschopnost. Na povrchu buněk se navíc nachází protein ORF8, který se naváže na hlavní histokompatibilní komplex a oslabuje rozpoznání virů prostřednictvím lymfocytů. Snížená aktivita protivirové imunity tak nastartuje těžký průběh infekce.
Kininová kaskáda představuje jeden ze čtyř plazmatických kaskádových systémů, které napomáhají udržet integritu organismu. Jejím hlavním konečným produktem je bradykinin, látka s řadou fyziologických účinků, která se uplatňuje zejména při zánětu (Ganong, Review of Medical Physiology 2001). Bradykinin aktivuje fosfolipázu A2 a tím buněčný metabolismus kyseliny arachidonové. Při něm se tvoří mediátory nespecifické imunity a spouští se těžká zánětlivá odpověď. Právě u pacientů s těžkým průběhem nemoci COVID 19 byla prokázána vysoká koncentrace bradykininu.
Další důležitou roli při této infekci má molekula STING – stimulátor genů pro interferon gama (IFNγ). SARS CoV 2 tvoří proteinázy, které na počátku infekce snižují koncentraci STING, je zabráněno tvorbě IFNγ, a proto je virus schopen poškodit buněčnou DNA. U pacientů s nízkou aktivitou STING se projevily nejzávažnější formy onemocnění, neboť neměli dostatečnou tvorbu IFNγ a nebyli schopni se bránit. „Ochranný vliv by zde mohl mít vitamin D ve formě blokace přehnané aktivity STING ve druhé fázi, kdy je poškozena DNA buňky,“ komentoval přednášející.
Co dále pomáhá při diferenciální
diagnostice
Pro stanovení diagnózy máme
jednoduché schéma, které v počátku může napomoci rozlišit
mezi alergií, chřipkou, nachlazením a COVID 19 (obr. 1). Problematická je komplikace v podobě pneumonie
a odlišení její virové a bakteriální etiologie
od manifestace nemoci COVID 19 (Sharma, et al., Coronavirus
Disease 2019, 2020). Při virové pneumonii se objevuje vysoká
teplota, kašel, bolest v krku, zvýšené množství leukocytů,
na RTG retikulární nálezy nebo atelektázy. Pro bakteriální
pneumonii je typická leukocytóza, vysoká sedimentace a vysoké
hodnoty C reaktivního proteinu, zatímco u COVID 19
nacházíme lymfopenii a nález na RTG může přetrvávat
i měsíce.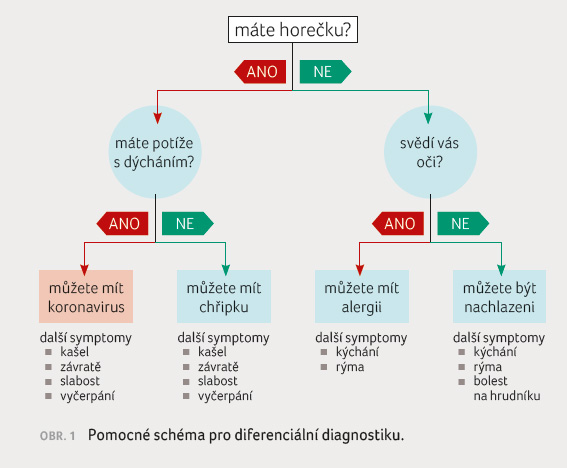
V případě chřipky je virus nebezpečnější, mutuje a každý rok je třeba proti němu očkovat novým typem vakcíny. Naproti tomu poslední mutace koronaviru není tak smrtelná, avšak snáze se šíří.
Úloha erdosteinu v léčbě
COVID 19
V druhé části své prezentace profesor Santus představil léčbu erdosteinem u pacientů s COVID 19 na základě zkušeností, které vycházejí z průběžných a aktuálně publikovaných výsledků real world observační studie (Santus, et al., Multidiscip Respir Med 2020).
Dlouhodobě čelíme znečištění životního prostředí pevnými částicemi, které se dostávají do různých částí respiračního systému, drobnější částice pak do periferních částí plic. Negativní vliv na plíce mají zejména částice PM10 – s průměrem menším než 10 mikronů, což prokázala řada studií. „Záměrem našeho sledování bylo otestovat hypotézu prozánětlivé oxidační aktivity PM10,“ vysvětlil profesor Santus (Li, et al., Thorax 1996). Výsledky ukazují, že počet neutrofilů v bronchoalveolární laváži u potkanů in vivo šest hodin po intratracheální aplikaci PM10, ultrajemných částic černého uhlíku, skutečně působí velmi negativně vzhledem ke stoupajícímu počtu neutrofilů. Rovněž bylo doloženo, že účinek intratracheální aplikace PM10 na produkci tumor nekrotizujícího faktoru a produkci oxidu dusnatého leukocyty v alveolární laváži je výrazně negativní. Tyto částice tedy zapříčiňují zánět v plicích a zároveň zvýšení oxidačního stresu (nerovnováhy mezi tvorbou reaktivního kyslíku a schopností organismu rychle odbourávat reaktivní meziprodukty). To je přímo spojeno se snížením koncentrací antioxidačních látek, zejména glutathionu (GSH). Glutathion představuje důležitý antioxidant u rostlin, zvířat, hub a některých bakterií, který je schopen zabránit poškození důležitých buněčných složek způsobených reaktivními druhy kyslíku, jako jsou volné radikály, peroxidy lipidů a těžké kovy.
Environmentální znečištění je v přímé korelaci se zhoršením situace kolem onemocnění COVID 19. Špatná kvalita ovzduší je spojena s navýšením počtu případů COVID 19 a také s nárůstem mortality. Oxidační stres zřejmě zvyšuje riziko virové infekce. Existují vědecké důkazy, které zdůrazňují úlohu redoxní rovnováhy v patologii oxidačního stresu. Akumulace radikálových kyslíkových forem a vymizení systému jejich odstraňování vede ke zvyšování oxidačního stresu, k aktivaci imunitních odpovědí a zánětu.
Infekce plic respiračními viry je obecně spojena s produkcí cytokinů, se zánětem, s buněčnou smrtí a s dalšími patologickými procesy, což může vyvolat zvýšená produkce reaktivních forem kyslíku (reactive oxygen species, ROS). Vyšetřování vlivu těchto infekcí na enzymy a systémy vedoucí k těmto formám kyslíku nám mohou pomoci zjistit, které z nich jsou klíčové pro replikaci patogenů a pro virové choroby. Je tedy možné, že infekce SARS CoV 2 v tomto směru negativně působí na dýchací cesty obecně, ale zapříčiňuje rovněž vaskulární problémy plic, např. trombózu a vaskulární zánět. Tyto procesy jsou spojeny se zvyšováním hodnot ROS, neutrofilů, feritinu a interleukinu 6. „Pokud budeme vycházet z hypotézy, že antioxidanty jsou významné při léčbě virových infekcí, je důležité, abychom měli jejich dostatečnou koncentraci. A zde může hrát značnou úlohu GSH, který ovlivňuje různé replikativní mechanismy různých virů v různých stadiích,“ vysvětlil přednášející. Imunomodulační aktivita GSH může být prospěšná v případě těchto virových onemocnění, kdy nastává nerovnováha mezi odpověďmi lymfocytů Th1 a Th2.
Používání GSH jako terapeutického
agens je vzhledem k jeho biochemickým a farmakokinetickým
vlastnostem omezeno, je však možné použít molekuly pro GSH,
které koncentrace GSH zvyšují ‒ k nim patří například
erdostein. Uvedené molekuly mohou být buď deriváty GSH, které
jsou schopny snáze překračovat buněčnou membránu, nebo mohou
být zdrojem thiolů pro syntézu GSH. Deficience GSH už byla
vyhodnocena i v souvislosti s onemocněním COVID 19
a jeho patogenezí, kdy vede ke zvýšené replikaci viru
a k poškození plic. U starších pacientů je nižší
příjem GSH spojen s rozvojem chronických chorob,
respiračních a metabolických onemocnění. Týká se to
hlavně mužů a aktivních kuřáků.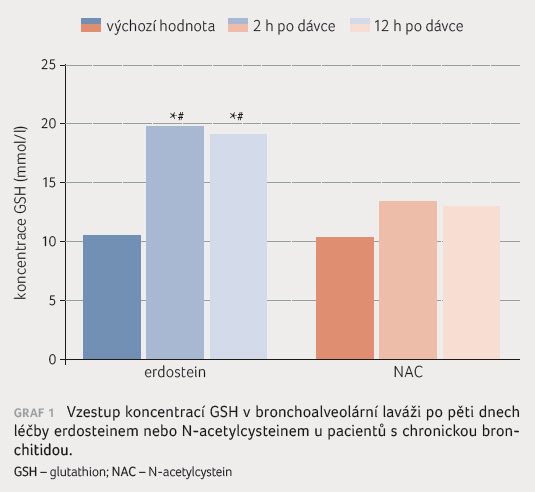
V jedné ze studií (Franternale, et al., Mol Aspects Med 2009) bylo prokázáno, že přítomnost GSH snižuje virovou zátěž a replikaci viru v kultivaci humánních fibroblastů. Dále sledování přineslo důkazy, že erdostein může zlepšit situaci u pacientů po pěti dnech léčby (2 h a 12 h po podání dávky). Zlepšení po podání erdosteinu je výraznější u pacientů, kteří tuto léčbu dostávali, v porovnání s kontrolní skupinou (graf 1). Z uvedených zjištění vyplývá, že snížení antioxidačního statusu podporuje vznik virových infekcí a virové infekce snižují antioxidační status (tzv. redox status).
V real world observační studii, která zahrnula 20 pacientů s COVID 19 spojeným s pneumonií a se závažným respiračním selháním, byl nemocným podáván erdostein v dávce 300 mg dvakrát denně po
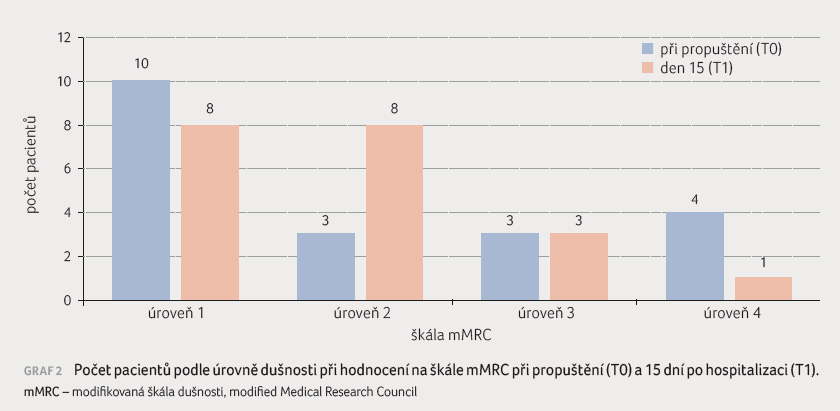
dobu 15 dnů po hospitalizaci (graf 2). Byla hodnocena kvalita života a dušnost na různých škálách. Všechny sledované parametry se zlepšily statisticky významně u pacientů užívajících erdostein. U nemocných, kterým erdostein nebyl podáván, byly symptomy přítomny dlouhou dobu po hospitalizaci. Ke klinicky významnému zmírnění příznaků (dušnost a kašel) a ke zlepšení kvality života podle škály HRQoL (Health Related Quality of Life) došlo u 65 % nemocných.
Redakčně zpracovala PhDr. Nikola Homolová Richtrová