Kyselina acetylsalicylová – stále neotřesitelné postavení i v roce 2018?
Key words: aspirin, salicylic acid, enterosolvent drug formulation, antithrombotic treatment, tumour chemoprophylaxis.
Není mnoho léků s tak bohatou historií, úspěšnou přítomností a nadějnou budoucností, jako má kyselina acetylsalicylová (ASA). Salicyláty jsou jednou z mála skupin léků, které přetrvaly po více než dvě tisíciletí. Kyselina acetylsalicylová je bezesporu jedním z nejúspěšnějších léků dvacátého století. Na počátku minulého století Franz Kafka nazývá Aspirin „zázrakem“, třicátá léta bývají označována jako „léta aspirinová“ a v roce 1968 byla ASA součástí lékárničky Apollo 11, tedy „Aspirin on the Moon“.
Dlouhá a zajímavá historie
Nezačíná li příběh ve starém Řecku, není důvěryhodný, historie salicylátů začíná u starořeckého Hippokrata. Ten kolem roku 400 př. n. l. doporučuje „hojně dopřát odvaru z kůry vrby na všechny typy horkosti a křečí“. Vrbová kůra je bohatým zdrojem salicinu. Léčba salicyláty – v indikaci antiflogistika, analgetika a antipyretika – přetrvala až do konce 19. století, kdy štafetu převzal derivát salicylátů s lepší snášenlivostí – kyselina acetylsalicylová.
Historie ASA je velmi zajímavá. V roce 1897 hledá německý chemik – zaměstnanec firmy Bayer – Felix Hoffman lék pro svého otce trpícího artritidou. Ten salicyláty pro zažívací potíže špatně snášel, syn proto zkoušel řadu derivátů kyseliny salicylové, které by byly lépe tolerovány. Objevuje půl století starý postup Francouze Gerhardta na syntézu kyseliny acetylsalicylové. Dodnes není jasno, z čí iniciativy byla ASA navržena jako „dobře tolerovaný“ salicylát. Patent byl sice přiřknut Felixi Hoffmanovi, idea však pravděpodobně pochází od jeho školitele Arthura Eichengrüna, jehož židovský původ byl v té době handicapem.
Pouť Aspirinu, jak byla ASA komerčně nazvána, nebyla jednoduchá, v cestě stál vedoucí firemního farmakologického výzkumu profesor Heinrich Dreser. Ten, coby otec diacetylmorfinu – heroinu, preferoval „své dítě“ a málem zabránil uvedení konkurenčního Aspirinu na trh se záminkou, že „negativně působí na srdce“. Nicméně když byl heroin roku 1898 úspěšně uveden na trh, na pokyn „shora“ doporučil Dreser též výrobu ASA. Paradoxně tak jedna osoba stála u zrodu dvou úspěšných léků – legálního Aspirinu a dnes ilegálního heroinu [1]. Ubezpečení, že Aspirin „nepůsobí na srdce“, pak bylo uvedeno na lahvičkách firmy Bayer až do čtyřicátých let. Farmakokinetické vlastnosti i klinický efekt prověřil u pěti desítek nemocných s artralgiemi v místní nemocnici Kurt Witthauer, zajímavé je, že již on v roce 1899 konstatuje dobrou absorpci ASA v kyselém prostředí žaludku a hydrolýzu ASA na kyselinu salicylovou v alkalickém prostředí střeva.
Nicméně ASA – jako antiflogistikum, antipyretikum i analgetikum – by dlouho nehrála první housle. Od šedesátých let jí konkuruje plejáda modernějších nesteroidních antirevmatik, zejména ibuprofen. Význam ASA jako antiflogistika, analgetika a antipyretika byl nahrazen důležitostí ASA jako léku s protidestičkovým působením a v současné době i s působením protinádorovým. I průnik do „kardiologické“ indikace má zajímavou historii. V roce 1951 si kalifornský praktik Dr. Craven všímá, že u nemocných léčených ASA se objevuje výrazné krvácení při tonzilektomii, a doporučuje pak svým nemocným aspirin jako lék na prevenci trombózy. Bohužel výsledek pozorování poklesu trombotických afekcí v souboru na tu dobu neuvěřitelných 8 000 nemocných byl publikován jen v místním časopise a na mnoho let zapadl. Ani další léta aspirinu nepřála. V sedmdesátých letech totiž americký epidemiolog Herschel Jick publikoval pozorování, že nemocní užívající ASA jsou přijímáni do nemocnice s infarktem myokardu méně často nežli nemocní, kteří ASA neužívali. Nález paradoxně interpretoval tak, že nemocní zemřeli dříve, než se dostali do nemocnice. Proti tomuto názoru se naštěstí postavil Peter Elwood, který počátkem sedmdesátých let minulého století provedl dvojitě zaslepenou studii a poukázal na trend ke snížení mortality o 12 % za 6 měsíců a o 25 % za 12 měsíců a snížení výskytu recidivy infarktu myokardu při užívání ASA. Tečku za debatami o prospěšnosti ASA u nemocných s aterotrombotickým postižením udělala až metaanalýza řady klinických studií, která příznivý efekt jednoznačně potvrdila.
V téže době, tedy v roce 1971, publikuje sir John Vayne v časopisu Nature objev, že ASA inhibuje cyklooxygenázu (COX) a tvorbu prostanoidů. Za tento objev dostává o deset let později Nobelovu cenu. Pozitivní výsledky klinického hodnocení, spolu s doložením protidestičkového účinku, umožnily v osmdesátých letech nástup ASA v indikaci antitrombotika u nemocných po infarktu myokardu. Jasně doložený efekt na zlepšení prognózy, relativně dobrá tolerance a nízká cena udělaly z ASA po farmakoekonomické stránce nejvýhodnější lék všech dob. Tak se kruh uzavřel: ASA na srdce přece jen působí. Za méně než korunu denně získáváme lék snižující mortalitu i výskyt akutních i chronických forem aterotrombotických onemocnění, zejména příhod koronárních a mozkových. A jak bude doloženo, platí to i v dnešní době. Navíc, při podávání ASA v prevenci aterotrombotických příhod přistupuje i „bonus“ ve formě snížení výskytu některých typů nádorů, zejména kolorektálního adenokarcinomu.
Co víme a co nevíme o mechanismu účinku
Není mnoho léků užívaných více než 100 let, kde bychom měli tak neúplné představy o mechanismu působení. Je sice pravděpodobné, že v protidestičkovém efektu hraje dominantní úlohu snížení syntézy tromboxanu A2 (TXA2) blokádou destičkové COX, ale na antitrombotickém účinku, jak bude ukázáno, se mohou podílet i jiné faktory. Není objasněn jak efekt samotné ASA – jako zdroje acetylové skupiny pro acetylaci proteinů, tak efekt aktivního metabolitu, tj. kyseliny salicylové – jako zprostředkovatele protizánětlivého, analgetického a antipyretického účinku. Není plně objasněna úloha biologicky aktivních metabolitů kyseliny salicylové.
Efekt ASA na změnu biologické aktivity řady proteinů jejich acetylací
Pravděpodobně hlavním
účinkem, alespoň stran protidestičkového působení, je
ireverzibilní inhibice cyklooxygenázy 1 (COX 1)
a cyklooxygenázy 2 (COX 2) acetylací aminokyseliny
serinu. Změna konfigurace v katalytickém místě enzymu
znemožní konverzi kyseliny arachidonové na prekurzory
prostanoidů. Ukazuje se, že acetylace není omezena pouze
na izoenzymy COX, ale acetylovány jsou i jiné proteiny
(enzymy či strukturální proteiny), nebo dokonce nukleotidy
nukleových kyselin. Příkladem acetylace jiných enzymů je
inhibice cy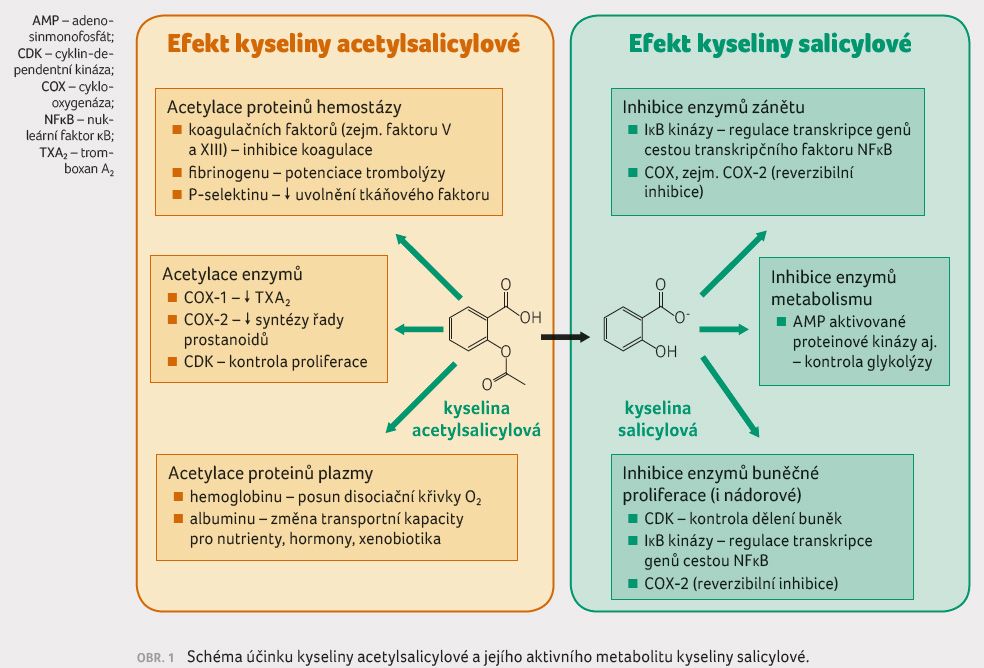 klin dependentních kináz (CDK), které řídí
proliferaci buněk (obr. 1).
Zde je možný vztah k protinádorovému působení ASA,
výsledný biologický význam zdaleka není objasněn.
klin dependentních kináz (CDK), které řídí
proliferaci buněk (obr. 1).
Zde je možný vztah k protinádorovému působení ASA,
výsledný biologický význam zdaleka není objasněn.
Jako příklad acetylace biologicky aktivních proteinů je možno uvést acetylaci aminokyseliny lysinu v řetězci fibrinogenu. Acetylace – na 12 místech – se týká všech řetězců fibrinogenu, farmakodynamický efekt však je dán zejména acetylací řetězce α v místě vzájemné vazby s ostatními řetězci. Výsledný modifikovaný fibrin je méně kompaktní a je pak přístupnější k fibrinolýze [2]. Tento facilitační efekt ASA na trombolýzu (doložený též in vivo) se pravděpodobně účastní příznivého efektu ASA při kombinaci s trombolytiky, který byl pozorován ve studii ISIS 2 [3]. Jiným příkladem je acetylace hemoglobinu, která ovlivňuje disociační křivku kyslíku, či acetylace albuminu ovlivňující jeho transportní kapacitu – např. pro nutrienty, vitaminy či hormony (konkrétně vazebnou kapacitu tyroxinu). Acetylací koagulačních faktorů (V či XIII) je ovlivněna též hemostáza sekundární. Výčet zdaleka není úplný, popsána je acetylace několika set proteinů (často enzymů), biologický efekt však není jasný a je možno se nadít překvapení.
V posledních letech se ukazuje, že malé dávky ASA potlačují vznik a progresi nádorového bujení. Cyklooxygenáza 2 je v časných stadiích tumorogeneze zvýšeně aktivní a vysoká nabídka aktivních metabolitů kyseliny arachidonové (prostanoidů i leukotrienů) se zdá být významným mediátorem proliferace nádorů. Byl prokázán nižší výskyt nádorů, zejména karcinomu kolon, při dlouhodobé aplikaci ASA. Tento efekt byl opakovaně doložen v megastudiích, kdy byla ASA podávána z indikace kardiologické.
K acetylaci biologicky aktivních proteinů v krvi (jak v plazmě, tak v cirkulujících buňkách) dochází již v portálním oběhu. Zde je totiž výrazně vyšší koncentrace ASA než po hydrolýze na kyselinu salicylovou v játrech. Též protidestičkový efekt – acetylace serinu v katalytickém místě COX – probíhá presystémově, tedy v cirkulaci portální. Do jaké míry má na biologickém efektu podíl nízká koncentrace ASA v systémové cirkulaci, není zcela jasné.
Efekt kyseliny salicylové – aktivního metabolitu ASA
Již od samého vývoje „aspirinu“ bylo cílem získat lépe tolerovaný salicylát, než jakým byla do té doby užívaná kyselina salicylová. Nepřekvapuje tedy, že za protizánětlivý, analgetický a antipyretický efekt je zodpovědná kyselina salicylová. Biotransformace ASA na kyselinu salicylovou ve střevě a v játrech je rychlá a masivní. Maximální plazmatické koncentrace ASA (v dávce 500 mg v rychle rozpustné formě) je dosaženo již za 20 minut a maximální plazmatické koncentrace kyseliny salicylové jen o málo později, asi za 30 minut [4]. Expozice (plocha pod křivkou plazmatické koncentrace [AUC] čili součin koncentrace a času v systémovém oběhu) je pak u kyseliny salicylové asi 40× vyšší (5−7 mg.h/l u ASA vs. 160−200 mg.h/l u kyseliny salicylové).
Mechanismus účinku kyseliny salicylové rovněž není zcela jasný. Většina prací dokládá, že dominuje efekt na úrovni genomu, konkrétně potlačení exprese izoenzymů COX působením na transkripční faktor NFκB (obr. 1). Výsledná inhibice COX tímto mechanismem je reverzibilní, trvá kratší dobu, není omezena na trombocyty, ale objevuje se v celé systémové cirkulaci včetně endotelií. Tak je potlačena syntéza celé řady vazodilatačních, prozánětlivých prostanoidů, dominuje efekt antiflogistický, antipyretický a analgetický. Do jaké míry se uplatní tento účinek, tj. snížení syntézy COX 1, na protidestičkovém působení a na poklesu výskytu aterotrombotických příhod, není zřejmé. Díky tomu, že reverzibilní inhibice COX (např. nesteroidními antiflogistiky) v celém cévním řečišti i v trombocytu naopak riziko kardiovaskulárních příhod zvyšuje, je málo pravděpodobné, že by tento mechanismus měl pozitivní efekt. Také nepřesvědčivé výsledky studií s ASA v enterosolventních formách, kdy dochází k deacetylaci ASA ještě v lumen střeva, svědčí ve prospěch klasické koncepce, tedy ireverzibilní inhibice COX acetylací. V protinádorovém působení hrají pravděpodobně úlohu metabolity kyseliny salicylové – dihydroxy a tetrahydroxyderiváty kyseliny benzoové vznikající působením střevních bakterií. Tyto aktivní metabolity velmi významně inhibují dělení buněk a proliferaci nádorů na úrovni již zmíněných CDK. Jejich vysoká nabídka právě v tračníku může přispívat k profylaktickému účinku na kolorektální karcinom [5].
Shrneme li, pak 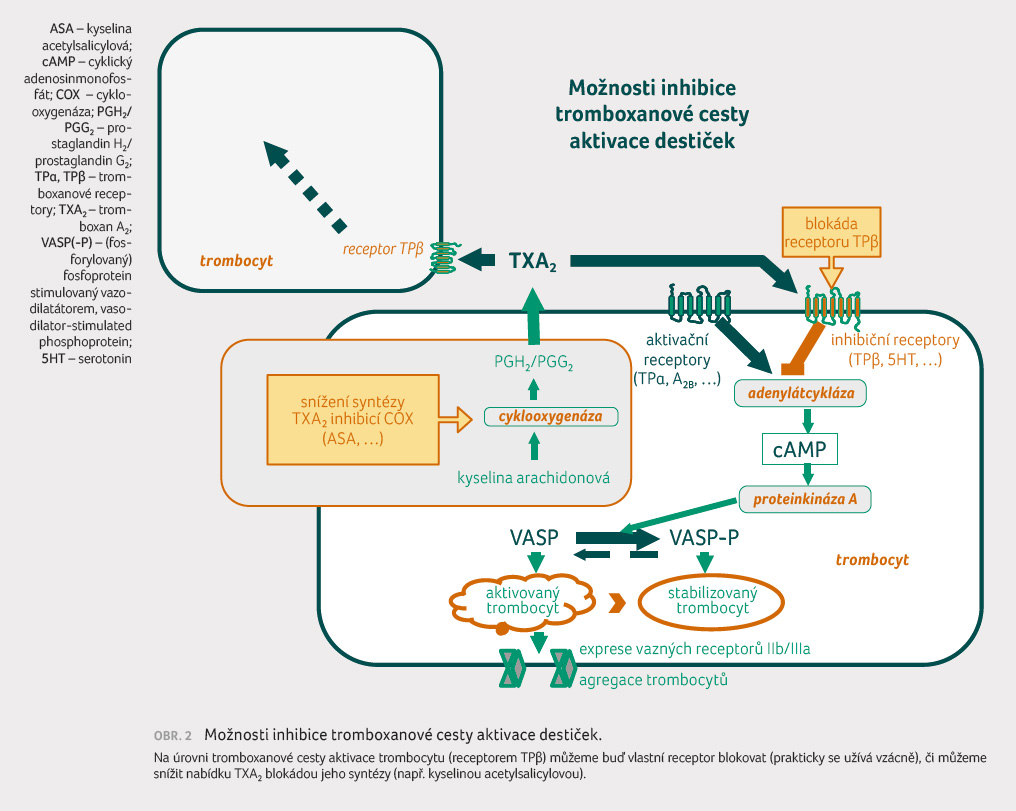 v dominující
indikaci ASA, tj. snížení rizika recidivy aterotrombotických
příhod, je protidestičkový efekt zprostředkován vlastní ASA,
tedy nevratnou blokádou COX 1. Snížení syntézy
TXA2 v trombocytu a následně pokles jeho
nabídky pro degranulaci je zřejmě efektem rozhodujícím (obr. 2). Mechanismem protizánětlivého účinku
je snížení aktivity obou izoenzymů COX 1 i COX 2,
klíčových enzymů syntézy jak vazokonstrikčně/trombogenně, tak
i vazodilatačně/antitrombogenně působících prostanoidů
(zejm. TXA2 a prostacyklinu PGI2).
Inhibice COX 1 se projevuje i v dávkách nízkých
(efekt ASA), inhibice COX 2 od dávek středních (efekt
kyseliny salicylové).
v dominující
indikaci ASA, tj. snížení rizika recidivy aterotrombotických
příhod, je protidestičkový efekt zprostředkován vlastní ASA,
tedy nevratnou blokádou COX 1. Snížení syntézy
TXA2 v trombocytu a následně pokles jeho
nabídky pro degranulaci je zřejmě efektem rozhodujícím (obr. 2). Mechanismem protizánětlivého účinku
je snížení aktivity obou izoenzymů COX 1 i COX 2,
klíčových enzymů syntézy jak vazokonstrikčně/trombogenně, tak
i vazodilatačně/antitrombogenně působících prostanoidů
(zejm. TXA2 a prostacyklinu PGI2).
Inhibice COX 1 se projevuje i v dávkách nízkých
(efekt ASA), inhibice COX 2 od dávek středních (efekt
kyseliny salicylové).
Klasickou koncepcí účinku ASA je
inhibice aktivity COX 1 na podkladě blokády katalytické
funkce enzymu jeho acetylací. V oblasti aktivního místa se
ASA kovalentně váže na serin a acetyluje jej.
Konformační změny v katalytickém centru pak zabrání
oxidaci kyseliny arachidonové a vytvoření prekurzorů
prostanoidů – prostaglandinů H2 a G 2.
Díky kovalentní vazbě je efekt ireverzibilní. Jako bezjaderná
buňka si trombocyt nemůže syntetizovat nový enzym, a efekt
tak přetrvává po celou dobu přežívání trombocytu
v krevním oběhu (tj. 5–7 dnů). Vzhledem k tomu, že je
potřeba funkčně vyřadit 60−80 % trombocytů a k denní
obnově 10−20 % destiček, trvá plný účinek asi 48
hodin, zcela funkční však je hemostáza až za 4–5 dnů
po vysazení léčiva. Vlastní acetylace COX v trombocytu
probíhá ještě v portálním oběhu, po průchodu játry
je (při užití terapeutických dávek) většina ASA deacetylována
na kyselinu salicylovou a kapacita pro acetylaci COX
v systémové cirkulaci je nedostatečná. Díky nízké
systémové dostupnosti ASA tak není ireverzibilně inhibována též
COX v endoteliích cév, a produkce PGI2 proto
významně neklesá. Souběžně s protidestičkovým
působením mají malé dávky ASA řadu dalších, často rovněž
významných účinků. Acetylací koagulačních faktorů je
potlačena též sekundární hemostáza a ovlivněna je
i fibrinolýza. Přehled komplexního působení ASA
na hemostázu je uveden v tabulce 1.
2.
Díky kovalentní vazbě je efekt ireverzibilní. Jako bezjaderná
buňka si trombocyt nemůže syntetizovat nový enzym, a efekt
tak přetrvává po celou dobu přežívání trombocytu
v krevním oběhu (tj. 5–7 dnů). Vzhledem k tomu, že je
potřeba funkčně vyřadit 60−80 % trombocytů a k denní
obnově 10−20 % destiček, trvá plný účinek asi 48
hodin, zcela funkční však je hemostáza až za 4–5 dnů
po vysazení léčiva. Vlastní acetylace COX v trombocytu
probíhá ještě v portálním oběhu, po průchodu játry
je (při užití terapeutických dávek) většina ASA deacetylována
na kyselinu salicylovou a kapacita pro acetylaci COX
v systémové cirkulaci je nedostatečná. Díky nízké
systémové dostupnosti ASA tak není ireverzibilně inhibována též
COX v endoteliích cév, a produkce PGI2 proto
významně neklesá. Souběžně s protidestičkovým
působením mají malé dávky ASA řadu dalších, často rovněž
významných účinků. Acetylací koagulačních faktorů je
potlačena též sekundární hemostáza a ovlivněna je
i fibrinolýza. Přehled komplexního působení ASA
na hemostázu je uveden v tabulce 1.
Jak je doložen efekt ASA v rámci prevence aterotrombotických příhod?
Na tomto místě nelze porovnávat
a probírat studie jednotlivě, je jich
několik set. Pro hodnocení efektu v rámci sekundární
prevence, což je hlavní indikace ASA, je vhodné užití renomované
metaanalýzy efektu od pracovní skupiny Antithrombotic
Trialists’ Collaboration (ATC). Tato analýza zahrnula celkem 287
studií se 135 000 nemocných [6]. Protidestičková léčba 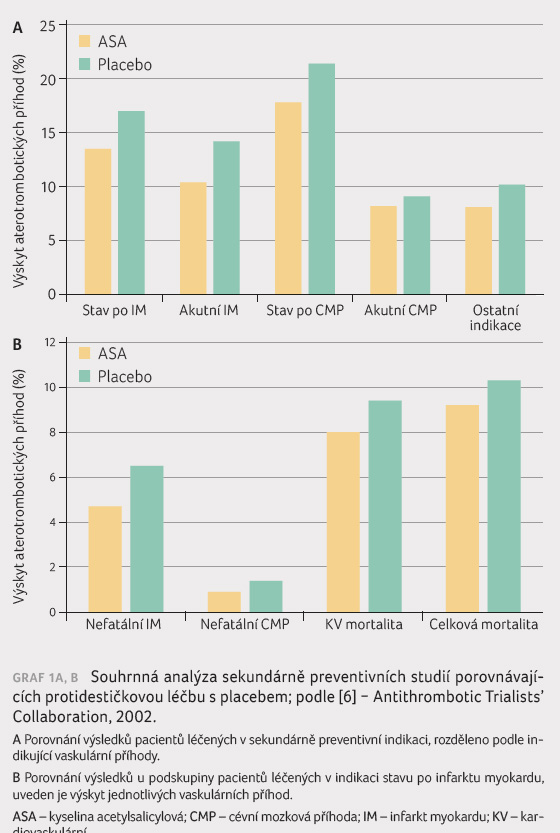 (až
na výjimky se jednalo o ASA v rychle
rozpustné formě) vedla ke snížení výskytu
vaskulárních příhod o čtvrtinu, z toho výskyt
nefatálních myokardiálních infarktů byl redukován o třetinu,
nefatální cévní mozkové příhody více než o čtvrtinu
a vaskulární mortalita klesla o šestinu. Vedle nemocných
indikovaných k léčbě pro ischemickou chorobu srdeční
(zejména po infarktu myokardu) či po cévní mozkové
příhodě jsou doklady o příznivém efektu ASA u pacientů
s aterosklerózou tepen dolních končetin, s postižením
v karotické oblasti či po revaskularizačních
a rekonstrukčních cévních zákrocích (po cévních
operacích či angioplastikách) v různé lokalizaci (graf 1A, B). Též poměr účinnosti (snížení výskytu
vaskulárních příhod) a bezpečnosti (výskytu významného
krvácení) byl příznivý.
(až
na výjimky se jednalo o ASA v rychle
rozpustné formě) vedla ke snížení výskytu
vaskulárních příhod o čtvrtinu, z toho výskyt
nefatálních myokardiálních infarktů byl redukován o třetinu,
nefatální cévní mozkové příhody více než o čtvrtinu
a vaskulární mortalita klesla o šestinu. Vedle nemocných
indikovaných k léčbě pro ischemickou chorobu srdeční
(zejména po infarktu myokardu) či po cévní mozkové
příhodě jsou doklady o příznivém efektu ASA u pacientů
s aterosklerózou tepen dolních končetin, s postižením
v karotické oblasti či po revaskularizačních
a rekonstrukčních cévních zákrocích (po cévních
operacích či angioplastikách) v různé lokalizaci (graf 1A, B). Též poměr účinnosti (snížení výskytu
vaskulárních příhod) a bezpečnosti (výskytu významného
krvácení) byl příznivý.
V primární prevenci se
problematikou účinnosti a bezpečnosti ASA zabývá
metaanalýza devíti kontrolovaných studií provedených u více
než 100 000 probandů [7]. Studie doložila významný sumární
pokles výskytu všech vaskulárních př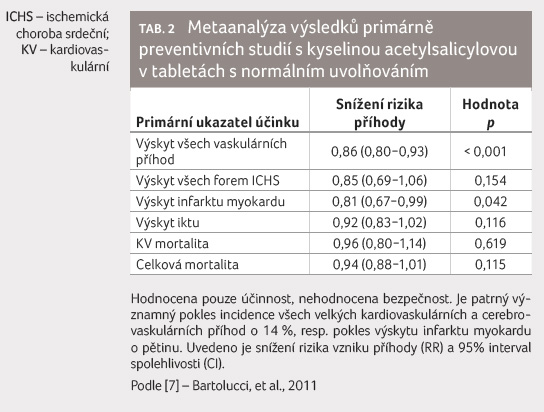 íhod o 10−20 %,
efekt na jednotlivé formy ukazuje tabulka 2. Čistý klinický přínos, tj. součet účinnosti
(kardiovaskulárních příhod) a rizika
(významných krvácení) však nedosáhl významnosti. Velká
krvácení se v intervenované skupině vyskytla asi o 1 %
(absolutní) častěji než při podávání placeba. V dalších
primárně preventivních studiích z recentní doby
(např. Japanese Primary Prevention Project či ASPREE) již bohužel
byly užity enterosolventní tablety ASA, problematika
této lékové formy bude diskutována později.
íhod o 10−20 %,
efekt na jednotlivé formy ukazuje tabulka 2. Čistý klinický přínos, tj. součet účinnosti
(kardiovaskulárních příhod) a rizika
(významných krvácení) však nedosáhl významnosti. Velká
krvácení se v intervenované skupině vyskytla asi o 1 %
(absolutní) častěji než při podávání placeba. V dalších
primárně preventivních studiích z recentní doby
(např. Japanese Primary Prevention Project či ASPREE) již bohužel
byly užity enterosolventní tablety ASA, problematika
této lékové formy bude diskutována později.
Platí data získaná ze studií provedených převážně v 90. letech i v dnešní době?
Předložená data ukázala, že minimálně v sekundární prevenci byly podány důkazy o příznivém efektu na pokles výskytu cévních příhod i mortality, v primární prevenci byl efekt omezen na infarkt myokardu, resp. na všechny vaskulární příhody. Podávání ASA v rámci prevence sekundární je součástí doporučených postupů a nepodání ASA či alternativní protidestičkové léčby by bylo postupem non lege artis. V současné době nelze efekt porovnávat proti placebu – ASA je v prevenci aterotrombotických příhod zlatým standardem.
Je však tento „zlatý standard“ skutečně „zlatý“? Tato otázka má velký význam, jen v České republice je ASA léčen necelý jeden milion nemocných. Pro srovnání – blokátory trombocytárních receptorů pro adenosindifosfát (ADP) užívá o celý řád méně osob. Právě s příchodem blokátorů receptorů pro ADP se spekulovalo o tom, že by tato skupina mohla ASA nahradit, resp. byly vzneseny pochybnosti, zda ASA má i v dnešní době dostatek důkazů o účinku v profylaxi aterotrombotických příhod. Hmatatelným dokladem o této skutečnosti je i „Grand debate – ASPIRIN FOR LIFE?“. Ta proběhla v srpnu 2017 na kongresu Evropské kardiologické společnosti (ESC) v Barceloně pod taktovkou nestora světové kardiologie profesora Eugena Braunwalda [8]. V aranžmá „pro a proti“ byly diskutovány otázky: Platí závěry ATC i v roce 2017? Je efekt ASA patrný i v dalších letech po infarktu myokardu, resp. po iktu? Je efekt ASA doložitelný u žen? Je efekt ASA doložitelný u seniorů? Je efekt ASA doložitelný u diabetiků 2. typu?
Podat jednoznačnou odpověď na řadu těchto otázek je obtížné. Předně proto, že naprostá většina studií dokládajících účinek ASA v primární a v sekundární prevenci probíhala před dvaceti či třiceti lety. V té době byly požadavky na kvalitu studií méně náročné a ne vždy doklady odpovídají nárokům současné „medicíny založené na důkazech“. Druhým důvodem je, že současná souběžná léčba je zcela jiná, než byla v osmdesátých a devadesátých letech minulého století. Jiná z pohledu dalších účinných léčebných postupů (zejm. v oblasti hypolipidemik a antihypertenziv) či jiná z pohledu významných lékových interakcí (např. masového podávání inhibitorů protonové pumpy). Třetím důvodem, který si zpravidla ani neuvědomujeme, je to, že užíváme jiné lékové formy než ty, které byly užity ve studiích hodnotících efekt ASA v různých indikacích. Zde mám na mysli především tzv. protektivní formy čili enterosolventní tablety ASA (Aspirin Protect či Stacyl). Opakovat tyto sekundárně preventivní studie dnes není možné. Veškeré kontrolované studie s ASA vůči placebu, které běží v současné době, jsou v prevenci primární (studie ASPREE, ASCEND a ARRIVE). V této indikaci, tj. v prevenci primární, je otázka poměru účinnosti a bezpečnosti stále z velké části otevřená.
Nemůžeme li u nemocných po kardiovaskulární či cerebrovaskulární příhodě opakovat kontrolované studie, jak situaci řešit? Naštěstí byla na podzim minulého roku zveřejněna velká observační studie, která porovnávala prognózu probandů léčených ASA v rámci primární či sekundární prevence s prognózou osob, které ASA přestaly užívat [9]. Model vysazení ASA sice neposkytuje o efektu léčby rovnocenná data, jako dávají kontrolované randomizované studie, nicméně pokud by léčba ASA nebyla přínosná, pak by její vynechání nemělo prognózu nepříznivě ovlivnit.
Jak bylo řečeno, práce má charakter observační studie, analýza dat byla provedena ve Švédském národním registru. První otázkou, kterou je nutno zvážit, je věrohodnost dat v souboru, z této stránky je odpověď pozitivní. Vlastní registr má řadu příznivých specifik: jeho vedení je pro lékaře předepisující léčivo povinné, je podporován řadou regulačních orgánů, synchronizován je s registrem úmrtí a s daty plátců péče. Jeho kvalita je odborníky považována za výbornou. Výhodou je také kompletnost dat, neboť ve Švédsku je užití nízkodávkové ASA vázáno na předpis. Do analýzy bylo zařazeno více než 600 000 osob ve věku od 40 let, které během prvního roku po preskripci (v rámci primární či sekundární prevence) užívaly ASA v dávce 75−160 mg denně (dominantně v rychle rozpustné formě) s nejméně 80% compliance. Lehce větší část probandů (54 %) byla léčena v rámci sekundární prevence. Celkový počet sledovaných let v riziku (time at risk − years) byl úctyhodný – 1,2 milionu, stejně tak byl dostatečně vysoký i počet kardiovaskulárních příhod během sledování (téměř 63 000). Otázka bezpečnosti léčby řešena nebyla, osoby s krvácením během sledování byly z analýzy vyloučeny. Tato stránka však není podstatná, na tomto místě se zabýváme účinností ASA i v současné době a efektem v rámci podskupin.
Během následujících let užívání ASA (medián byl 3 roky) asi 15 % účastníků registru léčbu přerušilo, resp. ukončilo z důvodů jiných nežli pro krvácení, zpravidla však bez racionálního důvodu. Prognóza této skupiny byla porovnávána s prognózou skupiny pokračující v léčbě. Celkem se objevilo téměř 63 000 příhod, jejich frekvence byla 4,2 % ročně, resp. ve skupině trvale léčené ASA 4,1 % a ve skupině, která ukončila léčbu z důvodů jiných, než je závažný nežádoucí účinek, 5,4 %.
Hlavní ukazatel efektu – velké
vaskulární příhody (fatální kardiovaskulární
příhoda i nefatální infarkt myokardu či iktus) – se
v celé skupině, která přerušila léčbu ASA, objevil
významně častěji, konkrétně o 37 % (poměr rizik
[HR] 1,37, interval spolehlivosti [CI] 1,34−1,41). Přerušení
léčby u probandů léčených v rámci prevence primární
mělo méně negativní dopad, vzestup počtu příhod činil 28 %
(HR 1,28, CI 1,22−1,34), zatímco v prevenci sekundární
představoval nárůst 46 % (HR 1,46, CI
1,41−1,51), viz graf 2.
Zvýšení výskytu cévních příhod po vysazení ASA bylo
největší během prvních 20 dnů, pokračovalo
však po celou dobu sledování.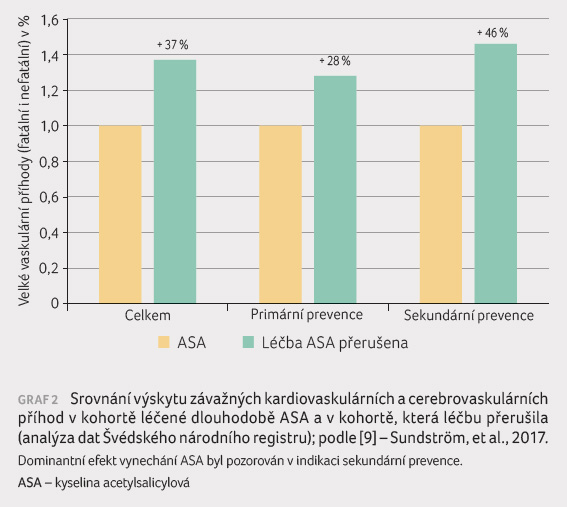
Vedle souhrnné analýzy celé kohorty je důležitá i analýza podskupin – zejména těch, u kterých je málo dokladů o efektu ze studií kontrolovaných, tj. u žen, seniorů v osmém a vyšším decenniu a u diabetiků. Zvýšené riziko aterotrombotických příhod po vynechání ASA v podskupinové analýze přetrvávalo. Nelišilo se při porovnání žen a mužů, mladších 70 let a starších, diabetiků a nediabetiků. Jednoznačně vyjádřený rozdíl byl při užití ASA v rámci primární a sekundární prevence, zde byl rozdíl statisticky i klinicky významný.
Pro analýzu věrohodnosti studie je významná otázka, zda též vynechání ASA s bezprostředním převedením na jiné antitrombotikum (jiné protidestičkové léčivo či antikoagulans) rovněž změní prognózu. Analýza ukázala, že změna antitrombotické strategie nezvýšila výskyt aterotrombotických komplikací, nález byl v souladu s očekáváním.
Shrneme li, pak s určitou nejistotou vyplývající z charakteru observační studie můžeme konstatovat, že ASA je stále účinná v primární a zejména v sekundární prevenci. V sekundární prevenci i v odstupu jednoho a více let po příhodě. Je účinná u žen, seniorů v osmém a vyšším decenniu a u diabetiků. Odpověď však není podána na otázku, jak je léčba bezpečná. Riziko krvácení řešeno nebylo. Zejména v prevenci primární, kdy je otázka bezpečnosti, resp. poměru účinnosti a bezpečnosti, klíčová, nám studie nedává odpověď na otázku celkového přínosu ASA v této indikaci.
Vedle odpovědi na výše uvedené otázky však vyvstala otázka nová: Není vysazení ASA spojeno s tzv. rebound fenoménem? Velká část příhod (konkrétní poměr ve studii neudán) se totiž objevila do 20 dnů po ukončení léčby. Na zodpovězení této otázky budeme muset ještě počkat.
Kdy indikovat léčbu ASA v prevenci aterotrombotické příhody aneb Koho léčit?
V jednom ohledu jsou data o účinnosti a bezpečnosti v primární i v sekundární prevenci konzistentní. Výskyt aterotrombotických příhod při léčbě ASA klesá o relativních 20 %, absolutní pokles se podle rizika liší. Riziko významného krvácení (velkého a život ohrožujícího) vzrůstá přibližně o absolutních 0,5−1 %. K dosažení klinického přínosu by měl být prospěch větší než riziko významného krvácení.
U nemocných se středně zvýšeným rizikem aterotrombotické příhody (tj. od 3−5% rizika vzniku příhody ročně) začíná být léčba ASA indikována. Poklesne li riziko vzniku ischemické příhody o pětinu, absolutní zisk se přiblíží 1 %, tj. převýší výskyt závažné hemoragické příhody. S takovýmto rizikem se setkáváme u nemocných s chronickými kardiovaskulárními či cerebrovaskulárními příhodami (po překonaném infarktu, s anginou pectoris, po iktu či po tranzitorní ischemické atace apod.), u nemocných s aterosklerotickým postižením v periferním řečišti (s ischemickou chorobou dolních končetin či s karotickým postižením) či v primární prevenci u velmi rizikových osob, např. u diabetiků s kumulací dalších rizikových faktorů, jakými jsou hypertenze, dyslipidemie a kouření. U nemocných s rizikem výrazně převyšujícím 5 %, zejména při akutních koronárních či ischemických mozkových příhodách a v prvních měsících po příhodě či u nemocných po intervenci v tepenném řečišti, je indikována duální protidestičková léčba kombinací ASA a blokátoru receptorů pro ADP.
Jaká dávka a jaká léková forma ASA má doložený efekt?
Otázka optimální dávky ASA je
významná, v Evropě preferujeme dávky v rozmezí
80−100 mg denně, resp. až 200 mg při akutním podání.
V USA jsou užívány dávky vyšší, 160−325 mg denně.
Důvody jsou spíše historické. Ve zmíněné analýze ATC
[6,7] je řešen vliv dávky na snížení morbidity
a mortality. Z tabulky 3 je patrné, že optimální data vykazují dávky
75−150 mg ASA denně, dávky nižší nemají efekt doložen.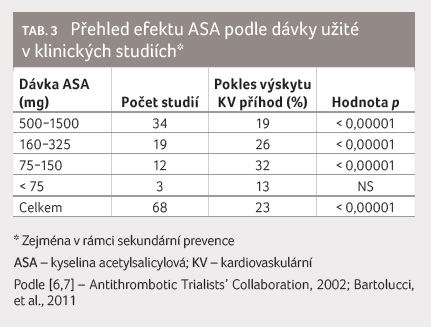
Zcela zásadní otázkou je výběr lékové formy ASA. Kyselina acetylsalicylová se jako slabá hydrofilní kyselina absorbuje v nedisociované formě, tedy v kyselém prostředí, při disociační konstantě 3,5, tedy při pH < 3,5. Takto kyselé prostředí je v žaludku a v proximálním duodenu. Biologická dostupnost je závislá na lékové formě a na aktuálním pH v žaludku. V klasické formě a při fyziologickém pH (< 3,5) je dobře absorbována do portálního oběhu. Nástup účinku je rychlý, do 20 minut. Vzhledem k tomu, že dále je ASA z rozhodující části v játrech transformována na kyselinu salicylovou, je maximální koncentrace ASA dosaženo v portálním oběhu. Zde probíhá vlastní efekt, tj. acetylace COX v trombocytu. Systémová expozice ASA je nízká, a v důsledku toho není dostatečná kapacita pro větší uplatnění acetylace COX. Při nitrožilním podání ASA nastupuje efekt během několika minut; poločas plazmatické eliminace je kolem 15 minut. Díky ireverzibilní blokádě COX však tento údaj není významný.
Při užití enterosolventních tablet
či při vzestupu pH (např. u osob léčených inhibitory
protonové pumpy) je ASA ve střevě z velké části
deacetylována esterázami (tzv. aspirinové esterázy) a absorbována
je převážně jako kyselina salicylová (obr. 3). Dostupnost aktivního metabolitu, zodpovědného
za antiflogistický účinek, tj. kyseliny salicylové, je
vysoká (kolem 80 %) a není výrazně závislá na lékové
formě a aciditě v žaludku. Kyselina salicylová je
eliminována zejména játry, poločas plazmatické eliminace je
variabilní, v dávkách užívaných k protidestičkovému
účinku je kolem dvou hodin, v dávkách antiflogistických
v desítkách hodin.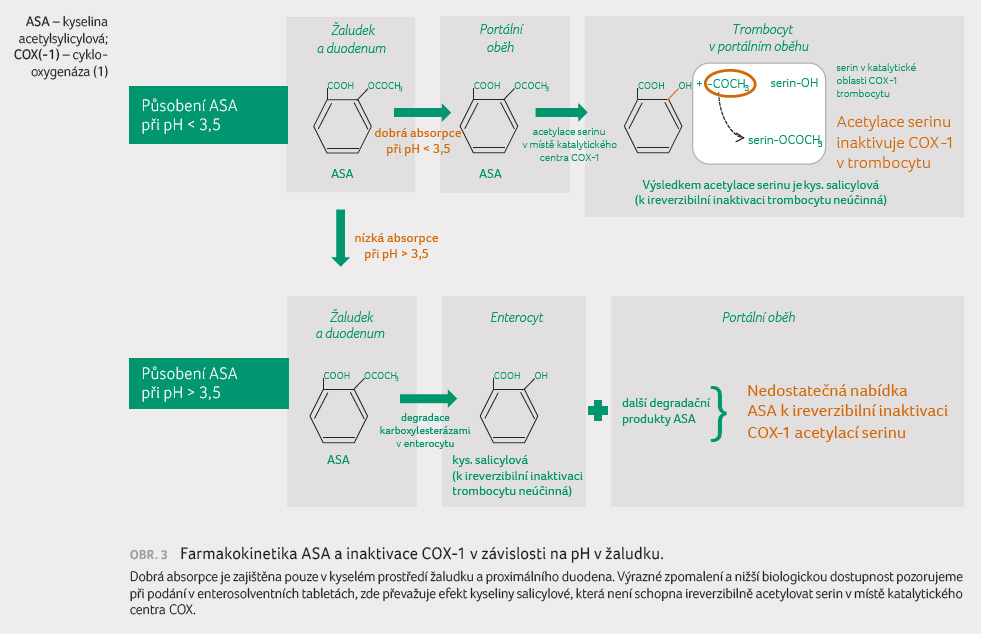
Až na výjimky byly do analýzy ATC zařazeny studie užívající pouze lékové formy ASA s normálním uvolňováním léčivé látky z tablety, a nikoliv formy enterosolventní. Doklad o účinnosti tedy platí pouze pro tuto „klasickou“ lékovou formu. Budeme li hodnotit efekt forem enterosolventních, pak vedle výhrad k biologické dostupnosti této lékové formy z čistě farmakologického hlediska je zásadním nedostatkem naprostá absence dokladu o klinické účinnosti. Máme publikované výsledky dvou studií provedených s enterosolventní ASA. První byla v primární prevenci – Japanese Primary Prevention Project, druhá u nemocných s asymptomatickou formou aterosklerotického postižení dolních končetin – studie Aspirin for Asymptomatic Atherosclerosis [10,11]. Obě práce doložily naprosto stejný efekt léčby enterosolventní ASA a placeba.
Megastudie ASPREE – Aspirin in Reducing Events in the Elderly (NCT01038583) – probíhala opět v indikaci prevence primární. Výsledky této randomizované studie u více než 19 000 seniorů sledovaných 6−7 let nebyly zatím in extenso zveřejněny. Nicméně podle tiskové zprávy organizátorů (National Institute on Aging) byla studie po sedmi letech ukončena pro absenci efektu (www.aspree.org). Podobně byla v roce 2016 ukončena studie ARRIVE (Aspirin to Reduce Risk of Initial Vascular Events), tentokrát pod taktovkou firmy Bayer (NCT00501059). V rámci dvojitě zaslepené studie porovnávající efekt enterosolventní ASA s placebem bylo hodnoceno více než 12 000 osob se středním rizikem. Výsledky zatím nebyly časopisecky zveřejněny, jsou však dohledatelné v registru evropských studií [12]. Primární ukazatele efektu ani ukazatele sekundární se v placebové a v intervenční větvi nelišily. Celková mortalita byla stejná – 2,55 % ve větvi s ASA proti 2,57 % ve větvi kontrolní. Velké vaskulární příhody typu MACE byly opět stejně frekventní (4,32 % vs. 4,51 %) a nelišil se ani výskyt všech karcinomů (4,02 % vs. 3,76 %) či kolorektálního karcinomu (0,48 % vs. 0,41 %). Tedy ani tato studie nedoložila efekt ASA v enterosolventní formě.
Jediná „pozitivní“ studie ISIS 2 u akutního infarktu myokardu, trvající bohužel jen čtyři týdny, sice deklarovala užití enterosolventní ASA, ale dle metodiky byly tablety před užitím rozkousány. Výsledkem, alespoň v prvních dnech, byla rychle rozpustná forma ASA.
Blíže je problematika enterosolventní formy ASA rozebrána jak z pohledu farmakologa/kardiologa, tak z pohledu farmakologa/farmaceuta v čísle 2 a 4 časopisu Remedia z roku 2017 [13,14].
Význam ASA v profylaxi karcinomu, zejména kolorektálního adenokarcinomu
V klinické medicíně se občas setkáme s milým překvapením – lék, který léta užíváme, se ukáže být přínosem i v jiné, neočekávané indikaci. Takováto milá překvapení „od starých přátel“ jsou skutečným „kořením“ suché vědy a doufejme, že jich bude stále více. Řečeno slovy velkého lékaře a ještě většího esejisty Lewise Thomase: „Největší překvapení medicíny leží ještě před námi, čekají zakopána do úrodné prsti budoucnosti, čekají, až je někdo vykope nebo až o ně zakopne, a to se dříve nebo později stane.“
Jedním z těchto překvapení je efekt ASA v nádorové chemoprofylaxi. Kyselina acetylsalicylová je jediným léčivem, kde její užití v rámci dlouhodobé profylaxe vzniku některých typů nádorů, zejména však karcinomu tračníku, uvádějí doporučené postupy v onkologii. Podávání ASA sice není určeno k samostatné „chemoprevenci“, ale jako významný bonus při indikaci protidestičkové léčby z důvodu profylaxe aterotrombotických příhod [15].
Význam ASA jako specifické nádorové prevence je prověřován řadou klinických studií. V současné době je předmětem zájmu porovnání účinnosti a bezpečnosti (zejména rizika krvácení) při podávání malých či velkých dávek ASA. Rozhodující megastudie fáze III, které mají zhodnotit chemoprofylaxi ASA v onkologických indikacích, probíhají. Výsledky řady z nich se očekávají ještě v tomto roce [16]. Doklady o pozitivním působení ASA jsou doloženy zejména pro kolorektální karcinom. Uvážíme li, že tento typ nádoru je třetím nejčastějším, pak pokles jeho výskytu v řádu desítek procent má velký klinický význam. Americké doporučení (U. S. Preventive Services Task Force) konstatuje dostatečné doklady o snížení incidence karcinomu tračníku po pěti až deseti letech podávání ASA [17]. Doporučení vychází z konzistentních výsledků více než 50 studií observačních i z řady studií randomizovaných (včetně jejich metaanalýz). Efekt byl pozorován jak v populaci se sporadickým výskytem kolorektálního adenomu a karcinomu, tak u nemocných s genetickým podkladem v rámci Lynchova syndromu. Analýza efektu dlouhodobé profylaxe malými dávkami ASA ve studiích typu případů a kontrol pozorovala významné snížení výskytu kolorektálního karcinomu o téměř 40 % (relativní riziko [RR] 0,62; 95% CI 0,58−0,67; p < 0,0001) [18]. V prevenci vzniku kolorektálního adenomu a karcinomu podáváním ASA není zásadní rozdíl v obecné nízkorizikové populaci a u Lynchova syndromu, tj. v populaci vysoce rizikové. Absolutní přínos však je v rizikové populaci výrazně vyšší, preventivní dlouhodobé podávání malých dávek ASA u Lynchova syndromu je v praxi výhodnější.
U ostatních typů nádorů trávicího traktu není situace tak jednoznačná, nicméně souhrnná analýza incidence všech nádorů traktu dokládá snížení jejich incidence o čtvrtinu (RR 0,76; 95% CI 0,66−0,88; p = 0,0003) [19]. V jiné metaanalýze hodnotící všechny typy gastrointestinálních nádorů byly výsledky ještě optimističtější (RR 0,62; 95% CI 0,55−0,70; p < 0,0001) [18].
V profylaxi karcinomu mammy kyselinou acetylsalicylovou je dostupná analýza dat ze souboru téměř milionu žen. Pozorován byl příznivý vliv ASA na snížení incidence nádoru, efekt byl výraznější při delším trvání léčby: po pěti letech expozice malým dávkám ASA poklesl výskyt o 14 %, po 10 letech o 27 % a po 20 letech o 46 % [20]. Z dalších typů nádorů máme pozitivní data zejména v profylaxi karcinomu prostaty. Celá řada dalších kontrolovaných chemopreventivních studií s ASA probíhá (ASPIRED aj.).
Pro posouzení přínosu
léčebného postupu, tedy i profylaxe nádorů podáváním
ASA, je nutno hodnotit nejen přínos, ale i riziko. Dominujícím
nežádoucím účinkem ASA je krvácení. V grafu 3A, B je uveden přínos podávání ASA, tedy pokles
výskytu aterotrombotických příhod a pokles výskytu všech
typů karcinomu, dále vzestup výskytu velkých krvácivých příhod,
a pak čistý klinický přínos (suma všech
příhod) u žen a u mužů ve věku 65−74
let. Je patrný obdobný přínos ASA u obou pohlaví, jen
u mužů je absolutní přínos větší (1% versus 2% pokles)
[21].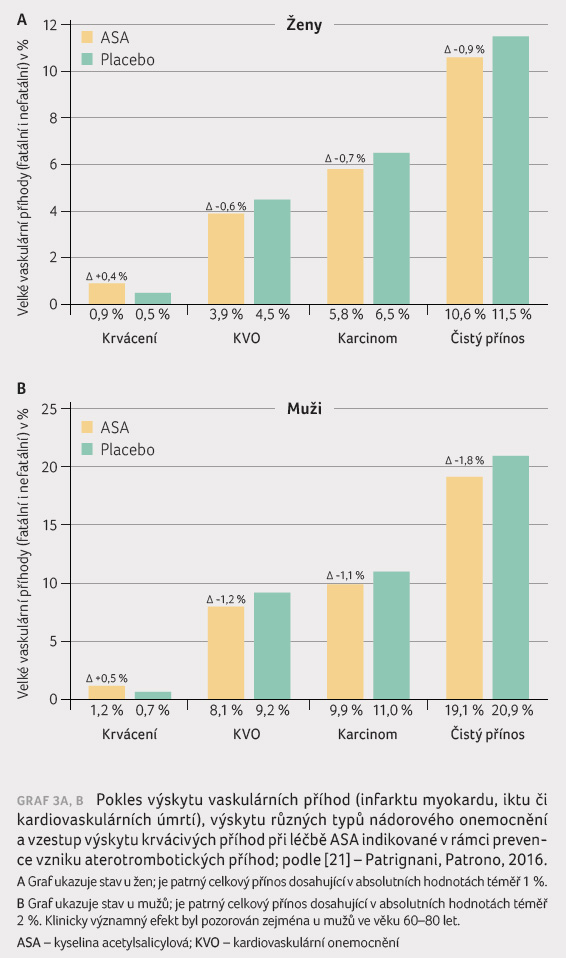
Shrneme li, pak protinádorové působení ASA při dlouhodobém podávání je vysoce pravděpodobné, v případě kolorektálního karcinomu je efekt jasně doložen a je reflektován i v doporučených postupech. Nicméně relativně vysoká frekvence významných hemoragií snižuje čistý klinický přínos. Racionální je tak profylaxe v rámci dvojí strategie – profylaxe aterotrombotických příhod a současně profylaxe onkologická. Pouze v případě hereditárního Lynchova syndromu je racionální samostatná dlouhodobá onkologická profylaxe – při poklesu výskytu kolorektálního karcinomu o více než 50 % a při jeho vysokém výskytu v této populaci je podávání ASA výhodné.
Co říci závěrem? Se stoupajícím věkem populace narůstá rovněž výskyt aterotrombotických příhod a onkologických onemocnění. Kolorektální adenokarcinom je jedním z nejvýznamnějších. Uvědomíme li si, že kyselina acetylsalicylová je léčivem, kterým můžeme zasáhnout na obou úrovních, pak na otázku položenou v úvodu musíme odpovědět kladně. Doufejme jen, že nám kyselina acetylsalicylová i v budoucnu přinese další milá překvapení.
Seznam použité literatury
- [2] Ajjan RA, Standeven KF, Khanbhai M. Effects of Aspirin on Clot Structure and Fibrinolysis Using a Novel In Vitro Cellular System. Arterioscler Thromb Vasc Biol 2009; 29: 712−717.
- [3] Bjornsson TD, Schneider DE, Berger H Jr. Aspirin acetylates fibrinogen and enhances fibrinolysis. Fibrinolytic effect is independent of changes in plasminogen activator levels. J Pharmacol Exp Ther 1989; 250: 154−161.
- [4] Kanani K, Gatoulis SC, Voelker M. Influence of Differing Analgesic Formulations of Aspirin on Pharmacokinetic Parameters, Pharmaceutics 2015; 7: 188–198.
- [5] Dachineni R, Kumar DR, Callegari E, et al. Salicylic acid metabolites and derivatives inhibit CDK activity: Novel insights into aspirin‘s chemopreventive effects against colorectal cancer. Int J Oncol 2017; 51: 1661−1673.
- [6] Antithrombotic Trialists’ Collaboration: Collaborative meta‑analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ 2002; 324: 71−86.
- [7] Bartolucci AA, Tendera M, Howard G, et al. Meta‑Analysis of Multiple Primary Prevention Trials of Cardiovascular Events Using Aspirin. Am J Cardiol 2011; 107: 1796–1801.
- [8] ESC Grand Debate: Aspirin for life, dostupné na: https://pace‑cme.org/2017/09/14/esc‑grand‑debate‑aspirin‑for‑life/
- [9] Sundström J, Hedberg J, Thuresson M, et al. Low‑Dose Aspirin Discontinuation and Risk of Cardiovascular Events A Swedish Nationwide, population‑Based Cohort Study. Circulation 2017; 136: 1183–1192.
- [10] Ikeda Y, Shimada K, Teramoto T, et al. Low‑dose aspirin for primary prevention of cardiovascular events in Japanese patients 60 years or older with atherosclerotic risk factors: a randomized clinical trial. JAMA 2014; 312: 2510‒2520.
- [11] Fowkes FG, Price JF, Stewart MC, et al. Aspirin for Asymptomatic Atherosclerosis Trialists, Aspirin for prevention of cardiovascular events in a general population screened for a low ankle brachial index: a randomized controlled trial. J Am Med Assoc 2010; 303: 841–848.
- [12] https://www.clinicaltrialsregister.eu/ctr‑search/trial/2006-
- [13] Bultas J, Karetová D. Enterosolventní forma kyseliny acetylsalicylové – ano, či ne? Remedia 2017; 27: 145−151.
- [14] Juřica J. Kyselina acetylsalicylová – galenické faktory ovlivňující antiagregační účinek. Remedia 2017; 27: 377−382.
- [15] Chan AT, Ladabaum U. Where Do We Stand With Aspirin for the Prevention of Colorectal Cancer? The USPSTF Recommendations. Gastroenterology 2016; 150: 14−18.
- [16] Patrono C. The multifaceted clinical readouts of platelet inhibition by low‑dose aspirin. J Am Coll Cardiol 2015; 66: 74–85.
- [17] Bibbins‑Domingo K, on behalf of the U.S. Preventive Services Task Force Aspirin Use for the Primary Prevention of Cardiovascular Disease and Colorectal Cancer: U.S. Preventive Services Task Force Recommendation Statement, Ann Intern Med 2016; 164: 836−845.
- [18] Algra AM, Rothwell PM. Effects of regular aspirin on long‑term cancer incidence and metastasis: a systemic comparison of evidence from observational studies versus randomised trials. Lancet Oncol 2012; 13: 518–527.
- [19] Ornelas A, Zacharias‑Millward N, Menter DG, et al. Beyond COX‑1: the effects of aspirin on platelet biology and potential mechanisms of chemoprevention. Cancer Metastasis Rev 2017; 36: 289–303.
- [20] Lu L, Shi L, Zeng J, et al. Aspirin as a potential modality for the chemoprevention of breast cancer: A dose‑response meta‑analysis of cohort studies from 857,831 participants. Oncotarget 2017; 8: 40389−40401.
- [21] Patrignani P, Patrono C. Aspirin and Cancer. J Am Coll Cardiol 2016; 68: 967–976.