Léčba aktinických keratóz
Souhrn:
Aktinická keratóza je často se vyskytující kožní léze vznikající na místech chronicky vystavených slunečnímu záření. Recentně je aktinická keratóza považována za carcinoma in situ spinocelulárního karcinomu. Léčebné metody užívané u aktinických keratóz můžeme dělit na invazivní – cílené na lézi, na farmakologické metody (ložiskově i plošně aplikované) a na fotodynamickou terapii. Nedílnou součástí péče o pacienty s aktinickými keratózami je fotoprotekce.
Key words: actinic keratosis – physical treatment – topical treatment – photodynamic therapy.
Summary:
Actinic keratosis is a frequent skin lesion, forming at areas chronically exposed to sun. Nowadays, actinic keratosis is considered carcinoma in situ of squamous cell carcinoma. Treatment options can be divided into physical – lesion directed, topical – lesion directed and field therapy, and photodynamic therapy. Integral part of actinic keratosis management is protection from sunlight.
Úvod
Aktinická keratóza (AK) je často se vyskytující kožní léze, která vzniká na místech chronicky vystavených slunečnímu záření. Prevalence onemocnění je 15–34 % u mužů a 6–18 % u žen ve věku 40–70 let [1], výskyt se zvyšuje s věkem. Mezi rizikové faktory, jež vedou ke vzniku AK, dále patří chronická expozice UV záření (opakované spálení na slunci zejména v dětství; životní styl – práce ve venkovním prostředí, opalování, rekreační aktivity), světlá kůže (fototyp I a II), mužské pohlaví, infekce lidským papilomavirem, imunologický stav (u příjemců transplantovaných orgánů stoupá riziko rozvoje AK až 250krát) a v neposlední řadě zeměpisná poloha. Austrálie je zemí, která leží blízko rovníku a žije zde vysoké procento populace se světlým typem pleti. Má zároveň nejvyšší prevalenci AK – u více než 60 % Australanů ve věku nad 40 let se AK objevuje [1]. Epidemiologické údaje hovoří o až osminásobném zvýšení počtu AK v populaci. Je to pravděpodobně důsledek globálního prodlužování věku, změny životního stylu (opálená kůže považována za krásnou, venkovní sporty, dovolené u moře) s prodlužováním chronické kumulativní expozice UV záření. S aktinickou keratózou jsou stále častěji konfrontováni nejenom dermatologové, ale i praktičtí lékaři. Stále více pacientů vnímá AK jako nežádoucí součást svého zevnějšku, ale mnohem závažnější je fakt, že na jejím podkladě může vzniknout spinocelulární karcinom (SCC).
Charakteristika onemocnění a klasifikace
Aktinická keratóza vzniká proliferací cytologicky atypických keratinocytů v epidermodermální junkční zóně. Morfologie těchto geneticky poškozených keratinocytů je identická s morfologickými změnami u SCC. Recentně je AK mnohými autory považována za carcinoma in situ. Podle míry invaze atypických buněk do epidermis lze AK rozdělit do tří tříd (keratinocytická intraepidermální neoplazie, KIN 1–3): 1. stupeň je charakterizován přítomností atypických buněk v dolní třetině epidermis, u 2. stupně nacházíme atypické buňky v dolních dvou třetinách epidermis, a pokud atypické keratinocyty prostupují celou tloušťku epidermis, mluvíme o AK 3. stupně [2].
Klinický obraz
Aktinické keratózy nacházíme na místech trvale exponovaných slunci. Především jsou to nos, spánky, čelo, temeno, uši, hřbety rukou a předloktí. Na kůži se projevují jako ostře ohraničené ploché papuly růžové, růžovofialové, hnědočervené až hnědožluté barvy se zhrubělým povrchem. Zpočátku jsou spíše hmatné než viditelné. Postupně se na povrchu tvoří šupinky, po jejichž stržení ložisko krvácí. S postupujícím časem dochází k zesílení léze a objevuje se hyperkeratotický povrch. Dle tloušťky lézí rozlišujeme AK tenké, střední a silné (AK I–III). Aktinické keratózy jsou obvykle vícečetné či mnohočetné a nacházejí se, jak již bylo uvedeno výše, v terénu kůže chronicky poškozené sluncem. Známkou solárního poškození jsou posuny pigmentu, atrofická tenká kůže, vrásky. „Field cancerization“ je termín používaný k označení přítomnosti mnohočetných (6 a více) nemelanomových kožních nádorů (nonmelanoma skin carcinoma, NMSC) nebo jejich prekursorů (AK) na částech lidského těla exponovaných slunci. Postiženi jsou především lidé s nízkým fototypem, imunosuprimovaní pacienti a pacienti po transplantacích. Koncept „field cancerization“ navrhl v roce 1953 Slaughter k popisu histologických abnormalit tkáně obklopující orální SCC, které by mohly přerůst v mnohočetné a rekurentní tumory. V roce 2003 koncept rozšířil Braakhuis, který popsal proces, při kterém se plochy geneticky pozměněných buněk vyvíjejí tak, aby vytvořily jeden nebo více tumorů v souvislém poli tvořeném preneoplastickými buňkami. Z konceptu vyplývá, že v oblastech, kde nacházíme známky slunečního poškození, jsou jednotlivé viditelné léze vždy obklopeny subklinickými lézemi. Protože nelze určit, kdy a které AK se změní v SCC, musejí být vždy léčeny všechny AK, včetně subklinických [3].
Diagnostika
K diagnostice AK většinou postačuje klinický obraz zahrnující lézi či vícečetné léze a známky solárního poškození kůže (posuny pigmentu, atrofická kůže, vrásky). Provádět biopsii s histologickou verifikací se doporučuje v případě ztluštění kůže, při přítomnosti ložiska většího než 1 cm, při infiltraci, v případě zánětlivých změn, ulcerace, krvácení, rychlého nárůstu, bolesti při palpaci, rychlé recidivy (do 2–3 měsíců od léčby), je‑li malá reakce na léčbu, perzistence po léčbě a u rizikových lokalit (červeň rtů, hřbety rukou, ušní boltce) [1].
Léčba
Budoucí chování AK nelze nikdy jednoznačně určit. Ve svém vývoji mohou spontánně regredovat, což se ale děje poměrně zřídka. Jindy mohou přetrvávat bez výraznějších změn nebo mohou progredovat do invazivního SCC (v 8–20 % případů), který již s sebou nese riziko metastazování a může vést i k úmrtí pacienta. Dle recentních poznatků je možná progrese do invazivního SCC jak u AK III. stupně, tak i u AK I. stupně. To, která léze bude progredovat do SCC, nejsme nikdy schopni určit. Smyslem a cílem léčby je tedy léčit všechny AK (klinické i subklinické formy), snížit pravděpodobnost vzniku nových projevů, snížit rekurenci onemocnění s prevencí přechodu do SCC. Faktory, které ovlivňují naše rozhodování o nejvhodnějším léčebném postupu, jsou typ, počet a velikost AK. Dále přihlížíme k celkovému zdravotnímu stavu pacienta (zejména imunosuprese), k jeho anamnéze předchozích kožních tumorů a úspěšnosti léčby, k věku. Důležité je též dbát na preference pacienta. Je třeba zohlednit bezpečnost léčby a nežádoucí účinky, stejně tak i ekonomickou dostupnost jednotlivých léčebných modalit. Neméně důležitá je ovšem i zkušenost lékaře s prováděním různých terapeutických postupů, stejně tak i možnosti a vybavení pracoviště.
Léčebné metody můžeme rozdělit do tří skupin:
- invazivní – cílené na lézi,
- farmakologické – ložiskově i plošně aplikované,
- fotodynamická terapie.
Mezi invazivní postupy patří chirurgická excize, kryoterapie, kyretáž + elektrokauter a dermabraze laserem. Tyto postupy volíme při ošetřování solitárních či málopočetných ložisek. Farmakologické metody zahrnují 5‑fluorouracil (5‑FU), 3% diclofenak v gelové formě s kyselinou hyaluronovou, 5% imiquimod, ingenol mebutát, lokální retinoidy a chemický peeling. Farmakologické metody spolu s fotodynamickou terapií lze využít pro ošetření jednotlivých lézí, ale i k léčbě mnohočetných ložisek, případně i k plošné terapii, která je žádoucí, zejména v případech tzv. field cancerization. Z výše uvedených léčebných možností není v České republice (ČR) dostupný 5‑FU, 3% diclofenak s kyselinou hyaluronovou a lokální retinoidy.
Invazivní léčebné metody
Chirurgická excize je vhodná pro ložiska AK podezřelá z přechodu do SCC vzhledem k možnosti následné histologické verifikace. Nevýhodou je nutnost anestezie a vznik jizev. Kryodestrukce představuje nejčastější metodu volby (60 %) využívající tekutý dusík ve spreji či v kontaktní aplikaci. Jedná se ovšem o nespecifickou terapii, dochází při ní k destrukci nejenom dysplastických, ale i normálních zdravých buněk. Výhodou kryodestrukce je, že jde o levnou metodu, rychle a jednoduše proveditelnou, s vysokou účinností dosahující 70–90 %, s výskytem recidiv 2–12 % do jednoho roku [1]. Nevýhodou je, že neexistuje jednotná standardizace léčby (není pevně stanoven počet ošetření, délka aplikace dusíku, teplota). Kryodestrukci nelze používat plošně, často dochází ke vzniku hypopigmentovaných jizev.
Kyretáž s následnou elektrokoagulací je metoda, kterou lze výše zmíněnou kryalizaci nahradit. Jejími výhodami jsou rychlost provedení a současné stavění krvácení. Lasery CO2 a Er:YAG v ablativním modu lze k léčbě AK využít, ale účinnost této metody nebyla prokázána žádnou studií. Nevýhodou jsou vysoké náklady, nutnost anestezie, změny pigmentace, jizvení.
Farmakologické metody
Pro léčbu tenkých a středně silných AK zaujímajících plochu maximálně 25 cm2 lze využít 5% imiquimod v krému. Jedná se o selektivně působící lokální modifikátor imunitní reakce, jehož antivirotické a antitumorózní účinky jsou dány stimulací imunitního systému kůže. Mechanismus účinku je založen na vazbě imiquimodu na toll‑like receptory (TLR), a to na sedmý podtyp tohoto receptoru (TLR‑7) na imunitních buňkách kůže. Po vazbě imiquimodu na TLR‑7 dochází k aktivaci tohoto receptoru s následnou indukcí transkripčního faktoru NF‑κB a s produkcí prozánětlivých cytokinů (IFNα, INFγ, TNFα, IL‑1, IL‑6, IL‑8, IL‑10, IL‑12), které jsou zodpovědné za komplexní antivirový a antitumorózní účinek. Krém s obsahem imiquimodu se aplikuje 3× týdně po dobu čtyř týdnů, následuje čtyřtýdenní přestávka, vyhodnocení účinku léčby, případně další cyklus. Výhodou léčby imiquimodem je dobrá účinnost – úplné nebo částečné vymizení projevů u 64,5 % pacientů po prvním cyklu a u 85,4 % pacientů po druhém cyklu terapie [4], dále cílenost léčby – působí na dysplastické buňky jak u klinicky zjevných, tak u subklinických (okem nedetekovatelných) lézí, má dobrý kosmetický efekt. Je tedy vhodný k léčbě mnohočetných AK zejména v obličeji a na vertexu pleši. Pacient si může krém aplikovat dle návodu sám doma. Nevýhodou této léčby jsou časté lokálně iritační reakce (erytém, edém, krusty, pálení), zřídka se vyskytující systémové projevy (myalgie, nevolnost, nauzea) a délka aplikace.
Novinkou ze spektra léčiv určených k léčbě AK je ingenol mebutát. Jedná se o molekulu izolovanou z běžně se vyskytující rostliny pryšce okrouhlého. Ve výrobě se však používá šťáva z rostlin, které se speciálně pro tento účel pěstují v australském Queenslandu. Pro léčbu AK byl ingenol mebutát schválen americkým Úřadem pro potraviny a léky (Food and Drug Administration) v roce 2012, a to v koncentraci 0,015 % na AK v oblasti obličeje a kštice s doporučenou aplikací 1× denně po tři po sobě jdoucí dny. Pro AK vyskytující se na trupu a končetinách je používán ingenol mebutát o koncentraci 0,05 % s aplikačním schématem 1× denně po dva dny, tento přípravek není ale v České republice k dispozici. Mechanismus účinku je duální. Jednak ingenol mebutát způsobuje poškození buněčných membrán, včetně membrán mitochondrií, což vede k nekróze buněk. Dále pak aktivuje B‑lymfocyty k tvorbě cytotoxických protilátek, jež se vážou na povrch dysplastických buněk, a následně dochází k infiltraci lézí neutrofily s uvolněním prozánětlivých cytokinů. Výhodou léčby ingenol mebutátem je zejména velmi krátká doba aplikace a dobrá účinnost, k úplnému zhojení po dvou měsících od ukončení terapie dochází u 42 % léčených [5]. Nevýhodou je omezená plocha aplikace (do 25 cm2) a iritační reakce (erytém, deskvamace, krusty, svědění, bolest), jež se hojí během 2–4 týdnů.
Pro úplnost je nutné také uvést dva přípravky, jež v ČR na trhu nejsou, a to 5% 5‑fluorouracil, indikovaný pro mnohočetné středně silné AK, a 3% diclofenak ve 2,5% hyaluronátovém gelu s indikací pro tenké mnohočetné AK s možnou plošnou aplikací. Prvně uvedený 5% 5‑fluorouracil je lokální chemoterapeutický antimetabolit, způsobuje inhibici syntézy DNA a zastavuje tak dělení buněk. Aplikuje se 2× denně po dobu 2–4 týdnů, což bývá provázeno silnou lokální reakcí (erytém, krusty, eroze, ulcerace), a tím i sníženou compliance pacientů. Druhý přípravek – 3% diclofenak v gelu 2,5% kyseliny hyaluronové – je inhibitorem cyklooxygenázy, způsobuje inhibici syntézy prostaglandinů, čímž negativně ovlivňuje růst nádorových buněk a neovaskularizaci. Doporučené dávkování je 2× denně po dobu 60–90 dní, léčba je pacienty velmi dobře tolerována, účinnost je udávána od 31 % do 47 % po 2–3 měsících od léčby [1].
U imunosuprimovaných pacientů, u pacientů po transplantaci či u pacientů s mnohočetným výskytem NMSC je využíván antiproliferační a prodiferenciační účinek systémově podávaného acitretinu v dávce 20–30 mg denně, tato chemoprofylaxe NMSC je účelná a účinná.
Fotodynamické terapie
Fotodynamická terapie je moderní neinvazivní cílená léčba s využitím fotosenzibilizátoru – methylesteru kyseliny δ‑aminolevulové. Spočívá v lokální aplikaci přípravku na ošetřovanou lézi (vychytáván je přednostně buňkami s vyšší metabolickou aktivitou) s následným ozářením viditelným světlem (červené světlo o vlnové délce 630 nm) za přítomnosti kyslíku. V léčbě AK I. a II. stupně lze uplatnit jednak klasický postup, také ovšem tzv. day‑light photodynamic therapy (DL‑PDT), který využívá k aktivaci fotosenzibilizátoru denní světlo (tento postup je již běžně používán ve státech jižní a západní Evropy, v ČR dosud schválen nebyl). Fotodynamickou léčbu užíváme pro ošetření jednotlivých lézí (se středním stupněm doporučení), ale zejména také pro léčbu mnohočetných AK a pro plošné ošetření (zde s vysokým stupněm doporučení). Dle Souhrnu informací o přípravku Metvix® jsou schválena dvě léčebná ošetření v odstupu tří měsíců. Úspěšnost léčby je hodnocena po třech měsících uplynulých od druhého léčebného sezení a je udávána v rozsahu 59–91 % [7]. Výskyt recidiv po 12 měsících od ukončení terapie je uváděn asi v 17 % [8]. Mezi nejčastější nežádoucí účinky fotodynamické terapie patří bolestivost, erytém a tvorba krust.
Fotoprotekce
Nedílnou součástí péče o pacienty s AK je fotoprotekce a neustálá edukace o ní. Spočívá ve správném chování – nevystavovat se slunci mezi 10.–14. hodinou, nosit vhodné oblečení – dlouhé kalhoty, košile či trička s dlouhými rukávy a klobouk se širokou krempou. Dále doporučujeme aplikovat dostačující množství lokálně širokospektrých extern s filtry v UVB i UVA oblasti UV záření (sunscreeny redukují množství mutací p53 indukovaných UV zářením a snižují imunosupresivní účinky UV záření). Denní používání sunscreenu snižuje tvorbu nových AK a zvyšuje množství remisí již existujících projevů AK v porovnání s vehikulem [6].
Závěr
Vzhledem ke zvyšujícímu se výskytu aktinických keratóz v populaci a k jejich možnému přechodu do invazivního spinocelulárního karcinomu nabývá tato problematika a zvláště terapeutický přístup stále na významu. Volba terapie je dána zejména množstvím lézí. Pro jednotlivé AK lze využít metody invazivní, z nichž v ČR dominuje kryalizace, pro mnohočetné léze a případné plošné postižení lze volit metody neinvazivní – farmakologické – či fotodynamickou léčbu. Jejich účinnost je srovnatelná, liší se délkou aplikace a závažností nežádoucích účinků. Pro indikaci aktinická keratóza však nejsou ze zdravotního pojištění hrazeny. Takže do rozhodovacího schématu určitě zasahuje i cena jednotlivých přípravků. V léčbě a zejména v prevenci AK nesmí být opomíjena účinná fotoprotekce.
Kasuistika
U pacientů s mnohočetnými aktinickými keratózami, které se nacházejí v solární lokalizaci (obličej, výstřih, ramena, hřbety rukou a předloktí), často kombinujeme více terapeutických metod. Takto jsme postupovali 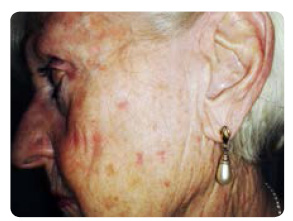 i u pacientky sledované na naší klinice od roku 2008. Jedná se o 78letou ženu fototypu I–II, která v mládí a ve středním věku trávila letní dovolenou u moře, často také pracovala na zahrádce. Fotoprotekci nepoužívala. Byla odeslána sektorovou dermatoložkou k léčbě mnohočetných aktinických keratóz v oblasti obličeje, výstřihu, ramen a na hřbetech rukou (obr. 1).
i u pacientky sledované na naší klinice od roku 2008. Jedná se o 78letou ženu fototypu I–II, která v mládí a ve středním věku trávila letní dovolenou u moře, často také pracovala na zahrádce. Fotoprotekci nepoužívala. Byla odeslána sektorovou dermatoložkou k léčbě mnohočetných aktinických keratóz v oblasti obličeje, výstřihu, ramen a na hřbetech rukou (obr. 1).
V prvním kroku jsme pacientku poučili o důsledné fotoprotekci. Většina aktinických keratóz byla léčena opakovaně kryalizací, aktinické keratózy III. stupně – silné (1× ve výstřihu a 1× na pravé paži) – byly excidovány s histologickým závěrem: aktinická keratóza s výraznou hyperkeratózou typu cornu cutaneum. V roce 2010 byla provedena jedna kúra fotodynamické terapie s plošným ošetřením mnohočetných ložisek ve výstřihu, další kúru pacientka pro finanční náročnost odmítla. Ze zdravotního pojištění není totiž léčba aktinických keratóz pomocí fotodynamické terapie hrazena.
V roce 2011 byl při kontrole odhalen a následně i histologicky verifikován bazocelulární karcinom u vnitřního koutku pravého oka. Provedená excize byla kompletní a ložisko zůstává i recentně bez známek recidivy. V letech 2011–2015 byly stále nově vznikající aktinické keratózy ošetřovány pomocí tekutého dusíku. Vzhledem k množství ložisek a vzhledem k rozsáhlému plošnému postižení však tato léčba nebyla pacientkou dobře tolerována. Po kryalizaci se ložiska dlouho hojila, vznikaly krusty a následně i hypopigmentované jizvy. Proto byl pacientce doporučen 3% diclofenak v gelu kyseliny hyaluronové k plošnému ošetření ložisek v obličeji. Pacientka si přípravek zakoupila v Rakousku a začala jej aplikovat od března 2015. Účinek léčby byl však pouze částečný, proto jsme se rozhodli přistoupit k další kúře metodou fotodynamické terapie po předchozím schválení methylesteru δ‑aminolevulové kyseliny revizním lékařem. V říjnu 2015 byla provedena první kúra a po třech měsících pak druhá kúra fotodynamické terapie plošně na oblast výstřihu a na ložiska na pravé tváři. Aktinické keratózy ve výstřihu se zhojily, hojení lézí na pravé tváři bylo protrahované vzhledem k závažnější lokální reakci s macerací a s tvorbou krust. Výsledný léčebný účinek byl však velmi dobrý, všechny aktinické keratózy byly zhojeny.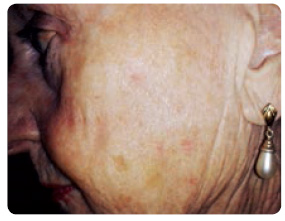
V březnu 2015 jsme se rozhodli využít k léčbě ložisek na levé tváři nový přípravek – ingenol mebutát. Pacientka aplikovala gel na doporučovanou plochu 25 cm2 po tři po sobě jdoucí dny. Ihned po aplikaci jsme zaznamenali lokální iritační reakci mírného stupně se zarudnutím a s tvorbou šupin, ta ale rychle odezněla a při kontrole po měsíci od podání byla všechna ošetřovaná ložiska zhojena (obr. 2). Pacientka byla opět poučena o fotoprotekci a dochází na pravidelné kontroly.
Seznam použité literatury
- [1] Dréno B, Amici JM, Basset Seguin N, et al. Management of actinic keratosis: a practical report and treatment algorithm from AKTeam expert clinicians. J Eur Acad Dermatol Venereol 2014; 28: 1141–1149.
- [2] Poláková K. Účinky topického imunomodulátoru (imiquimodu) v liečbe aktinickej keratózy. Dermatológia pre prax 2009; 3: 148–150.
- [3] Malvehy J. A new vision of actinic keratosis beyond visible clinical lesions. J Eur Acad Dermatol Venereol 2015; 29 (Suppl. 1): 3–8.
- [4] Stockfleth E, Sterry W, Carey Yard M, Bichel J. Multicentre, open label study using imiquimod 5% cream in one or two 4 week courses of treatment for multiple actinic keratoses on the head. Br J Dermatol 2007; 157 (Suppl 2): 41–46.
- [5] Lebwohl M, Swanson N, Anderson LL, et al. Ingenol mebutate for actinic keratoses. N Engl J Med 2012; 366: 1010–1019.
- [6] Pizinger K. Kožní maligní epitelové nádory. Referátorový výběr z dermatovenerologie 2007; 1 (speciál): 18–23.
- [7] Freeman M, Vinciullo C, Francis D, et al. A comparison of photodynamic therapy using topical methyl aminolevulinate (Metvix) with single cycle cryotherapy in patients with actinic keratosis a prospective, randomized study. J Dermatolog Treat 2003; 14: 99–106.
- [8] Braathen LR, Paredes BE, Saksela O, et al. Short incubation with methyl aminolevulinate for photodynamic therapy of actinic keratoses. J Eur Acad Dermatol Venereol 2009; 23: 550–555.