Moderní přístupy v hojení chronických ra
Souhrn:
Chronické, nehojící se rány se dostávají v posledním desetiletí do popředí zájmu zdravotníků, ale i laické populace. Představují velký socioekonomický problém, který prostupuje celou společností, postihuje muže i ženy různých věkových kategorií. Do léčebného procesu vstoupily nové moderní terapeutické metody a farmaceutický trh nabízí řadu materiálů vlhké terapie. Nejčastější chronickou ránou ve spektru našich pacientů je ulcerace venózní etiologie. V článku jsou uvedeny terapeutické možnosti se zaměřením na prostředky vlhké terapie, kdy jsou zmíněny základní skupiny krytí, jejich specifika, vlastnosti, indikace a praktické využití. Podstatnou a nezastupitelnou roli v léčbě hraje dále kompresivní terapie, farmakologická léčba (venotonika), chirurgická léčba a režimová opatření.
Key words: chronic wounds – venous insufficiency – modern dressing materials – compression therapy.
Summary:
Chronic, non‑healing wounds have been at the center of attention of both medical experts and the general public during the last decades. They represent a significant social and economic burden, affecting both genders across all age groups. New advanced therapeutic methods have been introduced into the treatment process. Additionally, the pharmaceutical market offers a variety of moist therapy material. Venous ulcers are the most common chronic wounds in the spectrum of our patients. The article contains information concerning therapeutic possibilities focused on moist wound healing and mentions different types of wound dressings, their specifics, characteristics, indications, and practical applications. Compression therapy, together with pharmacological treatment (venotonics), surgical treatment, and life style changes all play an essential role in chronic wound management.
Úvod
Chronická rána představuje pro každého člověka dyskomfort a mnohdy velmi těžko zvládnutelný problém. Pacienta i v současné době plné pokroku a výdobytků moderní doby v řadě ohledů handicapuje a znamená socioekonomický problém nejen pro každého individuálního jedince, ale i pro celou společnost. Celý diagnosticko terapeutický proces je skutečným během na dlouhou trať a vyžaduje naprostou spolupráci a ukázněnost pacienta, zapojení rodiny, plnou erudici a empatii zdravotnického personálu a samozřejmě dostupnost a znalost všech léčebných modalit a zdravotnických prostředků a materiálů. Neobejdeme se bez vzájemné souhry a jisté formy nadšení všech členů multioborového týmu, který se podílí na léčbě daného jedince. Jsme si vědomi skutečnosti, že v péči o osoby s chronickou ránou neexistuje univerzální návod a postup, který je možno považovat vždy za efektivní. Jednoznačně existují „návody“ umožňující postupy lege artis s vědomím účinné odborné pomoci a minimalizace rizik pro pečující i nemocné [1].
Výskyt chronických ran v populaci dosahuje l−2 %, postižena jsou bez rozdílu věku obě pohlaví. Skupina chronických ran je různorodá. Definujeme ji jako defekty, které se přes adekvátní terapii nezhojily do 6–9 týdnů. Tato definice vznikla na základě konsenzu odborníků České společnosti pro léčbu rány. Mezi nejčastější rány a defekty patří ulcerace venózní, arteriální či smíšené etiologie, syndrom diabetické nohy, poúrazové defekty, dekubity, dehiscence operačních ran, nehojící se popáleniny či omrzliny, defekty v terénu lymfedému, tumorózní rány a jiné.
S nehojícím se defektem se v průběhu praxe jistě setká každý zdravotník, ale i laik. Zvyšující se incidence chronických ran v populaci souvisí s nárůstem výskytu civilizačních chorob, jako jsou ateroskleróza, diabetes mellitus či chronická žilní insuficience.
Vývoj léčebných metod
Počátky moderní tzv. vlhké terapie se datují do roku 1962 a jsou spjaty se jménem George Wintera. V posledních desetiletích došlo k výrazným změnám. Na trh a do léčebného sortimentu vstoupila řada nových krycích materiálů. Dnes již můžeme hovořit o stovkách produktů, které nabízí farmaceutický průmysl. Tyto moderní prostředky, používané v léčbě především chronických ran, mají různou konzistenci, materiálové složení a z toho rezultující účinek [2].
Mezi další metody dnes již běžně využívané na řadě (nejen) chirurgických pracovišť řadíme aplikaci systému V.A.C. (působení řízeného podtlaku na ránu) či larvoterapii.
V débridementu neboli v očistě rány nesmíme zapomenout na možnost využití standardní chirurgické nekrektomie či exkochleace, na aplikaci chemických či enzymatických prostředků. Mezi nové techniky řadíme ultrazvukový débridement a hydrochirurgický débridement.
Správné použití jednotlivých modalit vyžaduje znalost procesu hojení ran, složení a účinku jednotlivých prostředků. Pokud dané léčebné prostředky indikujeme adekvátně, zkrátíme celkovou dobu hojení, snížíme frekvenci převazů u pacienta, redukujeme bolest a stres, zlepšíme kvalitu života a v konečném důsledku šetříme i finanční prostředky.
Neméně podstatnou skutečností je zachování fyziologického prostředí v ráně, a to adekvátní vlhkosti a teploty, klidu a zajištění reparačních procesů. Díky moderním prostředkům hojení ran je naprosto nežádoucí každodenní zásah a traumatizace rány, dovolím si říci, že jsou již dávnou minulostí převazy třikrát denně za využití různých balzámů a aromatických roztoků. Je nutné si uvědomit fakt, že po každém zásahu rána až 8 hodin stagnuje a musí opět nastartovat sérii hojivých procesů.
Z výše uvedených faktů vyplývá i jednoznačná časová úspora práce zdravotnického personálu, což může být jistým přínosem pro řadu zdravotnických zařízení, která se mnohdy potýkají s nedostatkem lékařů a sester.
Specifikace a terapie ulcerací venózní etiologie
Bércové ulcerace obecně tvoří
nejpočetnější skupinu z celkové množiny nehojících se
ran. Nejčastější jsou ulcerace venózní etiologie (obr. 1). V sestavě pacientů naší ambulance představují
minimálně 70 %. Kučera, který ve spolupráci s Českou
společností podpory zdraví realizoval v rámci edukačního
programu „Hojení 21“ populační šetření zaměřené
na odhalení prevalence bércových vředů v ČR,
předpokládá, že bércovými vředy aktuálně trpí nebo
v minulosti trpěla více než 3 % obyvatel starších 18 let.
V reálných číslech tato procenta znamenají, že bércovým
vředem je aktuálně postiženo kolem 150 000 dospělých
obyvatel ČR a dalších zhruba 130 000 onemocnění
bércovým vředem prodělalo [3].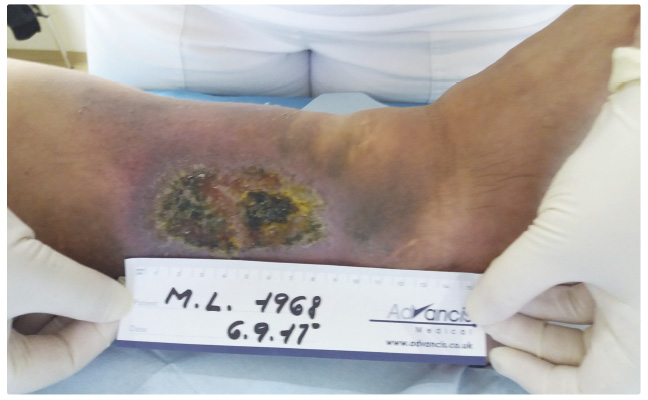
Venózní bércová ulcerace vzniká v terénu chronické žilní insuficience, kdy krev v oblasti dolních končetin stagnuje při žilní hypertenzi, případně jako důsledek posttrombotického syndromu. Mnohdy však stačí i drobné trauma či štípnutí hmyzem, kdy v terénu se špatnou trofikou lehce vznikne rozsáhlé poškození.
Defekt je nejčastěji lokalizován v oblasti mediálního kotníku, ale může se vyskytovat kdekoliv na bérci. Klinicky je patrný edém končetiny, hnědá hemosiderinová pigmentace, vazivová kožní indurace; defekty jsou často mapovité, nezřídka s dermatitidou v okolí vředu.
V terapii pacientů s ulceracemi žilní etiologie platí „pravidlo tří“, tj. nastavit správnou vlhkou terapii dle charakteru rány, zejména dle spodiny rány, zajistit adekvátní elastickou kompresi a dále venotonickou farmakoterapii.
V úvodu ošetření chronické rány (jakékoliv etiologie) by měl být aplikován obklad s dekontaminačním roztokem alespoň na 15 minut. Roztoky obsahují polyhexamid a betain, demineralizovanou vodu a 0,1% etylhexylglycerin či se jedná o superoxidované roztoky. U mobilních pacientů ideálně po předchozí sprše vlažnou vodou bez mýdla či šamponu, která nám zároveň zajistí mechanickou očistu a určitou formu masáže v ráně. Roztoky mají široký antibakteriální účinek včetně působení na kmeny meticilin rezistentního St. aureus (MRSA) a dokáží významně snížit mikrobiální zátěž.
Po této proceduře by měl následovat débridement, kdy zbavíme ránu povlaků, nekróz, koagul či zbytků předchozích převazových materiálů. Débridement musí být účinný a efektivní, ale zároveň šetrný, aby nedocházelo ke zbytečné traumatizaci rány. Nejčastěji jako chirurgové využíváme mechanický débridement (nůžky, skalpel, exkochleační lžičky), ale i chemický (různé formy gelů, jako jsou hydrogel s alginátem, gel s Ringerovým roztokem či oktenidinem, mezi přípravky jmenujme například Prontosan Wound gel X, Nu gel, Hydrosorb gel, Octenilin či Microdacyn gel aj.) nebo enzymatický. K dispozici je nám podtlaková terapie či larvoterapie nebo hydrochirurgie.
Dále volíme vhodný materiál z prostředků vlhké terapie dle charakteru spodiny rány. Řídíme se fází hojení rány, množstvím a druhem exsudátu, zápachem, lokalitou rány, charakterem okolí rány, bolestí v ráně a dostupností převazových materiálů. V současné době je na trhu k dispozici převazový materiál minimálně od 36 výrobců. Prostředky jsou volně prodejné ve zdravotnických potřebách či lékárnách, nebo je může pacientovi předepsat lékař – chirurg, internista, dermatolog, angiolog, diabetolog, ale i praktický lékař. Ovšem podléhají schválení revizního lékaře příslušné zdravotní pojišťovny. Většina přípravků vlhké terapie je v tomto případě hrazena plně, ale např. gely či obkladové/oplachové roztoky jsou hrazeny ze 75 % (25 % tvoří doplatek pacienta).
Materiály vlhké terapie
V dalším textu jsou probrány základní skupiny materiálů vlhké terapie, jejich indikační kritéria a možnosti využití.
Hydrokoloidní krytí
Hydrokoloidní krytí patří k nejstarším obvazům nové generace [2]. Jsou to primární krytí na ránu okluzivního typu. Tvoří je dvě vrstvy – zevní pěnová pro vodu nepropustná polyuretanová hmota a vnitřní neboli absorpční vrstva, která obsahuje hydrokoloidní polymerový komplex želatiny, pektin a karboxymetylcelulózu [2,4]. Existují různé formy krytí – hydrokoloidy s lepivým okrajem či bez něj, ve formě pasty či prášku, nebo hydrokoloidy s doplňky, dále hydrokoloidy – hydrovlákna (hydrofiber). Při kontaktu krytí s ranným exsudátem se na povrchu rány vytvoří gel, který je po sejmutí obvazu často mylně považován za hnis. Lze jej snadno odstranit oplachovým roztokem. Hydrokoloidy stimulují tvorbu granulační tkáně a angiogenezi. Rovněž podporují autolytický débridement. Používají se zejména k ošetřování ran ve fázi granulace bez zjevných známek infekce s nízkou až střední sekrecí [4]. Frekvence převazů se řídí intenzitou sekrece, mohou být ponechány na ráně až 7 dnů, ale v praxi nejčastěji převazujeme v rozmezí 3−4 dnů. Vyčerpání absorpční kapacity krytí se projeví „tvorbou puchýře“ v centru krytí, což představuje indikaci k převazu [2].
Antiseptická neadherentní krytí
Antiseptická neadherentní krytí mají svoje využití nejen v terapii chronických, nehojících se ran, ale i v akutní traumatologii či na operačních sálech nebo jako profylaktické ošetření invazivních vstupů. Jde o skupinu neadherentních mřížek impregnovaných antiseptickou látkou – jod povidonem, medem, stříbrem či chlorhexidinem. Kryty neabsorbují exsudát [4], musíme tedy správně vybrat vhodnou ránu, abychom zabránili okolní maceraci, a rovněž se cíleně ptát pacientů na alergie, zejména u jodových přípravků. Existuje možnost systémových účinků při absorpci účinné látky z krytí, proto je nutné omezit dlouhodobou aplikaci u novorozenců, těhotných či kojících žen a specificky u tyreopatiků. Aplikace jednoho typu antiseptického krytí se doporučuje maximálně po dobu 21 dnů [4]. Frekvenci převazů volíme obvykle v rozmezí 2−7 dnů dle množství ranné sekrece a stavu spodiny rány. Krytí jsou vhodná zejména pro povrchové rány.
Hydroaktivní krytí aneb hydroterapie
Hydroaktivní krytí aneb hydroterapie je oblíbenou a zejména v horkém létě hojně využívanou skupinou materiálů se superabsorpčním jádrem aktivovaným Ringerovým roztokem. Akrylát v savém jádru má vyšší afinitu pro ranný sekret. To umožňuje výměnu Ringerova roztoku ven a sekretu z rány dovnitř polštářku, včetně toxinů, tkáňové drtě a mikroorganismů [4]. Využíváme jej v terapii granulujících, ale i povleklých a nekrotických ran, ran hlubokých i povrchových. Krytí měníme zpravidla po 24 hodinách.
Hydrogelová krytí
Hydrogelová krytí jsou trojdimenzionální struktury sestávající především z polymerů nebo kopolymerů s vysokým obsahem vody. Patří mezi hydrofilní prostředky [2]. Mohou být čisté nebo s doplňky – algináty, pektiny, NaCl, medem aj. Jsou vyráběny ve formě kompaktní (s lepivým okrajem nebo bez lepivého okraje) nebo ve formě amorfní (hydrogely v tubě). Hydrogely jsou schopny rehydratovat suchou tkáň, na druhé straně absorbují sekret z exsudujících ran. V ráně upravují optimální vlhkost, autolyticky odstraňují nekrózy a fibrinové povlaky na spodině defektu. Vůči zdravým buňkám tkáně se chovají intaktně. Podporují tvorbu granulační tkáně a následně fázi epitelizační. Gely aplikujeme striktně do defektu, abychom zabránili maceraci okolní zdravé kůže, a sekundárně je kryjeme neadherentní mřížkou, transparentním filmovým krytím či pěnovým krytím. Rány převazujeme nejčastěji každé 2−3 dny. Přechodně může dojít i ke zvětšení defektu při vyčištění nekróz a k přesmyku do granulační fáze hojení. Tyto materiály patří mezi velmi oblíbené pro svoji vysokou účinnost, poměrně rychle a jasně viditelný efekt a snadnou manipulaci.
Pěnová krytí
Pěnová krytí tvoří bohatou skupinu převazových materiálů, základem je polyuretanová pěna s vysokou absorpční schopností. Některá krytí jsou jednoduchá, jiná vícevrstvá. Materiály jsou měkké, dobře formovatelné a snadno se přizpůsobí i kavitám a anatomicky obtížným lokalitám. Vyrábějí se s adhezivním okrajem nebo bez něj. Tyto materiály využíváme nejen jako krytí terapeutické, ale i jako krytí profylaktické, např. v antidekubitní prevenci v inkriminovaných partiích, jako jsou sakrum, paty, lokty a ušní boltce. Některé výrobky jsou na vnitřní straně opatřeny neadherentní silikonovou vrstvou, která umožňuje bezbolestnou a netraumatizující výměnu krytí s ochranou nově tvořených epitelií. Hovoříme o tzv. safetac technologii.
Spektrum využití těchto pěnových materiálů je velmi široké, pomohou nám u mírně až silně exsudujících ran, ve fázi granulace a epitelizace, dále i v traumatologii (u exkoriací) či v popáleninové medicíně či v plastické chirurgii, např. ke krytí odběrových ploch. Kryty není vhodné používat v kombinaci s oxidanty (sloučeniny chlóru, H2O2), dochází tím ke zhoršování fyzikálně chemických vlastností pěny [4]. Ideální je aplikace s přesahem 2 cm přes okraj defektu. Frekvence převazů závisí na stavu rány a na množství a charakteru exsudátu. Obvykle převazujeme v rozmezí 3−4 dnů, čisté epitelizující rány až za 7 dnů. Pěnová krytí se rovněž vyrábějí s doplňky – se stříbrem, s obsahem ibuprofenu, s akryláty či s hydroaktivní složkou – a dle konkrétní příměsi mají svá specifická využití.
Algináty
Algináty mají svůj původ v mořských řasách. Vyznačují se velkou absorpční schopností. Při kontaktu s exsudátem se přeměňují ve viskózní gel, který v ráně vytváří optimální vlhkost. Ionty Ca2+ a K+ obsažené v alginátu postupně nahrazují Na+ přítomné v exsudátu. Algináty mohou obsahovat doplňky – např. stříbro ve formě iontů Ag+ nebo nanokrystalický oxid stříbrný. Indikovány jsou jako primární krytí na rány povrchní i hluboké, se střední až silnou sekrecí, včetně ran podminovaných, chobotovitých či infikovaných. Je nutné je aplikovat striktně do defektu, abychom zabránili maceraci okolní zdravé kůže. Převazujeme zpravidla každé 2−3 dny. Při každém převazu musíme z rány vypláchnout zbytky krytí. Vyžadují aplikaci sekundárního krytí (nejčastěji gázy či netkané textilie).
Absorpční krytí s aktivním uhlím
Absorpční krytí s aktivním uhlím tvoří samostatnou a specifickou skupinu. Základem těchto obvazů je jemná nedráždivá pletenina z viskózy či porézního nylonu nasycená aktivním uhlím [2]. Aktivní uhlí může být impregnováno kovovým stříbrem. Krytí má obrovskou absorpční schopnost, pohlcuje bakterie, toxiny, degradační produkty metabolismu a zápach [4]. Redukuje tak bakteriální kolonizaci a potlačuje rannou infekci. Podmínkou pro adekvátní účinek krytí je dostatečná sekrece z rány, při nedostatečné sekreci jej můžeme kombinovat s hydrogelem. Krytí, která jsou uzavřena v nylonovém obalu, se nedoporučuje stříhat. Obvaz je měkký, snadno aplikovatelný. Jeho výměna se řídí intenzitou ranné sekrece a zápachem. Převazujeme zpravidla každé 1−2 dny.
Specifická krytí
Specifická krytí jsou přípravky s medem, s kolagenem, bioaktivní krytí, krytí s obsahem chitosanu, celulózová krytí, prostředky s kyselinou hayluronovou. Skupina je velmi polymorfní a každý z výše uvedených prostředků má jedinečné vlastnosti se specifickou indikací a s praktickým využitím. Materiály jsou často využívány ve druhé léčebné linii či při známých alergiích, např. medové přípravky při intoleranci stříbra pro své antibakteriální a antiseptické účinky.
Inhibitory proteolytických enzymů
Aktivita proteolytických enzymů je u chronických ran zvýšena. Typickým zástupcem je proteináza, která poškozuje extracelulární proteinovou matrix a růstové faktory. Strategie vývoje nových léčebných prostředků se v současné době zaměřuje na lokální aplikace proteinázových inhibitorů [2]. Kromě inaktivace proteináz a ochrany růstových faktorů podporují proliferaci fibroblastů a absorbují destruktivně působící volné radikály. Krytí se po aplikaci v ráně plně vstřebává v průběhu tří dnů.
Růstové faktory
U chronických ran je koncentrace aktivních růstových faktorů snížena, což negativně ovlivňuje hojení ran. Jedná se zejména o destičkový růstový faktor (PDGF), fibroblastový růstový faktor (FGF), epidermální růstový faktor (EGF) a transformující růstový faktor (TGF). Růstové faktory prostupují všemi fázemi hojení, aktivují migraci, proliferaci a diferenciaci buněk zapojených do procesu hojení, regulují syntézu a degradaci extracelulární matrix [2]. Růstové faktory se v léčbě používají samostatně nebo v kombinaci. Nadějné jsou zejména v terapii syndromu diabetické nohy.
Biologická krytí
Biologická krytí jsou využitelná nejen v akutní či popáleninové medicíně, ale i v terapii chronických ran. Řadíme sem klasické dermoepidermální kožní štěpy a kožní transplantáty, ale i tzv. bioinženýrské náhrady. Dermální náhrady jsou přechodné či trvalé. Jeden z nejnovějších bioinženýrských krytů je vyroben z prasečích kožních štěpů, ze kterých je enzymatickou preparací odstraněna epidermis a ostatní imunologicky aktivní buňky dermis [2]. Získáme tak biokompatibilní a imunologicky inertní materiál, jenž akceleruje hojení jako dočasný kryt. Biologická krytí jsou indikována ve fázi granulace, kdy je spodina čistá, bez povlaků, bez známek infekce.
Komplexní přístup
Léčba ulcus cruris venosum musí být vždy komplexní. Další neopominutelnou metodou je kompresivní terapie. Aplikujeme obinadla s krátkým tahem s vysokým pracovním tlakem. Důležitá je správná technika přiložení elastické bandáže. Obinadlo pokrývá nohu od prstů, včetně paty, končí o jednu úroveň výše nad místem klinicky patrného poškození žilního systému (otok, varixy). Jednotlivé otáčky se překrývají o dvě třetiny, nesmějí se tvořit přehyby. Bandáž provádíme v cirkulárních nebo klasových otáčkách, nesmí v žádném případě škrtit, v prohloubených oblastech aplikujeme polstrovací vložky (tzv. inlaye) [4]. Nejvyšší kompresní tlak musí být vyvinut v oblasti kotníků. Doporučení vycházejí z 22 studií, které jsou obsaženy v review databáze Cochrane (Cullum a kol., 2004 [1]). Správné provedení elastické bandáže vyžaduje určitou zručnost a praxi. Bandáže přikládáme před svěšením končetiny a započetím fyzické aktivity, anebo alespoň po 20minutovém klidu s elevovanou dolní končetinou. Postavení kotníku musí být 90 stupňů. Kompresivní bandáž zlepšuje a podporuje činnost svalové pumpy, akceleruje odtok krve k srdci, redukuje edém dolních končetin a má rovněž antiinflamatorní účinek. Někdy je ovšem velmi obtížné pacienty přesvědčit o nezbytnosti komprese, zejména v případech zvýšené ranné sekrece, kdy je nutná častá výměna sekundárního krytí. Důležitou roli zejména u pacientů v domácí péči hrají sestry domácí péče vyškolené v péči o chronickou ránu, které dohlížejí na průběh léčby a dokážou napravit relativně časté chyby při nakládání kompresivních bandáží.
V systémové léčbě venózních ulcerací jsou rutinně indikována a užívána venotonika s cílem zvýšení žilního tonu a zmírnění patologických změn mikrocirkulace [5]. Dochází k redukci edému a ke zmírnění subjektivních symptomů. Mezi běžně dostupná farmaka patří diosmin, rutosidy, deriváty z Ginkgo biloba a další kombinované přípravky.
V průběhu posledního desetiletí se v řadě aspektů změnil i přístup v chirurgické léčbě. Dříve bylo zásadou cévních chirurgů operovat pouze zhojený vřed. Dnes lze intervenovat již ve stadiu otevřeného defektu, který je relativně čistý, a tento progresivní přístup je zásadní pro zhojitelnost defektu. Vždy je potřeba odstranit zdroj povrchového refluxu. Byly vyvinuty méně traumatizující postupy např. pro přerušení perforátorů – endoskopické operační metody, intervence pod ultrazvukovou kontrolou aj. Před každým chirurgickým výkonem by měl být proveden kvalitní duplexní ultrazvuk (ideálně školeným rentgenologem či angiologem), který nám zhodnotí stav nejen hlubokého žilního systému, ale i vena saphena magna či vena saphena parva a její suficienci či insuficienci a rovněž zhodnotí nález na perforátorech. Můžeme tak zabránit řadě zbytečných intervencí, výkony minimalizovat, optimalizovat, pacientovi ušetřit pooperační stres, traumatizaci a bolest a zajistit mu rychlejší rekonvalescenci a včasnější návrat do zaměstnání.
Celková prognóza zhojení vředu závisí na řadě faktorů, na stáří pacienta (horší prognózu mají pacienti starší 70 let), na době trvání a velikosti defektu, na lokalizaci (problematická je laterální lokalizace) a na etiologii, kdy bývají problematické defekty smíšené etiologie, tedy s příměsí arteriální složky. I přes veškerou adekvátní péči a snahu není po roce asi třetina vředů zhojena, anebo hrozí vysoké riziko recidivy (až 30 %) do roka po vyhojení [5].
Závěr
Péče o pacienty s chronickou ránou je komplexní a multioborový problém. Terapeutické možnosti spějí mílovými kroky vpřed. Mezi zdravotníky v České republice působí řada kvalitních pracovníků ve „wound care“ a pacienty se snažíme centralizovat do ambulancí pro hojení chronických ran či do podiatrických poraden. Při setkání s pacientem, který trpí venózní bércovou ulcerací, si klademe následující cíle: zmírnit žilní hypertenzi, zredukovat otok, zhojit vřed za použití moderních prostředků vlhké terapie a ostatních léčebných modalit, ruku v ruce s tím léčit případnou infekci a pečovat o pokožku. Mnohdy je to ovšem běh na dlouhou trať, který vyžaduje compliance všech zúčastněných.
Seznam použité literatury
- [1] Pokorná A, Mrázová R. Kompendium hojení ran pro sestry. Praha: Grada, 2012; s. 8, 110–111.
- [2] Pospíšilová A. Léčba chronických ran moderními krycími prostředky. Praktické lékárenství 2010; 6: 276−281.
- [3] Koutná M, Ulrych O. Manuál hojení ran v intenzivní péči. Praha: Galén, 2015; s. 183.
- [4] Stryja J. Repetitorium hojení ran. Praha: Geum, 2008; s. 116–119, 136, 138, 146, 160, 181.
- [5] Karetová D, Staněk F. Angiologie pro praxi. Praha: Maxdorf, 2007; s. 274−275.