Reslizumab v terapii těžkého eozinofi lního astmatu
Souhrn:
Astma je v současné době poměrně dobře kontrolovatelným onemocněním. Existuje ovšem skupina nemocných, u nichž nelze běžnou léčbou, tzn. inhalačními kortikosteroidy nebo fixní kombinací inhalačních kortikosteroidů a dlouhodobě účinkujících β2 agonistů, kontroly dosáhnout. V této oblasti obtížně léčitelného astmatu se dnes uplatňuje, tak jako v jiných oborech medicíny, biologická léčba. Cílovou strukturou reslizumabu je interleukin 5, který hraje klíčovou roli v rozvoji eozinofilního zánětu. Klinické studie potvrzují účinnost reslizumabu u pacientů s těžkým eozinofilním astmatem, přičemž největší redukce počtu exacerbací je pozorována u pacientů s těžkým refrakterním eozinofilním astmatem. Dalšími pozitivně ovlivnitelnými parametry jsou plicní funkce, kontrola astmatu a kvalita života.
Key words: severe eosinophilic asthma − monoclonal antibodies against interleukin‑5 – reslizumab.
Summary:
Asthma is currently relatively well controlled disease. However, there is a group of patients who can not achieve control with conventional therapy, i.e., inhaled corticosteroids or a fixed combination of inhaled corticosteroids and long‑acting β2 agonists. In this area of difficult‑to‑treat asthma, as in other fields of medicine, biological treatment is now being applied. The target structure of reslizumab is interleukin 5 which plays a key role in the development of eosinophilic inflammation. Clinical studies confirm the efficacy of reslizumab in patients with severe eosinophilic asthma, with the greatest reduction in exacerbations being observed in patients with severe refractory eosinophilic asthma. Other positive parameters are pulmonary function, asthma control and quality of life.
Úvod
Těžké astma se vyskytuje asi u 5–10 % pacientů s astmatem a představuje významný zdravotní a ekonomický problém [1]. V posledních letech došlo k vývoji nových léčiv, která jsou cíleně zaměřena na jednotlivé podskupiny pacientů s ohledem na jejich fenotyp astmatu. Nejvýznamnější pokrok představuje bezesporu biologická léčba, konkrétně v terapii alergického (anti IgE) a eozinofilního (anti IL 5) astmatu. Na tomto poli je již několik léčiv zavedeno do klinické praxe, přičemž vykazují dobrou účinnost u indikovaných pacientů, včetně významného zlepšení kvality života u dříve těžko ovlivnitelných závažných průběhů choroby.
Monoklonální protilátky anti IL 5
Eozinofilní fenotyp astmatu je charakterizován zvýšenými koncentracemi eozinofilů v krvi nebo sputu a je přítomen přibližně u 50 % pacientů s astmatem [2]. Zvýšení koncentrace eozinofilů v krvi představuje rizikový faktor vzniku exacerbace astmatu [3]. Interleukin 5 (IL 5) patří mezi klíčové molekuly eozinofilního astmatu, je důležitý pro vývoj, diferenciaci, aktivaci a přežívání eozinofilů ve tkáních. Inhibice IL 5 tedy redukuje koncentraci eozinofilů v krvi nebo ve sputu, ale má v terapii astmatu i tzv. kortikoidy šetřící účinek.
Pro terapii těžkého eozinofilního astmatu byly dosud schváleny anti IL 5 monoklonální protilátky mepolizumab a reslizumab, registračním procesem prochází benralizumab.
Mepolizumab
Mepolizumab je humanizovaná anti IL 5 monoklonální protilátka, která blokuje vazbu molekuly IL 5 na receptorový komplex IL 5 na buněčném povrchu eozinofilů [4]. Počáteční rozčarování přinesly iniciální studie s mepolizumabem u neselektovaných pacientů s astmatem, kdy nebyl prokázán signifikantní klinický účinek mepolizumabu. V pozdějších studiích zařazujících pouze pacienty s eozinofilním astmatem byl zjištěn významný vliv mepolizumabu na redukci koncentrace eozinofilů v krvi a ve sputu, snížení frekvence exacerbací astmatu a zlepšení kvality
života pacientů [5].
Benralizumab
Benralizumab je humanizovaná monoklonální protilátka, která se váže na podjednotku alfa receptoru pro IL 5 (IL 5Rα) a indukuje destrukci bazofilů a eozinofilů mechanismem buněčné cytotoxicity závislé na protilátkách [2]. V klinických studiích byl prokázán účinek benralizumabu na snížení frekvence exacerbací astmatu a zlepšení jednovteřinové vitální kapacity, tj. objemu vzduchu vydechnutého za první vteřinu usilovného výdechu (forced expiratory volume in one second, FEV1) u pacientů s koncentrací eozinofilů v krvi > 300/µl [6].
Reslizumab
Reslizumab je humanizovaná monoklonální protilátka (IgG4) proti lidskému IL 5 [7]. Specificky se váže na IL 5 a interferuje s jeho vazbou na receptor na povrchu buněk, neutralizuje tedy cirkulující IL 5. Důsledkem je blokáda jeho biologické funkce a následně snížení přežití a aktivity eozinofilů. Reslizumab obsahuje oblast ERRR (glutamát, arginin, arginin, arginin), která koresponduje s epitopem aminokyselin 89−92 na IL 5, tento je zásadní pro interakci s receptorem pro IL 5, a následně tedy klíčový pro jeho biologickou aktivitu [8].
Farmakodynamické účinky reslizumabu
Účinky na eozinofily sputa
Účinek reslizumabu u pacientů s astmatem a se zvýšeným počtem eozinofilů ve sputu (nejméně 3 %) byl hodnocen v 15týdenní randomizované, dvojitě zaslepené, placebem kontrolované klinické studii fáze II s reslizumabem podávaným v dávce 3 mg/kg. Koncentrace eozinofilů ve sputu byly měřeny v podskupině 38 dospělých pacientů na konci léčby. V této studii bylo procento eozinofilů ve sputu sníženo ze střední výchozí hodnoty 17,4 % (standardní odchylka 15,9 %) o 82 % na konci léčby ve skupině léčené reslizumabem.
Účinky na eozinofily v krvi
V klinických studiích fáze I a II s reslizumabem v dávce 3 mg/kg bylo po první dávce pozorováno snížení počtů eozinofilů v krvi, které se udrželo celých 52 týdnů léčby bez známek tachyfylaxe [3,9]. Ve sloučených datech byly ve skupinách léčených placebem a reslizumabem výchozí střední hodnoty počtu eozinofilů 655/µl (n = 476) a 654/µl (n = 477), v 52. týdnu 514/µl (n = 405) a 61/µl (n = 407). Následné sledování pacientů léčených reslizumabem, s vyhodnocením po 90 dnech, prokázalo postupný návrat počtu eozinofilů k výchozím hodnotám (394/µl, n = 36). Pokles počtu eozinofilů v krvi souvisel se sérovou koncentrací reslizumabu.
Pokles počtu eozinofilů v krvi vyvolaný reslizumabem u pacientů s pozitivními protilátkami proti reslizumabu se nelišil od poklesu u pacientů s negativními protilátkami proti reslizumabu.
Klinická účinnost reslizumabu
V počátečních studiích s reslizumabem (podávaným intravenózně) u pacientů s těžkým eozinofilním astmatem (eozinofily ve sputu > 3 %) nedostatečně kontrolovaným vysokými dávkami inhalačních kortikosteroidů a další kontrolující medikací bylo prokázáno zlepšení skóre ACQ (Asthma Control Questionnaire, dotazník kontroly astmatu) a hodnoty FEV1 a naopak snížení počtu eozinofilů ve sputu [3].
V dalších studiích (klinická
hodnocení registrována jako NCT01287039
a NCT01285323,
v textu budou pro zjednodušení uvedena jako
studie I a II, viz tabulku 1) byl hodnocen vliv reslizumabu na četnost exacerbací
astmatu a bezpečnost intravenózně aplikovaného reslizumabu
[9]. Celkem 953 pacientů ve věku 12−75 let
s astmatem nedostatečně kontrolovaným střední až vysokou
dávkou inhalačních kortikosteroidů, s koncentrací
eozinofilů v krvi ≥ 400 /μl a s minimálně
jednou či více exacerbacemi astmatu v posledním roce bylo
randomizováno do dvou multicentrických, paralelních, dvojitě
zaslepených studií fáze III kontrolovaných placebem. V obou
studiích byl prokázán signifikantní pokles četnosti exacerbací
astmatu u pacientů, jimž byl aplikován reslizumab,
ve srovnání s placebem (studie 1: poměr rizik, [RR]
0,50; 95% interval spolehlivosti [CI] 0,37−0,67; studie 2: RR 0,41;
95% CI 0,28−0,59; pro obě studie p < 0,0001).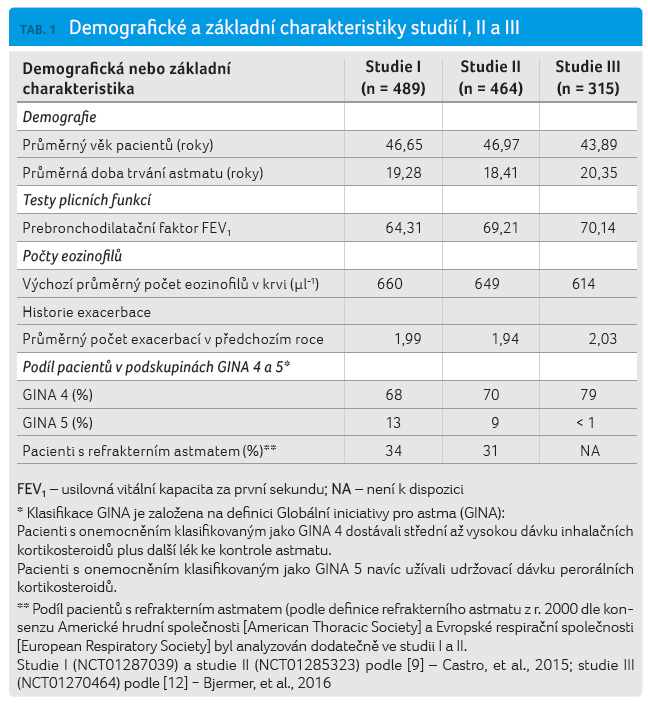
Primárním ukazatelem účinnosti v obou studiích (I a II) byla frekvence exacerbací astmatu u každého pacienta během období 52 týdnů léčby. V obou studiích byla exacerbace astmatu definována jako zhoršení astmatu, které vyžadovalo následující lékařský zákrok:
- užívání perorálních kortikosteroidů nebo zvýšení dávek podávaných inhalačních kortikosteroidů po dobu 3 nebo více dnů a/nebo
- neodkladný léčebný zákrok spojený s astmatem, který zahrnuje alespoň jednu z následujících možností: neplánovaná návštěva ošetřujícího lékaře za účelem zahájení léčby nebulizátorem nebo jiná urgentní léčba s cílem zabránit zhoršení astmatu (návštěva lékařské pohotovosti nebo hospitalizace v souvislosti s astmatem).
Celková populace
Ve studiích I a II
došlo u pacientů užívajících reslizumab v dávce
3 mg/kg k významnému snížení výskytu exacerbací astmatu
(o 50 %, resp. 59 %) ve srovnání s placebem (viz
tab. 2). Celkové
snížení počtu exacerbací dosahovalo 54 %. Podíl pacientů,
u kterých nedošlo k exacerbaci astmatu během 52týdenní
léčby, byl vyšší ve skupině léčené reslizumabem v dávce
3 mg/kg (62 % a 75 %) proti skupině s placebem (46 %
a 55 %) ve studiích I a II.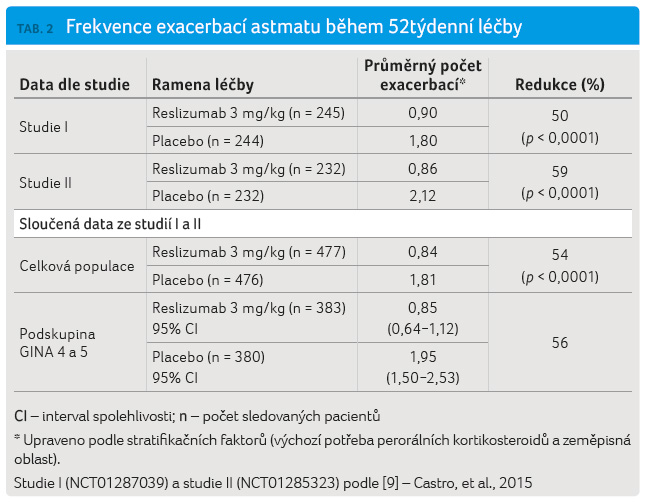
Pacienti s těžkým eozinofilním astmatem
Ve studiích I a II je těžké eozinofilní astma definováno jako jakýkoliv stav pacienta, který odpovídá podskupinám 4 a 5 podle GINA [1]. Pacienti byli léčeni střední až vysokou dávkou inhalačních kortikosteroidů (≥ 440 μg flutikason propionátu) plus dalším přípravkem ke kontrole astmatu, s udržovací léčbou perorálními kortikosteroidy nebo bez ní a s počtem eozinofilů ≥ 400/μl na začátku léčby. Kohorta 763 pacientů ze studií I a II splnila toto kritérium; primární výsledky účinnosti jsou uvedeny v tabulce 2. Ve sloučených datech studií I a II u pacientů léčených reslizumabem v dávce 3 mg/kg došlo k významnému snížení exacerbací astmatu (o 56 % u podskupiny GINA 4 a 5) ve srovnání s placebem.
Účinek léčby reslizumabem v dávce 3 mg/kg podávané jednou za 4 týdny na sekundární cílové parametry, zahrnující FEV1, dotazník AQLQ (Asthma Quality of Life Questionnaire, dotazník kvality života s astmatem), dotazník ACQ a index ASUI (Asthma Symptom Utility Index, index funkčnosti astmatických příznaků), dále svědčí ve prospěch účinnosti reslizumabu (3 mg/kg) ve srovnání s placebem. Zlepšení byla pozorována již za čtyři týdny po první dávce reslizumabu (AQLQ v 16 týdnech) a udržela se až do 52. týdne.
Pacienti se závažným refrakterním eozinofilním astmatem
Reslizumab vedl k významnému snížení exacerbací astmatu oproti placebu u refrakterní populace (59 %) i nerefrakterní populace (49 %). Výsledky byly podpořeny sekundárními cílovými ukazateli účinnosti a odpovídaly celé populaci.
Post hoc analýzou dat výše uvedené studie [9] byl hodnocen účinek reslizumabu na exacerbace astmatu u pacientů s pozdním začátkem astmatu, tzn. ve věku 40 let a později (LO astma = late onset asthma) [10]. Do klinického sledování bylo zahrnuto 273 pacientů s tzv. late onset astmatem a 658 pacientů s tzv. early onset astmatem (časně vzniklým astmatem). Jako signifikantní byl u pacientů prokázán vliv věku začátku astmatu na redukci exacerbací účinkem reslizumabu. Ve srovnání s placebem vedl reslizumab k 75% relativnímu snížení četnosti exacerbací astmatu u pacientů s late onset astmatem, což bylo podstatně více než u pacientů s early onset astmatem. Podobný vliv byl pozorován na hodnoty FEV1.
Další dvě studie se vzájemně podobným uspořádáním, randomizované a kontrolované placebem, kde byl reslizumab podáván intravenózně (i.v.) každé 4 týdny po dobu 16 týdnů, a to pacientům s nedostatečně kontrolovaným astmatem, sledovaly vliv na plicní funkce a kontrolu astmatu. V podskupině pacientů s eozinofilií (s koncentrací eozinofilů v krvi ≥ 400/μl) bylo prokázáno zlepšení plicních funkcí a kontroly astmatu, na rozdíl od skupiny pacientů bez eozinofilie [11]. U pacientů s eozinofilií bylo rovněž prokázáno zlepšení FEV1 při podávání reslizumabu v dávce 3 mg/kg versus placebo (rozdíl v léčbě: 160 ml, p = 0,0018). Zlepšení FEV1 bylo zaznamenáno za 4 týdny po podání první dávky reslizumabu. V této studii (registrována jako NCT01270464, v textu uvedena pro zjednodušení jako studie III, viz tab. 1) byl efekt na zlepšení plicních funkcí a kontroly astmatu prokázán v závislosti na dávce reslizumabu (3 mg/kg versus 0,3 mg/kg) [12].
Naše pracoviště se zúčastnilo klinické studie s reslizumabem v letech 2013−2014. Měli jsme možnost zařadit pět pacientek s těžkým eozinofilním astmatem, které užívaly reslizumab i.v. každé 4 týdny po dobu 52 týdnů. Pozorovali jsme snížení počtu exacerbací a zlepšení kontroly astmatu.
Bezpečnost reslizumabu
Ve studii I a II byly běžné nežádoucí události při podávání reslizumabu podobné jako u placeba. Nejčastějšími byly zhoršení symptomů astmatu (127 [52 %] při podávání placeba a 97 [40 %] v rameni s reslizumabem ve studii I; 119 [51 %] v rameni s placebem a 67 [29 %] v rameni s reslizumabem ve studii II); infekce horních cest dýchacích (32 [13 %] a 39 [16 %]; 16 [7 %] a 8 [3%]) a nazofaryngitidy (33 [14 %] a 28 [11 %]; 56 [24 %] a 45 [19 %]). Dva pacienti měli po podání reslizumabu anafylaktickou reakci, oběma byla podána standardní terapie ve studijních centrech s adekvátní odpovědí. Tito pacienti byli vyřazeni ze studie. Anafylaktická reakce je závažným nežádoucím účinkem, během nezaslepených studií kontrolovaných placebem byla hlášena a považována za související s reslizumabem u 3 pacientů (0,19 %). Tyto reakce byly pozorovány během infuze reslizumabu nebo do 20 minut po jejím ukončení a byly hlášeny již po aplikaci druhé dávky reslizumabu. Byly zcela vyřešeny standardní léčbou bez reziduálních následků. Projevy zahrnovaly postižení kůže nebo sliznic, dušnost, sípání, gastrointestinální příznaky a zimnici. Tyto případy vedly k ukončení léčby. Vzhledem k překrývání příznaků nebylo ve všech případech možné rozlišit mezi anafylaktickou reakcí, jinou hypersenzitivní reakcí a reakcí související s infuzí.
Myalgie byla hlášena u 0,97 % pacientů (10 z 1 028) ve skupině s reslizumabem podávaným v dávce 3 mg/kg ve studiích kontrolovaných placebem ve srovnání s 0,55 % pacientů (4 ze 730) ve skupině s placebem. Zvýšená aktivita kreatinfosfokinázy v krvi byla častějším nálezem, ovšem pouze přechodným a asymptomatickým, což nevedlo k předčasnému ukončení léčby.
Srovnání monoklonálních protilátek v léčbě astmatu
Při léčbě těžkého astmatu, který nedostatečně reaguje na klasickou antiastmatickou léčbu, je při indikaci a výběru biologické léčby nutné respektovat fenotyp astmatu. Reslizumab (i.v. podání) je indikován pro těžké eozinofilní astma, mepolizumab (s.c. podání) pro těžké refrakterní eozinofilní astma a omalizumab (s.c. podání) pro těžké perzistující alergické astma. Od roku 2016 jsou v zemích Evropské unie, a tím i v České republice registrovány pro léčbu těžkého eozinofilního astmatu přípravky Nucala (společnosti GlaxoSmithKline) a Cinqaero (společnosti Teva). Vzhledem k tomu, že dosud nejsou ukončena cenová jednání se zdravotními pojišťovnami, je možno předepisovat tyto přípravky jen v rámci mimořádného dovozu podle všech předpisů s tím souvisejících. Schválení úhrady zdravotními pojišťovnami můžeme očekávat koncem roku 2017 či počátkem roku 2018, jak zaznělo na sympoziu farmaceutické společnosti Teva v rámci XXIV. Luhačovických dnů.
Poslední přehledy a metaanalýzy dosud provedených kontrolovaných dvojitě zaslepených studií s reslizumabem při léčbě těžkého eozinofilního astmatu, který nedostatečně reaguje na odpovídající klasickou antiastmatickou léčbu, dokládají bezpečnost a účinnost této formy léčby [13−16].
Závěr
V souladu s trendem posledních let, kdy dochází k rozvoji fenotypově cílené terapie astmatu, demonstruje další zástupce biologické terapie − anti IL 5 protilátka reslizumab − účinnost především u pacientů s těžkým eozinofilním astmatem. V publikovaných studiích byl prokázán jeho efekt na redukci koncentrace eozinofilů ve sputu a v krvi. Byla potvrzena klinická účinnost reslizumabu na snížení exacerbací astmatu (50−60 %), zlepšení hodnoty FEV1, zlepšení kontroly astmatu a zlepšení kvality života. Výsledky klinických studií podporují užití reslizumabu u pacientů s eozinofilním, refrakterním astmatem nedostatečně kontrolovaným klasickou antiastmatickou léčbou z hlediska současných standardů léčby. Dle nejnovějších poznatků představuje terapie cílící na redukci exacerbací největší přínos pro skupinu pacientů s tzv. late onset těžkým eozinofilním astmatem ve srovnání s tzv. early onset astmatem.
Reslizumab je dobře tolerovaným přípravkem, mezi nejčastější nežádoucí účinky léčby pozorované ve studiích patří zvýšená aktivita kreatinfosfokinázy a myalgie; anafylaktická reakce byla pozorována u tří pacientů (0,19 %).
V srpnu 2016 schválila Evropská komise k distribuci a prodeji léčivý přípravek Cinqaero obsahující jako účinnou látku reslizumab. Vyrábí se jako vodný roztok, který se aplikuje jednou za 4 týdny jako nitrožilní infuze (trvající 20−50 minut) po naředění příslušné dávky. Doporučená dávka je individuální a vychází z tělesné hmotnosti pacienta (3 mg × tělesná hmotnost pacienta v kg). Eliminační poločas reslizumabu je 24 dnů a po přechodném snížení počtu eozinofilů se po čtyřech týdnech začíná jejich počet opět zvyšovat, což určuje i frekvenci podávání. Přípravek je určen pro dlouhodobou léčbu, rozhodnutí o pokračování léčby je třeba učinit nejméně jednou za rok podle závažnosti onemocnění a úrovně kontroly astmatu. Aktuálně probíhající studie jsou zaměřeny na zhodnocení subkutánního podání reslizumabu [13].
Podle Souhrnu údajů o přípravku je reslizumab indikován jako doplňková léčba dospělých pacientů se závažným eozinofilním astmatem nedostatečně kontrolovaným i přes užívání vysokých dávek inhalačních kortikosteroidů, případně dalšího léku na kontrolu astmatu. Od března 2016 je reslizumab dostupný ve Spojených státech amerických a od září 2016 v zemích Evropské unie.
V České republice zatím čekáme na stanovení úhrady ze zdravotního pojištění.
Seznam použité literatury
- [1] Global Strategy for Asthma Management and Prevention (2017 Update). http://ginasthma.org/2017‑gina‑report‑global‑strategy‑for‑asthma‑management‑and‑prevention/ (21. 3. 2017)
- [2] Fajt ML, Wenzel SE. Development of new therapies for severe asthma. Allergy Asthma Immunol Res 2017; 9: 3−14.
- [3] Castro M, Mathur S, Hargreave F, et al. Reslizumab for poorly controlled, eosinophilic asthma: a randomized, placebo‑controlled study. Am J Respir Crit Care Med 2011; 184: 1125−1132.
- [4] Patel TR, Sur S. IgE and eosinophils as therapeutic targets in asthma. Curr Opin Allergy Clin Immunol 2017; 17: 42−49.
- [5] Pavord ID, Korn S, Howarth P, et al. Mepolizumab for severe eosinophilic astma (DREAM): A multicentre, double‑blind, placebo‑controlled trial. Lancet 2012; 380: 651−659.
- [6] Bleecker ER, Fitzgerald JM, Chanez P, et al. Efficacy and safety of benralizumab for patients with severe asthma uncontrolled with high‑dosage inhaled corticosteroids and long‑acting β2‑agonists (SIROCCO): a randomised, multicentre, placebo‑controlled phase 3 trial. Lancet 2016; 388: 2115−2127.
- [7] Egan RW, Athwahl D, Chou CC, et al. Inhibition of pulmonary eosinophilia and hyperreactivity by antibodies to interleukin‑5. Int Arch Allergy Immunol 1995; 107: 321−322.
- [8] Zhang J, Kuvelkar R, Murgolo NJ, et al. Mapping and characterization of the epitope(s) of Sch 55700, a humanized mAb, that inhibic human IL‑5. Int Immunol 1999; 11: 1935−1944.
- [9] Castro M, Zangrilli J, Wechsler MF, et al. Reslizumab for inadequately controlled asthma with elevated blood eosinophils counts: results from two multicentre, parallel, double‑blind, randomised, placebo‑controlled, phase 3 trials. Lancet Respir Med 2015; 3: 355−366.
- [10] Brusselle G, Germinaro M, Weiss S, Zangrilli J. Reslizumab in patients with inadequately controlled late‑onset asthma and elevated blood eosinophils. Pulm Pharmacol Ther 2017; 43: 39−45.
- [11] Corren J, Weinstein S, Janka L, et al. Phase 3 Study of Reslizumab in Patients With Poorly Controlled Asthma: Effects Across a Broad Range of Eosinophil Counts. Chest 2016; 150: 799−810.
- [12] Bjermer L, Lemiere C, Maspero J, et al. Reslizumab for inadequately controlled asthma with elevated blood eosinophil levels: a randomized phase 3 study. Chest 2016; 150: 789−798.
- [13] Máspero J. Reslizumab in the treatment of inadequately controlled asthma in adults and adolescents with elevated blood eosinophils: clinical trial evidence and future prospects. Ther Adv Respir Dis 2017; 6: 1−15.
- [14] Pelaia G, Vatrella A, Buscet MT, et al. Role of biologics in severe eosinophilic asthma – focus on reslizumab. Ther Clin Risk Manag 2016; 12: 1075−1082.
- [15] Li J, Wang F, Lin C, et al. The efficacy and safety of reslizumab for inadeqately controlled asthma with elevated blood eosinophil counts: A systemic review and meta‑analysis. J Asthma 2017; 54: 300−307.
- [16] Deeks ED, Brusselle G. Reslizumab in Eosinophilic Asthma: A Review. Drugs 2017; 77: 777−784.