Sekvenční terapie metastatického renálního karcinomu
V cílené léčbě metastatického renálního karcinomu (mRCC) se v současnosti využívají léky dvou kategorií: inhibitory kaskády vaskulárního endoteliálního faktoru a jeho receptoru (VEGFRi) a inhibitory serin-threoninové kinázy nazvané mammalian target of rapamycin (mTORi). Do první skupiny se řadí sunitinib, sorafenib, pazopanib, axitinib a bevacizumab, do skupiny druhé pak everolimus a temsirolimus. Sekvenční cílená léčba mRCC je v současnosti předmětem mnoha diskusí a optimální pořadí dostupných léků není přesně známo. V praxi je nutné léčbu individualizovat podle průběhu nemoci, komorbidit pacienta a profilu toxicity jednotlivých léků.
Úvod
Renální karcinom (renal cell carcinoma, RCC) patří k nejčastějším urologickým malignitám a je charakteristický svým dlouhým asymptomatickým průběhem. Asi u 40–50 % pacientů dochází v době diagnózy nebo později k metastatickému rozsevu.Etiopatogeneze RCC není přesně známa. Mezi rizikové faktory renálního karcinomu patří kouření, bydlení ve městě a výskyt tohoto typu nádoru v rodině. Nosiči mutace Hippelova-Lindauova (VHL) genu mají 40% pravděpodobnost onemocnění karcinomem ledviny, který bývá často multiplicitní a bilaterální. U sporadických karcinomů ledviny je gen VHL inaktivován asi v 75 % případů. V cílené léčbě metastatického renálního karcinomu (mRCC) se v současnosti využívají léky dvou kategorií: inhibitory kaskády vaskulárního endoteliálního faktoru a jeho receptoru (VEGFRi) a inhibitory serin-threoninové kinázy mammalian target of rapamycin (mTORi).
Hlavním mechanismem působení obou skupin léků je jejich antiangiogenní účinek.Do první skupiny se řadí inhibitory kináz sunitinib, sorafenib, pazopanib, axitinib a monoklonální protilátka bevacizumab, do skupiny druhé everolimus a temsirolimus. Sekvenční cílená léčba mRCC je v současnosti předmětem mnoha diskusí. Optimální sekvence nebyla dosud stanovena a guidelines umožňují jak sekvenci VEGFRi-VEGFRi-mTORi, tak i VEGFRi-mTORi-VEGFRi. Cílem tohoto přehledu je stručný popis podkladů pro sekvenční léčbu mRCC podle zásadmedicíny založené na důkazech (evidence based medicine).
V těchto úvahách o sekvenční léčbě se nezabývám podáním cytokinů, které z většiny současných algoritmů vymizely. V řadě studií není léčba cytokiny ani považována za samostatnou linii a počítají se jen linie cílené léčby.
Současná doporučení České onkologické společnosti pro léčbu metastatického renálního karcinomu (tab. 1) se opírají hlavně o guidelines Evropské společnosti pro klinickou onkologii (ESMO) a v podstatných částech se shodují s dalšími doporučení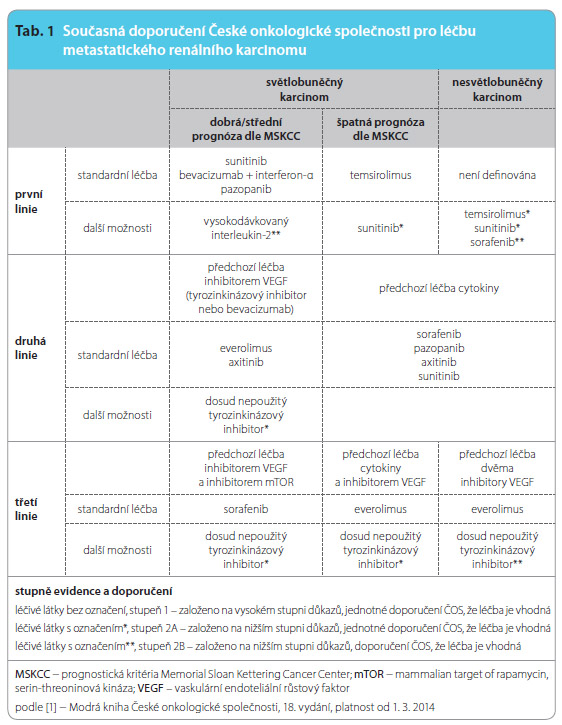 mi velkých světových organizací, například Evropské urologické asociace (EAU) [1–3]. Zvolený léčebný postup závisí na typu renálního karcinomu (světlobuněčný nebo nesvětlobuněčný typ) a prognostické kategorie určené systémem podle Memorial Sloan Kettering Cancer Center (MSKCC), jehož současná modifikovaná podoba je součástí všech výše zmíněných doporučení. U pacientů s dobrou a střední prognózou, což je největší skupina nemocných, se zahajuje léčba antiangiogenním lékem z kategorie VEGFRi.
mi velkých světových organizací, například Evropské urologické asociace (EAU) [1–3]. Zvolený léčebný postup závisí na typu renálního karcinomu (světlobuněčný nebo nesvětlobuněčný typ) a prognostické kategorie určené systémem podle Memorial Sloan Kettering Cancer Center (MSKCC), jehož současná modifikovaná podoba je součástí všech výše zmíněných doporučení. U pacientů s dobrou a střední prognózou, což je největší skupina nemocných, se zahajuje léčba antiangiogenním lékem z kategorie VEGFRi.
V současné době jsou pro léčbu druhé linie registrovány na základě randomizovaných studií třetí fáze dva cílené léky: mTORi everolimus a VEGFRi axitinib.
Sekvenční terapie mRCC je spojena s delším celkovým přežitím (doba od zahájení léčby do úmrtí; OS) pacientů, ale je pravděpodobné, že se na tom podílí vedle účinku léků i příznivá biologie nemoci, která tuto sekvenční léčbu umožní. Při hodnocení výsledků studií s léč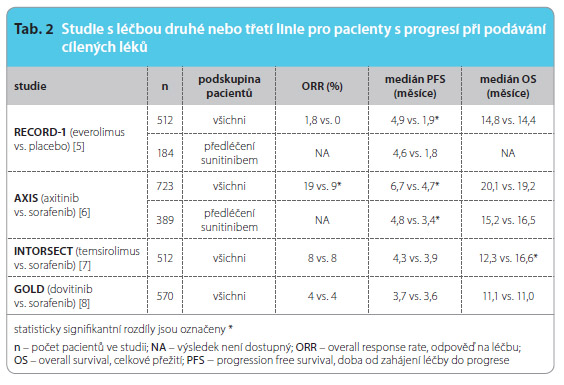 bou druhé, či dokonce třetí linie je tedy nutné myslet na to, že se jedná o vybranou skupinu pacientů s relativně dobrou prognózou. Cena cílené léčby mRCC se v současnosti pohybuje kolem 70 000 Kč až 100 000 Kč měsíčně, jedná se tedy o mimořádně drahou léčebnou intervenci. Navzdory tomu, že se u části nemocných daří dosáhnout dlouhodobé stabilizace nemoci, zůstává mRCC i při rychlém pokroku terapeutických možností většinou nevyléčitelným onemocněním. Jedinou kurativní možností u RCC je časný chirurgický zákrok.V tomto článku poskytuji přehled základních studií týkajících se sekvenční léčby mRCC (tab. 2). Nežádoucí účinky léků byly standardně hodnoceny podle škály pro hodnocení toxicity CTCAE (Common Terminology Criteria for Adverse Events), verze 4.0 [4].
bou druhé, či dokonce třetí linie je tedy nutné myslet na to, že se jedná o vybranou skupinu pacientů s relativně dobrou prognózou. Cena cílené léčby mRCC se v současnosti pohybuje kolem 70 000 Kč až 100 000 Kč měsíčně, jedná se tedy o mimořádně drahou léčebnou intervenci. Navzdory tomu, že se u části nemocných daří dosáhnout dlouhodobé stabilizace nemoci, zůstává mRCC i při rychlém pokroku terapeutických možností většinou nevyléčitelným onemocněním. Jedinou kurativní možností u RCC je časný chirurgický zákrok.V tomto článku poskytuji přehled základních studií týkajících se sekvenční léčby mRCC (tab. 2). Nežádoucí účinky léků byly standardně hodnoceny podle škály pro hodnocení toxicity CTCAE (Common Terminology Criteria for Adverse Events), verze 4.0 [4].
Nejdůležitější randomizované studie druhé a třetí linie léčby
Klinická studie RECORD-1: everolimus versus placebo u nemocných s progresí při léčbě sunitinibem a/nebo sorafenibemEverolimus je perorální mTORi registrovaný na základě randomizované studie RECORD-1. Do ní byli zařazováni pacienti s progresí při léčbě VEGFRi sunitinibem a/nebo sorafenibem. Everolimus prodloužil dobu do progrese onemocnění (doba od zahájení léčby do progrese choroby nebo do úmrtí – progression free survival, PFS) ve srovnání s placebem o tři měsíce [5]. U nemocných s progresí při léčbě jedním VEGFRi byla prokázána delší doba do progrese ve srovnání s nemocnými s progresí při léčbě dvěma přípravky typu VEGFRi (5,4 měsíce vs. 4,0 měsíce). V obou případech byl medián PFS delší u nemocných, jimž byl podáván everolimus, nežli u pacientů dostávajících placebo (hazard ratio, poměr rizik – HR: 0,32; p < 0,001). Prodloužení OS u nemocných randomizovaných k léčbě everolimem nebylo prokázáno, ale ve studii došlo k masivnímu (až 80%) překřížení ramen, což nejspíše výrazně ovlivnilo tento výsledek. Nejčastějšími nežádoucími účinky stupně 3 a 4 byly infekční komplikace (10 %), dušnost (7 %) a únava (5 %). Závažnou komplikací léčby inhibitory mTOR je pneumonitida, těžké formy onemocnění se rozvinou asi u 2 % nemocných léčených everolimem.
Nejdůležitější randomizované
studie druhé a třetí linie léčby
Klinická studie AXIS:
axitinib versus sorafenib u pacientů s progresí při léčbě antagonisty VEGF nebo cytokiny
Axitinib je tyrozinkinázový inhibitor s vysokou selektivitou pro VEGFR. Ve studii fáze III AXIS byl axitinib srovnáván se sorafenibem u nemocných s progresí při jedné předchozí systémové terapii (sunitinib, bevacizumab s interferonem α, temsirolimus, cytokiny [6]). Ve skupině nemocných léčených axitinibem byla PFS 8,3 měsíce ve srovnání s 5,7 měsíce ve skupině se sorafenibem, rozdíl byl statisticky signifikantní. Nejčastějšími nežádoucími účinky stupně 3–4 provázejícími léčbu axitinibem byly hypertenze (16 %), průjem (11 %), únava (11 %), nechutenství (5 %) a hand-foot syndrom (5 %). V podskupině nemocných předléčených sunitinibem, který je v klinické praxi v ČR nejpoužívanějším lékem první linie, byla PFS 4,8 měsíce pro axitinib a 3,4 měsíce pro sorafenib. Medián OS byl ve studii AXIS pro obě ramena prakticky stejný, a to 20,1 měsíce pro axitinib a 19,2 měsíce pro sorafenib. Protože ve studii AXIS nebylo povoleno překřížení ramen, a i tak bylo OS stejné jako u axitinibu, někteří experti považují i sorafenib za validní možnost pro druhou linii léčby.
Klinická studie GOLD:
dovitinib versus sorafenib
u pacientů s progresí při léčbě antagonisty VEGFR a inhibitory mTOR
Studie GOLD byla otevřená multicentrická randomizovaná studie fáze III [7]. Jejím cílem bylo vyzkoušet a zavést do praxe nový multikinázový inhibitor dovitinib. Předpokládá se, že při primární nebo sekundární rezistenci na VEGFRi se výrazně uplatňuje dráha fibroblastového růstového faktoru (FGF). Dovitinib inhibuje kromě VEGFR právě i receptor pro FGF. Výsledky studie GOLD však přinesly pro výrobce dovitinibu zklamání. Medián PFS pro dovitinib byl 3,7 měsíce, pro sorafenib 3,6 měsíce (HR: 0,86; p = 0,063). Medián OS byl pro oba léky stejný – 11,1 měsíce vs. 11,0 měsíce (HR: 0,96; p = 0,357). Dovitinib měl vyšší gastrointestinální toxicitu (průjem: 68 % vs. 45 %, nevolnosti: 53 % vs. 29 %, zvracení: 44 % vs. 16 %, naopak u sorafenibu byla zjištěna vyšší kožní toxicita (palmoplantární erytrodysestezie: 40 % vs. 11 %), hypertenze (28 % vs. 19 %) a alopecie (21 % vs. 1 %). Tyto výsledky (dlouhé celkové přežití i po ukončení systémové terapie) nepřímo podporují výše uvedenou hypotézu, že pacienti schopní dostat cílenou léčbu třetí linie mají inherentně příznivý (relativně indolentní) průběh onemocnění.
Klinická studie INTORSECT:
sorafenib versus temsirolimus u pacientů s progresí při léčbě sunitinibem
V randomizované studii fáze III nazvané INTORSECT se srovnával VEGFRi sorafenib s intravenózně podávaným mTORi temsirolimem u nemocných s progresí při léčbě sunitinibem. Ani jeden z uvedených léků nepředstavoval v době zahájení studie standardní možnost druhé linie léčby mRCC. Mezi oběma rameny nebyl zjištěn statisticky významný rozdíl v PFS (4,3 měsíce ve srovnání s 3,9 měsíce). Medián OS byl nicméně signifikantně delší pro sorafenib (16,4 měsíce vs. 12,3 měsíce) [8]. Podávání sorafenibu v sekvenční terapii zahájené po léčbě jinými cílenými léky je u nás v současnosti blokováno zněním registračního omezení a platnými úhradovými podmínkami. Výsledky studie INTORSECT nepřímo naznačují, že sekvence VEGFRi-VEGFRi je výhodnější než VEGFRi-mTORi, alespoň u nemocných, jejichž onemocnění progredovalo při léčbě sunitinibem.
Sekvenční klinické studie
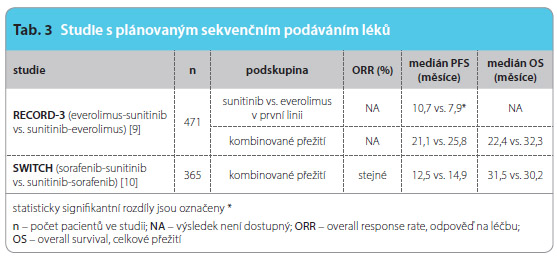
Sekvenční klinické studie jsou ty, u nichž se již předem počítá s určitou sekvencí podané léčby (tab. 3). Celkové hodnocení může zahrnovat PFS spojenou s jednotlivými léky, ale nejdůležitějšími výsledky jsou kombinované PFS (tj. součet PFS při postupně podávaných lécích) a zejména OS. Na základě těchto parametrů se pak hodnotí účinek celé sekvence léků.
Klinická studie RECORD-3:
sekvenční terapie sunitinibem a everolimem
RECORD-3 byla multicentrická randomizovaná studie fáze II, která srovnávala sekvenční léčbu everolimem po progresi při užívání sunitinibu s obráceným pořadím uvedených léků. V této studii byla potvrzena neinferiorita sekvence everolimus-sunitinib pro PFS. Studie RECORD-3 byla první publikovanou randomizovanou studií, která srovnávala účinnost a bezpečnost dvou sekvencí cílené terapie [9]. Do této studie bylo zařazeno celkem 471 pacientů s mRCC, z nichž většina (85 %) měla nádor typu konvenčního (světlobuněčného) renálního karcinomu. Po progresi při podávání prvního léku byla zahájena léčba druhým přípravkem, která pokračovala do druhé progrese.
Výsledky studie prokazují, že je výhodnější zahájit léčbu sunitinibem (PFS 10,7 měsíce vs. 7,9 měsíce, HR: 1,43; 95% interval spolehlivosti, confidence interval – CI: 1,15–1,77). Pro hodnocení kombinovaného přežití, což je pro sekvenční studie zásadní parametr, neměla zatím data dostatečnou výpovědní hodnotu a bude nutná delší doba sledování. I zde se ukazuje výhoda sekvence sunitinib-everolimus; OS dosáhlo 32,3 měsíce v rameni sunitinib-everolimus a 22,4 měsíce v rameni everolimus-sunitinib. Nicméně jen přibližně 50 % pacientů v obou ramenech bylo schopno pokračovat v terapii druhé linie podle plánu klinické studie a to ztěžuje statistické hodnocení výsledků.Ve studii fáze II nazvané ESPN (Everolimus versus sunitinib prospective evaluation in metastatic non-clear cell renal cell carcinoma – prospektivní hodnocení everolimu proti sunitinibu u metastatického světlobuněčného renálního karcinomu) a prezentované na konferenci ASCO 2014 se rovněž prokázalo, že by se inhibitor mTOR everolimus neměl v první linii používat, a to ani u pacientů s nesvětlobuněčnými renálními karcinomy [10].
Klinická studie SWITCH:
sekvenční léčba sunitinibem a sorafenibem
Studie SWITCH byla randomizovaná sekvenční studie fáze III, která probíhala v evropských centrech [11]. Nemocní s mRCC byli randomizováni k sekvenci sunitinib-sorafenib nebo k sekvenci opačné. Vstup do studie byl podmíněn dobrou nebo střední prognózou podle MSKCC (prognostická kritéria Memorial Sloan Kettering Cancer Center), přítomností alespoň jedné měřitelné léze a kontraindikací cytokinové léčby, která představovala podmínku poněkud kontroverzní a nejasnou. Zařazeno bylo celkem 365 pacientů. Neprokázaly se signifikantní rozdíly v kombinované hodnotě PFS (HR:1,01), OS (HR: 1,0) ani v PFS v první linii léčby (HR: 1,19). Obě sekvence léčby jsou tudíž ekvivalentní. Studie byla navržena před registrací současných standardních léků druhé linie, jimiž jsou everolimus a axitinib. Není tudíž jisté, zda její závěry platí také pro sekvenci sunitinib-axitinib a pro sekvenci axitinib-sunitinib. Pro sekvenci sunitinib-everolimus nicméně odpověď známe, a to díky studii RECORD-3 (viz výše) [9].
Retrospektivní a observační studie
Retrospektivní/observační studie poskytují důkazy nižší kvality než studie randomizované, protože jsou zatíženy vyšším rizikem statistického zkreslení výsledků. Nicméně se jedná o cenné analýzy – poskytují údaje o účinnosti jednotlivých léčebných strategií v běžné klinické praxi a zabývají se i otázkami, jež lze v klinických studiích zodpovědět jen velmi obtížně. Výsledky retrospektivních studií zabývajících se sekvenční léčbou mRCC nejsou zcela konkordantní. V italském souboru, který publikoval Iacovelli a kol., bylo OS delší u pacientů léčených sekvencí VEGFRi-VEGFRi-mTORi [12]. Signifikantní rozdíly nicméně nebyly pozorovány v řadě dalších studií: německé [13], americko-kanadské [14] a v nedávno publikovaných českých analýzách pacientů z registru RENIS [15]. V analýzách registru RENIS jsme mimo jiné ukázali, že na základě PFS v první linii léčby nelze předvídat PFS pro druhou linii terapie při použití sekvence sunitinib-sorafenib nebo opačně [16]. PFS při léčbě everolimem pozitivně koreluje s PFS při použití VEGFRi jen u nemocných léčených everolimem ve druhé linii, pro třetí linii léčby to už neplatí [15]. Nicméně retrospektivní údaje ukazují, že léčba everolimem může být odložena až do třetí linie bez ztráty účinnosti nebo zvýšení toxicity [15].
Nevyřešené otázky a další směr výzkumu
Terapie nesvětlobuněčných renálních karcinomů je stále předmětem výzkumu, stanovit jednoznačná doporučení je proto obtížné. Dosud se však nikdy jasně neprokázalo, že by v této heterogenní skupině nemocných neměla platit doporučení (guidelines) léčby pro pacienty se světlobuněčným renálním karcinomem.
U pacientů se špatnou prognózou dle MSKCC je terapií volby v první linii temsirolimus, sekvence dalších cílených léků po progresi při léčbě temsirolimem není jasná. Průběh onemocnění v této skupině pacientů je zpravidla nepříznivý a případné odpovědi na léčbu krátkodobé, tudíž zde není velký prostor pro sekvenční léčbu.
V klinických studiích pro druhou a vyšší linii léčby je zkoušeno několik nových léků, nejdále zatím pokročil inhibitor receptoru PD-1 (programmed death-1) nivolumab, u něhož probíhá klinická studie s randomizací proti everolimu v léčbě druhé a třetí linie.
Závěr
Na základě klinických studií nelze zatím jednoznačně doporučit optimální sekvenci tří cílených léků, sekvence VEGFRi-mTORi-VEGFRi i VEGFRi-VEGFRi-mTORi zůstávají validními možnostmi terapie. Dosud chybějí validované molekulární markery, které by pomohly s individualizací terapie cílenými léky pro mRCC. V klinické praxi se rozhodujeme podle stavu nemocného, komorbidit a očekávané toxicity jednotlivých léků a také podle platných registračních a úhradových omezení.
Seznam použité literatury
- [1] Modrá kniha České onkologické společnosti. 18. vydání (platnost od 1. 3. 2014), Masarykův onkologický ústav, Brno. http://www.linkos.cz/informace-pro-praxi/modra-kniha/ (navštíveno 12. 8. 2014)
- [2] Escudier B, Eisen T, Porta C, et al. Renal cell carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2012; 23 (Suppl 7): vii65–71.
- [3] Ljungberg B, Bensalah K, Bex A, et al. Guidelines on renal cell carcinoma. European Association of Urology 2014. http://www.uroweb.org/gls/pdf/10%20Renal%20Cell%20Carcinoma_LR.pdf (navštíveno 12. 8. 2014)
- [4] Common Terminology Criteria for Adverse Events (CTCAE) version 4.0. http://evs.nci.nih.gov/ftp1/CTCAE/CTCAE_4.03_2010-06-14_QuickReference_5x7.pdf (navštíveno 12. 8. 2014).
- [5] Motzer RJ, Escudier B, Oudard S, et al. Efficacy of everolimus in advanced renal cell carcinoma: a double-blind, randomised, placebo-controlled phase III trial. Lancet 2008; 372: 449–456.
- [6] Rini BI, Escudier B, Tomczak P, et al. Comparative effectiveness of axitinib versus sorafenib in advanced renal cell carcinoma (AXIS): a randomised phase 3 trial. Lancet 2011; 378: 1931–1939.
- [7] Motzer RJ, Porta C, Vogelzang NJ, et al. Dovitinib versus sorafenib for third-line targeted treatment of patients with metastatic renal cell carcinoma: an open-label, randomised phase 3 trial. Lancet Oncol 2014; 15: 286–296.
- [8] Hutson TE, Escudier B, Esteban E, et al. Randomized phase III trial of temsirolimus versus sorafenib as second-line therapy after sunitinib in patients with metastatic renal cell carcinoma. J Clin Oncol 2014; 32: 760–767.
- [9] Motzer RJ, Barrios CH, Kim TM, et al. Record-3: Phase II randomized trial comparing sequential first-line everolimus (EVE) and second-line sunitinib (SUN) versus first-line SUN and second-line EVE in patients with metastatic renal cell carcinoma (mRCC). J Clin Oncol 2013; 31 (suppl): abstr 4504.
- [10] Tannir NM, Jonasch E, Altinmakas E, et al, Everolimus versus sunitinib prospective evaluation in metastatic non-clear cell renal cell carcinoma (The ESPN Trial): A multicenter randomized phase 2 trial. J Clin Oncol 2014; 32: 5s, 32 (suppl; abstr 4505).
- [11] Goebell PJ, Vervenne W, De Santis M, et al. Subgroup analyses of a randomized sequential open-label study (SWITCH) to evaluate efficacy and safety of sorafenib (SO)/sunitinib (SU) versus SU/SO in the treatment of metastatic renal cell cancer (mRCC). J Clin Oncol 2014; 32: 5s (suppl; abstr 4567).
- [12] Iacovelli R, Cartenì G, Sternberg CN, et al. Clinical outcomes in patients receiving three lines of targeted therapy for metastatic renal cell carcinoma: results from a large patient cohort. Eur J Cancer 2013; 49: 2134–2142.
- [13] Busch J, Seidel C, Erber B, et al. Retrospective comparison of triple-sequence therapies in metastatic renal cell carcinoma. Eur Urol 2013; 64: 62–70.
- [14] Heng DYC, Rini BI, Lee JL, et al. First-, second-, third-line therapy for metastatic renal cell carcinoma (mRCC): Benchmarks for trials design from the International mRCC Database Consortium (IMDC). J Clin Oncol 2013; 31 (suppl): abstr 4586.
- [15] Buchler T, Bortlicek Z, Poprach A, et al. Efficacy of everolimus in second- and third-line therapy for metastatic renal cell carcinoma: A registry-based analysis. Urol Oncol 2014; 32: 569–575.
- [16] Buchler T, Pavlik T, Bortlicek Z, et al. Objective response and time to progression on sequential treatment with sunitinib and sorafenib in metastatic renal cell carcinoma. Med Oncol 2012; 29: 3321–3324.