Sledování mutace KRAS při léčbě cetuximabem u spinocelulárních karcinomů hlavy a krku
Tato práce se zabývá klinickým významem mutace KRAS u spinocelulárních karcinomů hlavy a krku. Mutace KRAS zde byla sledována v multicentrické studii v rámci hledání prediktivních markerů při léčbě cetuximabem a radioterapií. Výsledky léčby byly u našich pacientů velmi dobré (80 % kompletních remisí u lokoregionálně pokročilých karcinomů), avšak očekávaný negativně prediktivní vliv sledované mutace prokázán nebyl.
Úvod
V posledních letech jsme v onkologii svědky rozšiřujících se možností cílené léčby, která je zaměřena na blokádu specifického proteinu v signální soustavě nádorových buněk. Současně s novými metodami léčby přichází i potřeba nalezení vhodných prediktivních markerů, které by nám pomohly najít nejvhodnější pacienty pro tuto léčbu. Přestože je celosvětově předmětem výzkumu velké množství prediktivních markerů, přínos pro praxi má ve výsledku jen malá část z nich.
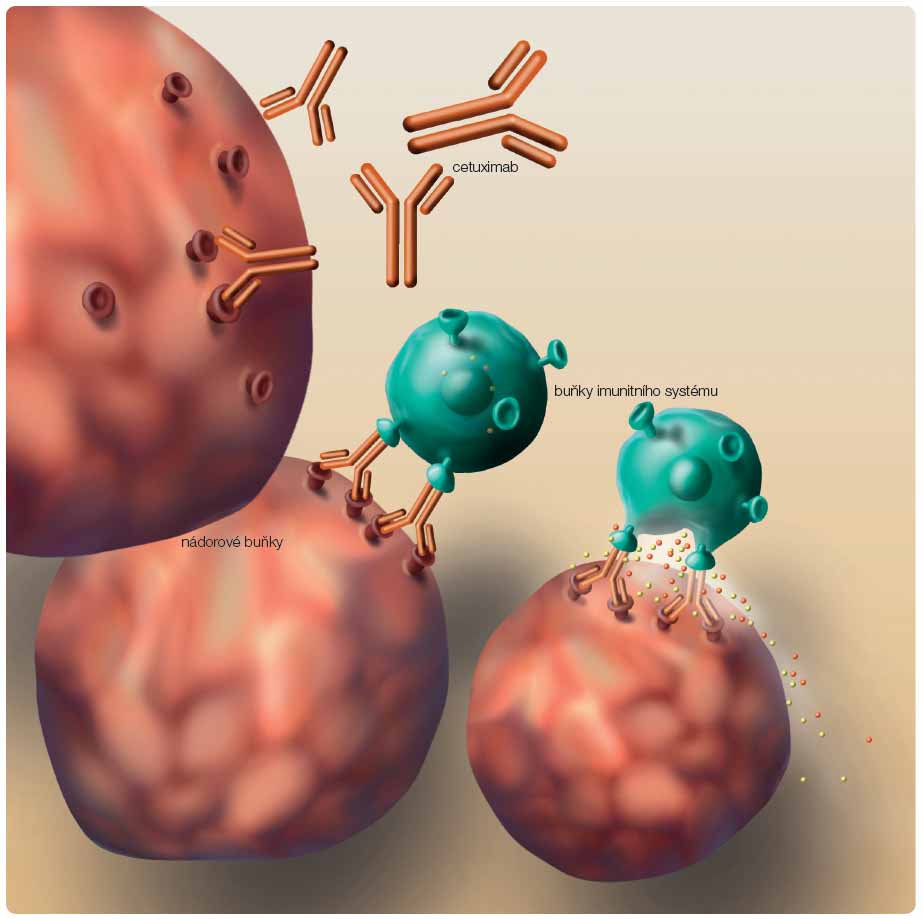 Pro indikace spinocelulárních karcinomů hlavy a krku byl v rámci cílené léčby zaregistrován zatím pouze jediný přípravek – cetuximab, který patří do skupiny extracelulárních inhibitorů receptoru pro epidermální růstový faktor (EGFR). Tento receptor hraje v kancerogenezi klíčovou roli, jeho signální cesta způsobuje u nádorů aktivaci buněčného dělení, inhibici apoptózy, angiogenezi, metastazování, ale i rezistenci na radioterapii, chemoterapii a hormonální léčbu [1]. Zvýšená exprese EGFR je nalézána u mnoha nádorů a může korelovat jak s horší prognózou, tak s horším přežitím [2]. Ze všech epiteliálních nádorů je nejvyšší exprese EGFR nalézána právě u spinocelulárních karcinomů hlavy a krku (HNSCC). EGFR kromě klíčového významu v kancerogenezi hraje svoji roli i u normálních tkání, jako jsou střeva, kůže nebo ledviny, a z toho vyplývají i nežádoucí účinky antiEGFR léčby, jako je průjem, kožní vyrážka nebo hypomagnezemie (blokáda EGFR interferuje s transportním mechanismem magnesia, čímž zabraňuje zpětnému vychytávání magnesia v Henleově kličce ledvin) [3, 4]. Extracelulární inhibitory (monoklonální protilátky) u HNSCC vykazují lepší účinnost než inhibitory intracelulární, což lze přisoudit jinému mechanismu účinku. Monoklonální protilátky vedle zablokování signální cesty receptoru aktivují na protilátkách závislou buněčnou cytotoxicitu (ADCC, antibody-dependent cellular cytotoxicity) [5]. Tato aktivace imunitního systému proti nádoru je spuštěna navázáním protilátky na nádorovou buňku, avšak je specifická pouze pro protilátky třídy IgG1, jejichž zástupcem je např. cetuximab (obr. 1). Aktivace ADCC není přítomna u IgG2, kam patří panitumumab.
Pro indikace spinocelulárních karcinomů hlavy a krku byl v rámci cílené léčby zaregistrován zatím pouze jediný přípravek – cetuximab, který patří do skupiny extracelulárních inhibitorů receptoru pro epidermální růstový faktor (EGFR). Tento receptor hraje v kancerogenezi klíčovou roli, jeho signální cesta způsobuje u nádorů aktivaci buněčného dělení, inhibici apoptózy, angiogenezi, metastazování, ale i rezistenci na radioterapii, chemoterapii a hormonální léčbu [1]. Zvýšená exprese EGFR je nalézána u mnoha nádorů a může korelovat jak s horší prognózou, tak s horším přežitím [2]. Ze všech epiteliálních nádorů je nejvyšší exprese EGFR nalézána právě u spinocelulárních karcinomů hlavy a krku (HNSCC). EGFR kromě klíčového významu v kancerogenezi hraje svoji roli i u normálních tkání, jako jsou střeva, kůže nebo ledviny, a z toho vyplývají i nežádoucí účinky antiEGFR léčby, jako je průjem, kožní vyrážka nebo hypomagnezemie (blokáda EGFR interferuje s transportním mechanismem magnesia, čímž zabraňuje zpětnému vychytávání magnesia v Henleově kličce ledvin) [3, 4]. Extracelulární inhibitory (monoklonální protilátky) u HNSCC vykazují lepší účinnost než inhibitory intracelulární, což lze přisoudit jinému mechanismu účinku. Monoklonální protilátky vedle zablokování signální cesty receptoru aktivují na protilátkách závislou buněčnou cytotoxicitu (ADCC, antibody-dependent cellular cytotoxicity) [5]. Tato aktivace imunitního systému proti nádoru je spuštěna navázáním protilátky na nádorovou buňku, avšak je specifická pouze pro protilátky třídy IgG1, jejichž zástupcem je např. cetuximab (obr. 1). Aktivace ADCC není přítomna u IgG2, kam patří panitumumab.
Mezi další mechanismy aktivace imunitního systému proti nádoru patří aktivace komplementu a na komplementu závislá cytotoxicita (complement-dependent cytotoxicity). Dalším faktem je, že tyrozinkinázové inhibitory EGFR mohou být považovány za méně specifické než monoklonální protilátky, neboť mohou v buňce inhibovat i jiné tyrozinkinázové cesty ovlivňující i normální buněčné funkce. V grantové studii, která probíhala na klinice otorinolaryngologie a chirurgie hlav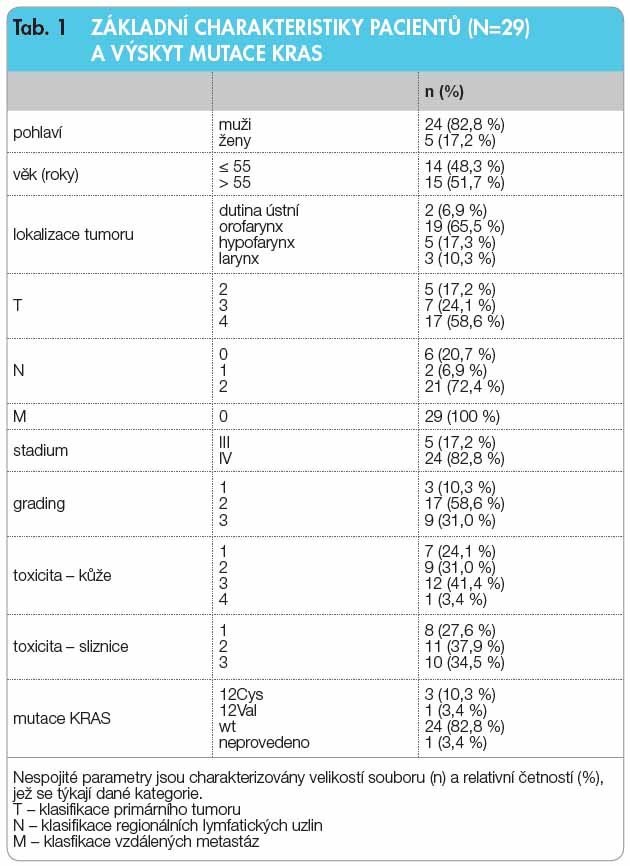 y a krku v Brně a Praze, jsme se zaměřili na sledování různých genetických alterací signální cesty EGFR. Mezi nejvíce sledované patří mutace KRAS genu, která prokázala negativně prediktivní vliv při léčbě extracelulárními inhibitory EGFR u kolorektálních karcinomů, kde je již zavedena do praxe jako prediktivní marker [6, 7]. KRAS protein (produkt KRAS genu) je jedním z přenašečů v signální cestě EGFR a při mutaci KRAS genu dochází ke kontinuální aktivaci signální cesty nezávisle na aktivaci nebo inhibici receptoru. Nemutovaný protein má schopnost inaktivace ze stavu GTP do GDP pomocí GTPázy. Aktivující bodové mutace v exonu 1 KRAS genu (v kodonech 12 a 13) snižují hydrolytickou aktivitu GTPázy, což má za následek kontinuální aktivaci KRAS proteinu. Mutace KRAS byla nalezena u mnoha typů nádorů, např. u nádorů plic, kolorekta, pankreatu či HNSCC. Na meetingu AHNS (American Head and Neck Society)
y a krku v Brně a Praze, jsme se zaměřili na sledování různých genetických alterací signální cesty EGFR. Mezi nejvíce sledované patří mutace KRAS genu, která prokázala negativně prediktivní vliv při léčbě extracelulárními inhibitory EGFR u kolorektálních karcinomů, kde je již zavedena do praxe jako prediktivní marker [6, 7]. KRAS protein (produkt KRAS genu) je jedním z přenašečů v signální cestě EGFR a při mutaci KRAS genu dochází ke kontinuální aktivaci signální cesty nezávisle na aktivaci nebo inhibici receptoru. Nemutovaný protein má schopnost inaktivace ze stavu GTP do GDP pomocí GTPázy. Aktivující bodové mutace v exonu 1 KRAS genu (v kodonech 12 a 13) snižují hydrolytickou aktivitu GTPázy, což má za následek kontinuální aktivaci KRAS proteinu. Mutace KRAS byla nalezena u mnoha typů nádorů, např. u nádorů plic, kolorekta, pankreatu či HNSCC. Na meetingu AHNS (American Head and Neck Society) 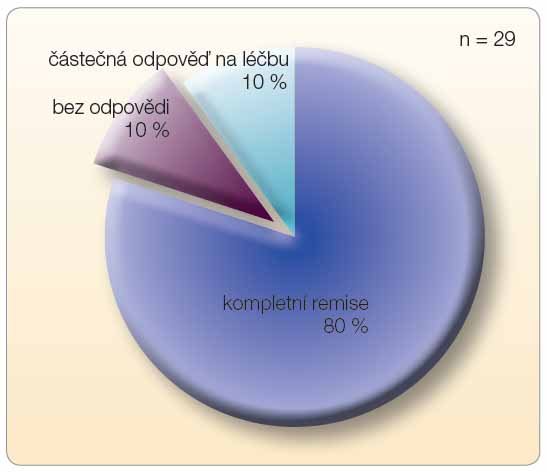 v roce 2008 byla prezentována studie sledující mutaci KRAS ve vztahu k lokoregionální kontrole, k přežití bez známek onemocnění a ve vztahu k přežití bez vzdálených metastáz u pacientů s místně pokročilými karcinomy hlavy a krku, kteří byli léčeni chemoradioterapií a chirurgicky nebo bez chirurgického zákroku. Analýza DNA se podařila u 197 pacientů, z nichž 3,5 % mělo přítomnu mutaci KRAS v kodonu 12. Závěr této studie zněl, že mutace KRAS je u karcinomů hlavy a krku spojena se selháním léčby, celkovou agresivitou onemocnění, a mohla by proto ovlivnit druh volené terapie.Naše prospektivní studie zahrnovala pacienty s lokoregionálně pokročilými karcinomy hlavy a krku klinického stadia III/IV v dobrém celkovém stavu a ve věku nižším než 65 let. Vzorky tumoru byly odebírány především z periferních částí tumoru a zmraženy v RNAlateru. Konkomitantní léčbu cetuximabem a radioterapií (70Gy) podstoupilo celkem 29 pacientů, z toho 24 mužů a 5 žen. Dle lokalizace se jednalo o tumory orofaryngu (65,5 %), hypofaryngu (17,3 %), laryngu (10,3 %) a dutiny ústní (6,9 %), viz tab. 1.
v roce 2008 byla prezentována studie sledující mutaci KRAS ve vztahu k lokoregionální kontrole, k přežití bez známek onemocnění a ve vztahu k přežití bez vzdálených metastáz u pacientů s místně pokročilými karcinomy hlavy a krku, kteří byli léčeni chemoradioterapií a chirurgicky nebo bez chirurgického zákroku. Analýza DNA se podařila u 197 pacientů, z nichž 3,5 % mělo přítomnu mutaci KRAS v kodonu 12. Závěr této studie zněl, že mutace KRAS je u karcinomů hlavy a krku spojena se selháním léčby, celkovou agresivitou onemocnění, a mohla by proto ovlivnit druh volené terapie.Naše prospektivní studie zahrnovala pacienty s lokoregionálně pokročilými karcinomy hlavy a krku klinického stadia III/IV v dobrém celkovém stavu a ve věku nižším než 65 let. Vzorky tumoru byly odebírány především z periferních částí tumoru a zmraženy v RNAlateru. Konkomitantní léčbu cetuximabem a radioterapií (70Gy) podstoupilo celkem 29 pacientů, z toho 24 mužů a 5 žen. Dle lokalizace se jednalo o tumory orofaryngu (65,5 %), hypofaryngu (17,3 %), laryngu (10,3 %) a dutiny ústní (6,9 %), viz tab. 1. 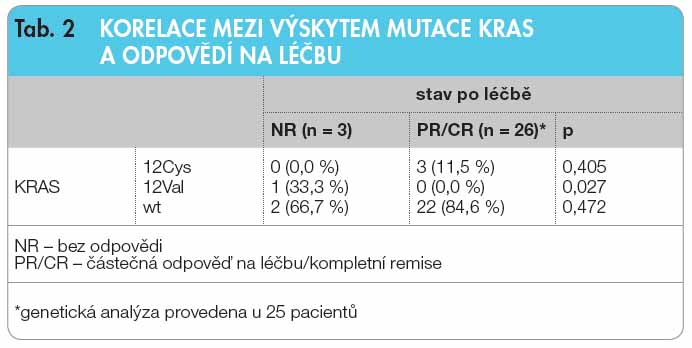 Kompletní remise bylo dosaženo u 80 % pacientů, 10 % dosáhlo parciální remise a pouze 10 % pacientů zůstalo bez odpovědi na léčbu (graf 1). Většina pacientů (82,8 %) měla KRAS nemutovaný gen. Mutace p.Gly12Cys byla nalezena u 3 pacientů (10,3 %) a mutace p.Gly12Val u jednoho pacienta (3,4 %). Pouze přítomnost mutace p.Gly12Val v KRAS genu byla sdružena s absencí odpovědi na léčbu (p = 0,027), viz tab. 2.
Kompletní remise bylo dosaženo u 80 % pacientů, 10 % dosáhlo parciální remise a pouze 10 % pacientů zůstalo bez odpovědi na léčbu (graf 1). Většina pacientů (82,8 %) měla KRAS nemutovaný gen. Mutace p.Gly12Cys byla nalezena u 3 pacientů (10,3 %) a mutace p.Gly12Val u jednoho pacienta (3,4 %). Pouze přítomnost mutace p.Gly12Val v KRAS genu byla sdružena s absencí odpovědi na léčbu (p = 0,027), viz tab. 2.
Diskuse a závěr
Léčba cetuximabem a radioterapií je na našem pracovišti zhodnocena zatím pouze u omezeného počtu pacientů, avšak v souladu se zahraničními zkušenostmi se tato kombinace jeví jako dobře účinná a méně toxická alternativa chemoradioterapie [8]. Mutace KRAS je u určitých tumorů používána jako negativní prediktivní faktor [6, 7], avšak její výskyt u pacientů s karcinomy hlavy a krku je velmi nízký [9, 10]. V naší studii byly nalezeny 3 případy mutace 12Cys, všechny však s kompletní remisí po léčbě. Mutace 12Val byla nalezena pouze u jednoho pacienta a korelovala s rezistencí na léčbu, avšak nebylo možno statisticky významně zhodnotit její prediktivní význam. Ověření klinického významu mutace 12Val by vyžadovalo větší soubor pacientů. Přestože byla tato naše studie provedena na malém souboru pacientů, naše výsledky ukazují, že obecně detekce mutace KRAS u HNSCC neodhalí rezistenci na léčbu cetuximabem, a proto se v této oblasti bude potřeba zaměřit na jiné markery.
Tato studie byla podpořena grantem IGA MZCR No. NS 10108-4.
Seznam použité literatury
- [1] Kalyankrishna S, Grandis JR. Epidermal growth factor receptor biology in head and neck cancer. J Clin Oncol 2006; 24: 2666–2672.
- [2] Egloff AM, Grandis J. Targeting EGFR and Src Pathways in Head and Neck Cancer. Semin Oncol 2008; 35: 286–297.
- [3] Schrag D, Chung KY, Flombaum C, et al. Cetuximab therapy and symptomatic hypomagnesemia. J Natl Cancer Inst 2005; 97: 1221–1224.
- [4] Tejpar S, Piessevaux H, Claes K, et al. Magnesium wasting associated with epidermal-growth-factor receptor-targeting antibodies in colorectal cancer: a prospective study. Lancet Oncol 2007; 8: 387–394.
- [5] Kawaguchi Y, Kono K, Mimura K, et al. Cetuximab induce antibody- dependent cellular cytotoxicity against EGFR-expressing esophageal squamous cell carcinoma. Int J Cancer 2007; 120: 781–787.
- [6] Liévre A, Bachet JB, Le Corre D, et al. K-RAS mutation status is predictive of response to cetuximab therapy in colorectal cancer. Cancer Research 2006; 66: 3992–3995.
- [7] Di Fiore F, Blanchard F, Charbonnier F, et al. Clinical relevance of KRAS mutation detection in metastatic colorectal cancer treated by Cetuximab plus chemotherapy. Br J Cancer 2007; 96: 1166–1169.
- [8] Bonner JAS, Harari PM, Giralt J, et al. Radiotherapy plus cetuximab for squamous-cell carcinoma of the head and neck. N Engl J Med 2006; 354: 567–678.
- [9] Van Damme N, Deron P, Van Roy N, et al. Epidermal Growth Factor Receptor and K-RAS status in two cohorts of squamous cell carcinomas. BMC Cancer 2010; 10: 189–198.
- [10] Bissada E, Abou-Chacra Z, Weng X, et al. Prevalence of K-RAS codon 12 mutations in locally advanced head and neck squamous cell carcinoma and influence with regards to response to chemoradiation therapy. J Clin Oncol, Meeting Proceedings (Post-Meeting Edition). ASCO Annual M, 2008, Vol. 26.