Studie ENSURE‑AF
Souhrn:
U pacientů s fibrilací síní se stále častěji užívají nová antikoagulancia spíše než antagonisté vitaminu K – warfarin v prevenci tromboembolických příhod. Ve velkých randomizovaných studiích byl srovnáván účinek nových antikoagulancií s warfarinem u nevalvulární fibrilace síní, kdy nová antikoagulancia byla účinnější a bezpečnější než warfarin. Existuje pouze jedna prospektivní studie s rivaroxabanem u pacientů podstupujících kardioverzi z důvodu fibrilace síní (X‑VeRT). ENSURE‑AF je největší prospektivní randomizovanou studií, která srovnává edoxaban, přímý inhibitor koagulačního faktoru Xa, s enoxaparinem/warfarinem u pacientů s fibrilací síní podstupujících časnou nebo odloženou elektrickou kardioverzi. Primární cílový ukazatel (cévní mozková příhoda, systémová embolizace, infarkt myokardu a mortalita z kardiovaskulárních příčin) se vyskytl u pěti (< 1 %) nemocných léčených edoxabanem a u 11 (1 %) pacientů léčených enoxaparinem a warfarinem. Primární bezpečnostní cílový ukazatel (velké krvácení a méně závažné klinicky relevantní krvácení) se vyskytl u 16 (1 %) pacientů léčených edoxabanem a u 11 (1 %) nemocných léčených enoxaparinem a warfarinem. Studie ENSURE‑AF prokazuje bezpečnost i účinnost edoxabanu ve srovnání s enoxaparinem/warfarinem při elektrické kardioverzi nevalvulární fibrilace síní.
Key words: atrial fibrillation – anticoagulation – edoxaban – warfarin – cardioversion.
Summary:
In patients with atrial fibrillation new anticoagulants are increasingly used, than vitamin K antagonists – warfarin in the prevention of thromboembolic events. In large randomized studies was compared the effect of new anticoagulant and warfarin in non‑valvular atrial fibrillation, when the new anticoagulants were more effective and safer than warfarin. There is only one prospective trial with rivaroxaban in patients undergoing cardioversion for atrial fibrillation (X‑Vert). ENSURE‑AF is the largest prospective, randomized trial comparing edoxaban, direct factor Xa inhibitor, with enoxaparin/warfarin in patients with atrial fibrillation undergoing early or deferred electrical cardioversion. The primary endpoint (stroke, systemic embolism, myocardial infarction and mortality from cardiovascular causes) occurred in 5 (< 1%) patients treated with edoxaban and 11 (1%) treated with enoxaparin and warfarin. The primary safety endpoint (major bleeding and non‑major clinically relevant bleeding) occurred in 16 (1%) patients treated with edoxaban and in 11 (1%) patients treated with enoxaparin and warfarin. ENSURE-AF trial demonstrating the safety and efficacy of edoxaban compared to enoxaparin/warfarin when electrical cardioversion non‑valvular atrial fibrillation.
Úvod
Cévní mozková příhoda (CMP) je druhou nejčastější příčinou úmrtí na celém světě, je zodpovědná za zhruba 6,2 milionu úmrtí každý rok. Pacienti s fibrilací síní (FS) mají dvakrát vyšší mortalitu a asi 3‒5× vyšší riziko vzniku CMP než populace se sinusovým rytmem. Pravděpodobnost, že CMP bude fatální, je u pacientů s FS dvakrát vyšší než u pacientů bez FS [1‒4]. Pokud FS trvá déle než 48 hodin nebo je nejasného stáří, je u pacienta vzhledem k riziku vzniku tromboembolické nemoci nutná antikoagulační léčba. Pokud je nastavena adekvátní účinná antikoagulace, tzn. alespoň tři týdny účinná warfarinizace s hodnotou INR (mezinárodní normalizovaný poměr) 2‒3 nebo podání nových perorálních antikoagulancií (new oral anticoagulants, NOAC), potom je riziko vzniku tromboembolie v souvislosti s elektrokardioverzí či medikamentózní kardioverzí nízké (0‒1 %). Zatím byla data výskytu tromboembolických příhod u pacientů podstupujících kardioverzi k dispozici pouze z metaanalýz substudií s NOAC (studie s dabigatranem, rivaroxabanem, apixabanem) a pouze z jedné randomizované studie X VeRT s rivaroxabanem, která zahrnula celkem 1 504 nemocných a byla prezentována v roce 2014 [5,6]. Proto bylo třeba další randomizované prospektivní studie k potvrzení účinnosti a bezpečnosti NOAC u pacientů s nevalvulární fibrilací síní podstupujících elektrickou kardioverzi.
Edoxaban je perorální inhibitor koagulačního faktoru Xa, jehož účinnost a bezpečnost byla sledována ve dvou velkých klinických studiích ve srovnání s warfarinem. V roce 2013 byla prezentována klinická studie ENGAGE AF TIMI 48 s 21 105 pacienty, v níž se podával edoxaban oproti warfarinu u pacientů s nevalvulární FS z důvodu prevence tromboembolických příhod [7]. V roce 2014 byla představena studie Hokusai VTE s 8 292 pacienty, v níž se podával edoxaban v porovnání s warfarinem u pacientů s hlubokou žilní trombózou a/nebo s plicní embolií [8]. V obou studiích byla dávka edoxabanu 60 mg jednou denně. Pokud byl přítomen jeden nebo více rizikových faktorů jako středně závažná porucha funkce ledvin (clearance kreatininu [CrCl] 30‒50 ml/min), tělesná hmotnost ≤ 60 kg nebo současná medikace specifickými inhibitory P-glykoproteinu (verapamil, chinidin, dronedaron), byla dávka edoxabanu redukována ze 60 mg na 30 mg jednou denně. V obou studiích u téměř 30 000 pacientů byl edoxaban účinnější a bezpečnější než warfarin.
Studie ENSURE AF
ENSURE AF (EdoxabaN vs. warfarin in subjectS UnderRgoing cardiovErsion of Atrial Fibrillation) byla mezinárodní multicentrická, prospektivní randomizovaná, otevřená klinická studie probíhající v 239 centrech v 19 zemích Evropy a Severní Ameriky [9]. Centrum na Interní kardiologické klinice FN Brno, jehož hlavním zkoušejícím byl profesor Špinar a studijní koordinátorkou docentka Lábrová, patřilo k největším na světě. Účelem této studie bylo porovnat edoxaban se standardní antikoagulační terapií ‒ warfarinem a enoxaparinem ‒, aby se zjistilo, zda je léčba edoxabanem bezpečná a účinná v prevenci CMP a systémových embolizací u pacientů s FS podstupujících elektrickou kardioverzi. Očekávalo se, že edoxaban bude v účinnosti srovnatelný s warfarinem a bude přinejmenším stejně bezpečný jako warfarin ve vztahu k výskytu krvácení.
Charakteristika souboru, metodika a cílové ukazatele
Studie ENSURE AF probíhala
od března 2014 do října 2015, bylo do ní
zařazeno 2 119 nemoc![OBR. 1 uspořádání studie ensure‑af; podle [9] – lip, et al., 2015. a Dávka edoxabanu redukovaná na 30 mg denně, pokud pacienti splňují ≥ 1 z následujících kritérií: CrCl 15–50 ml/min; tělesná hmotnost ≤ 60 kg nebo současné užívání inhibitorů P-glykoproteinu (s výjimkou amiodaronu). b Pacienti s hodnotou INR při randomizaci ≥ 2 nevyžadovali podání enoxaparinu. CrCl – clearance kreatininu; inr – mezinárodní normalizovaný poměr, international normalized ratio; tee – transezofageální echokardiografi e](https://www.remedia.cz/photo-a-31123---.jpg) ných s nevalvulární FS,
1 095 pacientům byl podáván edoxaban a 1 104 pacientům
byl podáván enoxaparin/warfarin. Uspořádání studie ukazuje
obrázek 1,
počet randomizovaných pacientů obrázek 2.
ENSURE AF srovnávala podání 60 mg edoxabanu jednou
denně se strategií enoxaparin/warfarin u nemocných
s nevalvulární FS podstupujících elektrickou kardioverzi.
Dávka edoxabanu byla u rizikových pacientů redukovaná stejně
jako ve studii ENGAGE AF TIMI 48 u nemocných
s FS nebo ve studii Hokusai VTE u hluboké žilní
trombózy či plicní embolie ze 60 mg na 30 mg jednou
denně.
ných s nevalvulární FS,
1 095 pacientům byl podáván edoxaban a 1 104 pacientům
byl podáván enoxaparin/warfarin. Uspořádání studie ukazuje
obrázek 1,
počet randomizovaných pacientů obrázek 2.
ENSURE AF srovnávala podání 60 mg edoxabanu jednou
denně se strategií enoxaparin/warfarin u nemocných
s nevalvulární FS podstupujících elektrickou kardioverzi.
Dávka edoxabanu byla u rizikových pacientů redukovaná stejně
jako ve studii ENGAGE AF TIMI 48 u nemocných
s FS nebo ve studii Hokusai VTE u hluboké žilní
trombózy či plicní embolie ze 60 mg na 30 mg jednou
denně.![OBR. 2 randomizace nemocných ve studii ensure‑af; podle [9] – lip, et al., 2015. tee – transezofageální echokardiografie](https://www.remedia.cz/photo-a-31124---.jpg)
Pro zařazení do studie ENSURE AF musela FS trvat nejméně 48 hodin a nesměla být delší než 12 měsíců a zároveň se nemuselo jednat o nově diagnostikovanou FS, skóre CHA2DS2 VASc (index rizika vzniku tromboembolických komplikací u nemocných s FS) bylo ≥ 2 a pacienti byli indikovaní k elektrické kardioverzi. Vzhledem k tomu, že mohli být zařazeni i jedinci s recidivujícími FS, mohla být antikoagulace zahájena již před zařazením do studie nebo se mohlo jednat o novou terapii. Pokud byla hodnota INR 2‒3, nebyli pacienti ve větvi s warfarinem překryti léčbou enoxaparinem. Jestliže v této větvi došlo během tří týdnů před kardioverzí k poklesu hodnoty INR pod 2, tak se opět přechodně podával enoxaparin do účinné hodnoty INR a od užití enoxaparinu mohla být elektivní kardioverze naplánována za další tři týdny.
Průměrný věk pacientů ve skupině
s edoxabanem byl 64 let, 84 % nemocných bylo ve věku
nižším než 70 let, více než polovina zařazených (66 %) byli
muži, 81 % pacientů mělo perzistentní FS (trvání FS > 7
dnů a < 1 rok), 63 % nemocných bylo v době
zařazení do studie antikoagulováno: 47 % užívalo warfarin
a 14 % NOAC, průměrná hodnota skóre CHA2DS2 VA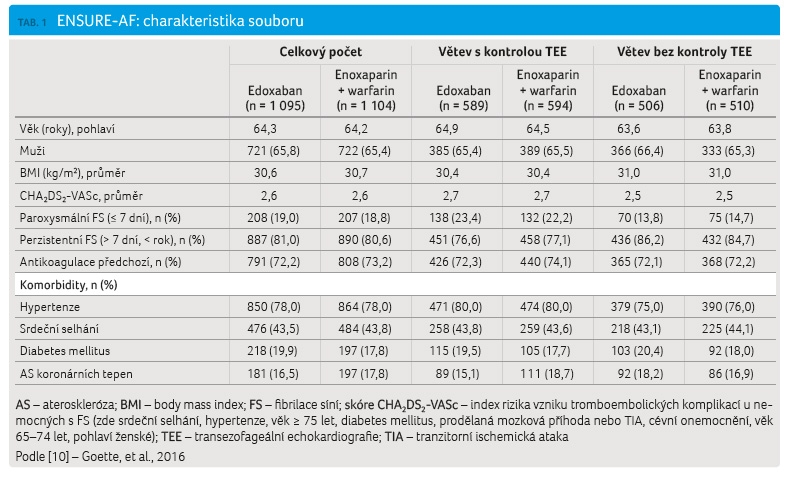 Sc
byla 2,6. V průběhu studie se hodnota warfarinu nacházela
v terapeutickém rozmezí u 70,8 % léčených, což je
vynikající úroveň antikoagulační léčby. Z komorbidit
byla nejčastěji přítomna hypertenze – v 78 %,
srdeční selhání se vyskytovalo ve 43 %, diabetes ve 20 %,
ateroskleróza koronárních tepen v 17 %, proběhlá CMP nebo
tranzitorní ischemická ataka byla zaznamenána u 6 %
jedinců. V demografických datech a základní
charakteristice se větev s warfarinem od skupiny
s edoxabanem významně nelišila. Modifikovanou charakteristiku
souboru ukazuje tabulka 1.
Sc
byla 2,6. V průběhu studie se hodnota warfarinu nacházela
v terapeutickém rozmezí u 70,8 % léčených, což je
vynikající úroveň antikoagulační léčby. Z komorbidit
byla nejčastěji přítomna hypertenze – v 78 %,
srdeční selhání se vyskytovalo ve 43 %, diabetes ve 20 %,
ateroskleróza koronárních tepen v 17 %, proběhlá CMP nebo
tranzitorní ischemická ataka byla zaznamenána u 6 %
jedinců. V demografických datech a základní
charakteristice se větev s warfarinem od skupiny
s edoxabanem významně nelišila. Modifikovanou charakteristiku
souboru ukazuje tabulka 1.
Pacienti indikovaní k elektrické kardioverzi byli dle rozhodnutí zkoušejícího zařazeni k časné nebo odložené kardioverzi. V obou skupinách byli nemocní randomizováni k terapii edoxabanem nebo enoxaparinem/warfarinem v poměru 1 : 1. Před časnou kardioverzí byla provedena transezofageální echokardiografie (TEE), pokud byl zjištěn trombus v levé síni, byla elektrická kardioverze kontraindikována a pacient ve studii nepokračoval. Po TEE mohla být elektrická kardioverze provedena nejpozději do tří dnů. Edoxaban se podával v dávce 60 mg jednou denně, pouze u 9 % pacientů byla dávka redukována na 30 mg. Pokud se podávala první dávka edoxabanu v den kardioverze, byla medikována 2‒12 h před jejím provedením. Odložená kardioverze byla provedena po minimálně třítýdenní antikoagulaci. Studijní medikace se podávala 28 dnů a potom nemocní přecházeli na warfarin dle protokolu studie nebo na léčbu jiným dostupným NOAC. Dalších 30 dnů představoval bezpečnostní interval.
Primární účinnostní složený
cílový ukazatel zahrnoval vznik CMP, systémové embolizace,
infarktu myokardu 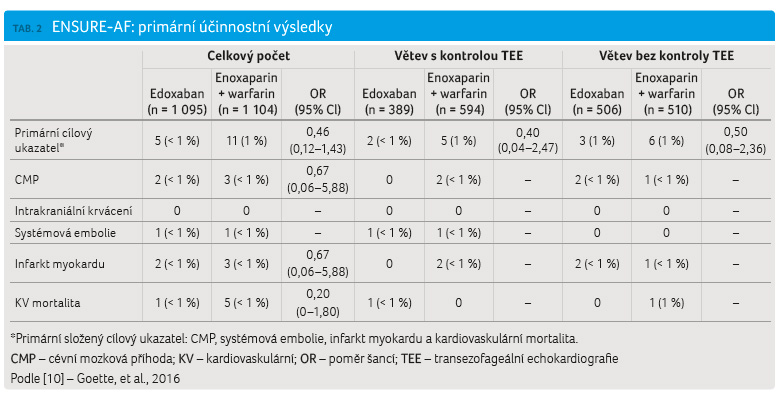 a mortalitu z kardiovaskulárních příčin
ve skupině s edoxabanem oproti podání
enoxaparinu/warfarinu v časovém období od randomizace
do konce sledování, tzn. 58 dnů po kardioverzi.
Primárním bezpečnostním cílovým ukazatelem bylo velké krvácení
a přítomnost klinicky významného menšího krvácení
po alespoň jedné dávce léčiva.
a mortalitu z kardiovaskulárních příčin
ve skupině s edoxabanem oproti podání
enoxaparinu/warfarinu v časovém období od randomizace
do konce sledování, tzn. 58 dnů po kardioverzi.
Primárním bezpečnostním cílovým ukazatelem bylo velké krvácení
a přítomnost klinicky významného menšího krvácení
po alespoň jedné dávce léčiva.
Výsledky studie
Výsledky studie ENSURE AF byly
prezentovány v roce 2016 na kongresu Evropské
kardiologické společnosti (European Society of
Cardiology, ESC) v Římě a publikovány ve stejném
roce v odborném časopise Lancet. Primární složený cílový
ukazatel se vyskytl u pěti (< 1 %) nemocných léčených
edoxabanem a u 11 (1 %) pacientů léčených
enoxaparinem a warfarinem (nesignifikantní) [10]. Výsledky
primárního složeného cílového ukazatele ukazuje tabulka 2
a graf 1.![GRAF 1 složený primární cílový ukazatel studie ensure‑af; podle [10] – Goette, et al., 2016. Ci – interval spolehlivosti; OR – poměr šancí; tee – transezofageální echokardiografi e; ttr – čas v terapeutickém rozmezí](https://www.remedia.cz/photo-a-31127---.jpg)
Primární bezpečnostní cílový
ukazatel se vyskytl u 16 (1 %) pacientů léčených
edoxabanem a u 11 (1 %) nemocných léčených
enoxaparinem/warfarinem (nesignifikantní), jak uvádí tabulka 3.
Výskyt jak složeného primárního účinnostního, tak
bezpečnostního cílového ukazatele prokazuje bezpečnost
i účinnost edoxabanu při elektrické kardioverzi nevalvulární
fibrilace síní. Výsledky nebyly závislé na tom, zda se
jednalo o kardioverzi časnou, kontrolovanou TEE, nebo
o kardioverzi odloženou.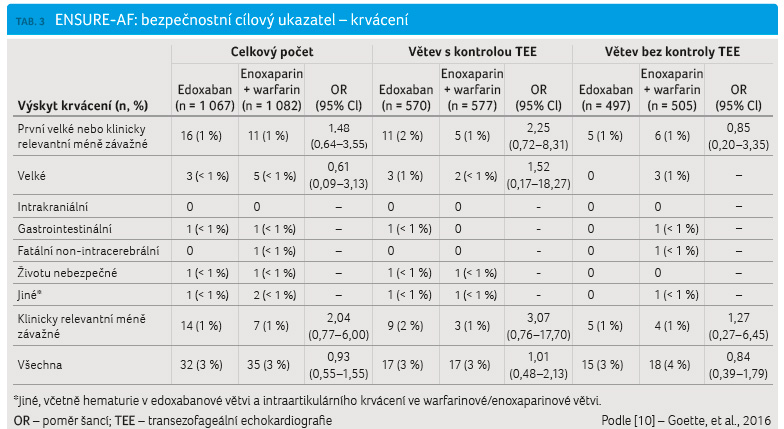
Závěr
ENSURE AF je největší prospektivní randomizovanou klinickou studií s antikoagulační léčbou u elektrické kardioverze provedené z důvodu nevalvulární fibrilace síní prokazující bezpečnost i účinnost edoxabanu ve srovnání s terapií enoxaparinem/warfarinem. Při používání NOAC se nemůžeme laboratorně přesvědčit, zda je antikoagulace účinná, zda pacient medikaci užívá pravidelně, proto je nutné se nemocného na tuto informaci zeptat a zaznamenat ji do dokumentace. Pokud je compliance k léčbě NOAC nejasná, je lépe kardioverzi odložit a vyloučit nález trombu pomocí TEE nebo provést specifické testy na přítomnost přímých inhibitorů trombinu (Hemoclot test) nebo inhibitorů koagulačního faktoru Xa. Nález trombu při TEE je kontraindikací k provedení kardioverze. Nově je kontraindikací k výkonu rovněž přítomnost „sludge“ v oušku levé síně. Kardioverze je indikována, pokud je v levé síni přítomen pouze spontánní echokontrast a v případě, jestliže dojde k rozpuštění trombu v srdečních oddílech.
Práce byla podpořena
projektem
(Ministerstva zdravotnictví ČR) koncepčního rozvoje
výzkumné organizace 65269705 (FN Brno).
Seznam použité literatury
- [2] Špinar J, Vítovec J. Edoxaban v klinických studiích a klinické praxi. Remedia 2016; 26: 1–4.
- [3] Čihák R, Haman L, Táborský M. Updated European Heart Rhythm Association Practical Guide on the use of non‑vitamin K antagonist anticoagulants in patients with non‑valvular atrial fibrillation: Summary of the document prepared by the Czech Society of Cardiology, Cor et Vasa 2016; 58: e153–e174, jak vyšel v online verzi Cor et Vasa na http://www.sciencedirect.com/science/article/pii/S0010865016000084.
- [4] Heidbuchel H, Verhamme P, Alings P, et al. Updated European Heart Rhythm Association Practical Guide on the use of non‑vitamin K antagonist anticoagulants in patients with non‑valvular atrial fibrillation. Europace 2015; 17: 1467–1507.
- [5] Cappato R, Ezekowitz MD, Klein AL, et al. Rivaroxaban vs. vitamin K antagonists for cardioversion in atrial fibrillation. Eur Heart J 2014; 35: 3346–3355.
- [6] Plitt A, Ezekowitz MD, De Caterina R, et al. Cardioversion of atrial fibrillation in ENGAGE AF‑TIMI 48. Clin Cardiol 2016; 39: 345–346.
- [7] Gugliano RP, Ruff CT, Braunwald E, et al. For the ENGAGE TIMI 48 Investigators: Edoxaban versus warfarin in Patients with Atrial fibrillation. NEJM 2013; 369: 2093–2104.
- [8] The Hokusai‑VTE Investigators: Edoxaban versus Warfarin for the Treatment of Symptomatic Venous Tromboembolism. N Engl J Med 2013; 369: 1406–1415.
- [9] Lip GY, Merino J, Ezekowitz M, et al. A prospective evaluation of edoxaban compared to warfarin in subjects undergoing cardioversion of atrial fibrillation: the edoxaban vs. warfarin in subjects undergoing cardioversion of atrial fibrillation (ENSURE‑AF) study. Am Heart J 2015; 169: 597–604.
- [10] Goette A, Merino JL, Ezekowitz MD, et al. Edoxaban versus enoxaparin–warfarin in patients undergoing cardioversion of atrial fibrillation (ENSURE‑AF): a randomised, open‑label, phase 3b trial. Lancet 2016; 388: 1995–2003. doi:10.1016/