Použití asciminibu u polymorbidního nemocného s CML s intolerancí dvou předchozích linií léčby tyrozinkinázovými inhibitory
Souhrn
Szeligová L. Použití asciminibu u polymorbidního nemocného s CML s intolerancí dvou předchozích linií léčby tyrozinkinázovými inhibitory.
Zavedení cílené léčby tyrozinkinázovými inhibitory (TKI) do klinické praxe zásadně změnilo osud nemocných s chronickou myeloidní leukemií. Nicméně stále zůstává nemalá skupina pacientů, u nichž není léčebná odpověď dostatečně hluboká, léčebnou odpověď ztrácejí nebo TKI musejí být vysazeny pro nežádoucí účinky. S cílem minimalizovat nežádoucí účinky TKI byl vyvinut asciminib s odlišným mechanismem účinku. Lék představuje vítanou alternativu především u starších polymorbidních pacientů, jak dokládá i popisovaný případ. Klíčová slova: chronická myeloidní leukemie – tyrozinkinázové inhibitory – asciminib – polymorbidní pacient.
Summary
Szeligova L. Asciminib use in a polymorbid patient with CML and intolerance of two previous lines of tyrosine kinase inhibitor treatment.
Introduction of targeted tyrosine kinase inhibitor (TKI) treatment in clinical practice has changed the fate of patients with chronic myeloid leukemia dramatically. However, there are still quite many patients in whom the therapeutic response is not deep enough, gets lost over time or has to be given up because of TKI adverse effects. Asciminib has been developed in order to minimize these side effects thanks to its different mechanism of action. This drug represents a welcome alternative especially in older polymorbid patients, as shown in our case study. Key words: chronic myeloid leukemia – tyrosine kinase inhibitors – asciminib – polymorbid patient.
Úvod
Chronická myeloidní leukemie (CML) je myeloproliferativní onemocnění, které je charakteristické přítomností tzv. filadelfského chromozomu, kdy dochází k reciproké translokaci části ramének mezi chromozomy 9 a 22 za vzniku fúzního genu BCR::ABL1. Vznikne tak patologická konstitutivně aktivovaná tyrozinkináza BCR::ABL1, která způsobí nekontrolovanou proliferaci myeloidních buněk a sníženou odpověď na proapoptotické signály [1].
Zavedení cílené léčby tyrozinkinázovými inhibitory (TKI) do klinické praxe v roce 2001 zásadně změnilo osud nemocných a z fatálního onemocnění se stalo onemocnění chronické. Nicméně stále zůstává nemalá skupina pacientů (20–30 %), u nichž není léčebná odpověď dostatečně hluboká, léčebnou odpověď ztrácejí nebo TKI musejí být vysazeny pro nežádoucí účinky [2]. S cílem minimalizovat nežádoucí účinky TKI byl vyvinut lék asciminib, první zástupce nové třídy inhibitorů STAMP (Specifically Targeting the BCR‑ABL Myristoyl Pocket). Ten má odlišný mechanismus účinku než ostatní používané TKI, které cílí na vazebné místo pro adenosintrifosfát (ATP). Asciminib cílí na jiné vazebné místo kinázy BCR::ABL1 – myristoylovou kapsu –, čímž napodobuje autoinhibiční účinek ABL [3]. Asciminib byl schválen americkým Úřadem pro kontrolu potravin a léčiv (FDA) v říjnu 2021 a Evropskou lékovou agenturou (EMA) v srpnu 2022 pro léčbu nemocných s CML léčených alespoň dvěma TKI nebo s mutací T315I.
Popis případu
Pacient ve věku 75 let byl odeslán do naší ambulance pro nově zjištěnou CML BCR::ABL1 pozitivní v chronické fázi, podtyp major b2a2. Ve vstupních parametrech krevního obrazu byly leukocyty 211 × 109/l, hemoglobin 99 g/l, trombocyty 525 × 109/l. Dále měl nemocný hmatnou splenomegalii s přesahem 7 cm pod žeberní oblouk, dle ultrasonografického vyšetření byla velikost sleziny 19 cm × 8 cm × 5 cm. Klinicky si nemocný stěžoval při minimální námaze na dušnost trvající asi dva týdny a na nechtěné hubnutí – snížení hmotnosti o 10 kg během dvou měsíců. Prognostická skóre CML byla: Sokalovo 1,24 (vysoké), Hasfordovo 1 012,16 (střední) a EUTOS 70 (nízké). Jednalo se o obézního polymorbidního nemocného s ischemickou chorobou srdeční po infarktu myokardu v minulosti s nutností zavedení stentu, s diabetes mellitus 2. typu a hypertenzí.
Po úvodní cytoredukční terapii hydroxykarbamidem byla zahájena léčba TKI imatinibem ve standardní dávce 400 mg/den. Během prvního měsíce léčby se rozvinula kožní toxicita (svědivý celotělový exantém), dále průjem a otoky obličeje, které nevymizely ani po redukci dávky na 300 mg/den a adekvátní podpůrné léčbě. Proto byl po třech měsících léčby imatinib vysazen a zahájena léčba TKI 2. generace dasatinibem v mírně redukované dávce 90 mg/den pro předchozí toxicitu imatinibu. Léčba byla zpočátku dobře tolerována. Ve třetím měsíci léčby bylo dosaženo velké molekulární odpovědi (major molecular response, MMR) a po šesti měsících léčby byla léčebná odpověď na úrovni MR 4.0. Pro neurotoxicitu byla dávka v devátém měsíci léčby snížena na 70 mg/den, pro kožní toxicitu byla v 15. měsíci léčby nutná další redukce dasatinibu na 70 mg 5× týdně. Z důvodu další toxicity – progredující bolesti hlavy, přičemž neurologické vyšetření bylo bez patologie – byl dasatinib vysazen a byla zavedena analgetická léčba.
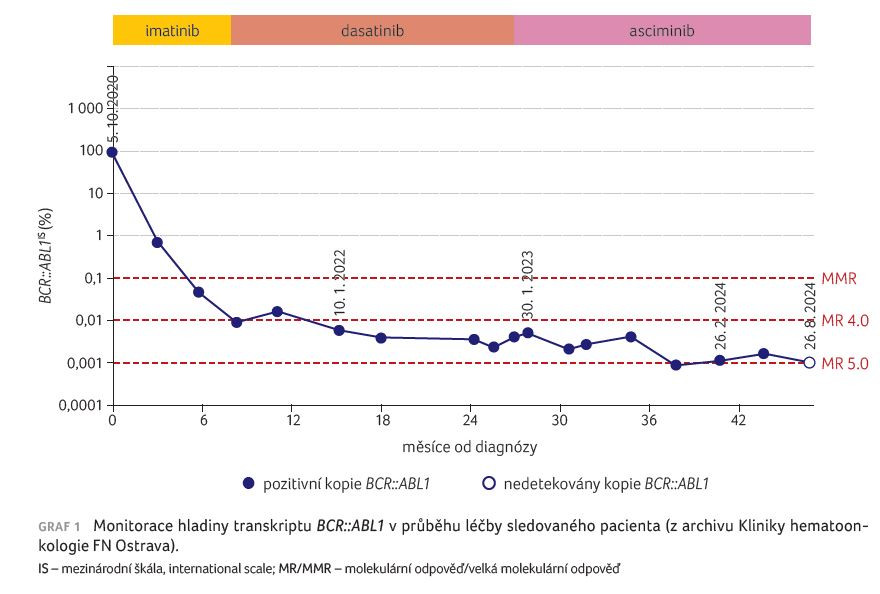 Ve třetí linii byla zahájena léčba inhibitorem STAMP asciminibem ve standardní dávce 80 mg/den. Po úvodní dobré toleranci se ve třetím měsíci výrazně zhoršily bolesti hlavy, rozvinulo se nechutenství, slabost, léčba asciminibem byla přerušena a bylo objednáno vyšetření mozku magnetickou rezonancí (MR). Po měsíci přerušení léčby nedošlo ke zmírnění bolestí hlavy, tedy bylo zhodnoceno, že potíže nesouvisejí s asciminibem. Byla navýšena dávka analgetik a znovuzahájena léčba asciminibem. Krátce nato byl nemocný hospitalizován na spádovém neurologickém oddělení pro rozvoj dvojitého vidění a ztráty rovnováhy. Na provedeném vyšetření výpočetní tomografií (CT) mozku byla popisována suspektní mastoiditida vpravo. Otorinolaryngologem byl nález zhodnocen jako chronický zánět středouší, byl chirurgicky ošetřen a klinický stav nemocného se zlepšil. Na doplněném MR vyšetření mozku byla popisována mírná atrofie mozku, prosáknutí pyramid a mastoidálních sklípků, bez známek abscesu či empyému, bez známek trombózy splavů. Vzhledem k přetrvávajícím, i když výrazně zmírněným obtížím byla dávka asciminibu redukována na polovinu, tedy na 40 mg/den. Nyní – po dalších 18 měsících léčby asciminibem – je stav nemocného stabilní, mírné chronické bolesti hlavy přetrvávají a léčebná odpověď se prohloubila na MR 5.0 s negativním nálezem kopií BCR::ABL1 (graf 1).
Ve třetí linii byla zahájena léčba inhibitorem STAMP asciminibem ve standardní dávce 80 mg/den. Po úvodní dobré toleranci se ve třetím měsíci výrazně zhoršily bolesti hlavy, rozvinulo se nechutenství, slabost, léčba asciminibem byla přerušena a bylo objednáno vyšetření mozku magnetickou rezonancí (MR). Po měsíci přerušení léčby nedošlo ke zmírnění bolestí hlavy, tedy bylo zhodnoceno, že potíže nesouvisejí s asciminibem. Byla navýšena dávka analgetik a znovuzahájena léčba asciminibem. Krátce nato byl nemocný hospitalizován na spádovém neurologickém oddělení pro rozvoj dvojitého vidění a ztráty rovnováhy. Na provedeném vyšetření výpočetní tomografií (CT) mozku byla popisována suspektní mastoiditida vpravo. Otorinolaryngologem byl nález zhodnocen jako chronický zánět středouší, byl chirurgicky ošetřen a klinický stav nemocného se zlepšil. Na doplněném MR vyšetření mozku byla popisována mírná atrofie mozku, prosáknutí pyramid a mastoidálních sklípků, bez známek abscesu či empyému, bez známek trombózy splavů. Vzhledem k přetrvávajícím, i když výrazně zmírněným obtížím byla dávka asciminibu redukována na polovinu, tedy na 40 mg/den. Nyní – po dalších 18 měsících léčby asciminibem – je stav nemocného stabilní, mírné chronické bolesti hlavy přetrvávají a léčebná odpověď se prohloubila na MR 5.0 s negativním nálezem kopií BCR::ABL1 (graf 1).
Závěr
Přes dobrou účinnost u většiny nemocných jsou TKI u nezanedbatelné skupiny zejména starších polymorbidních pacientů špatně tolerovány i v redukovaných dávkách a je nutné je vysadit. Pro tyto nemocné je vítanou alternativou asciminib s odlišným mechanismem účinku. Jak ukazuje případ našeho nemocného, je možnost redukovat dávku vítaným způsobem, jak dosáhnout dobré, v našem případně dokonce prohloubené léčebné odpovědi a současně zajistit dobrou toleranci léčby.
MUDr. Lenka Szeligová, Ph.D.
Klinika hematoonkologie, FN Ostrava
17. listopadu 1790, 708 52 Ostrava
e‑mail: lenka.szeligova@fno.cz
Literatura
[1] Soverini S, Mancini M, Bavaro L, et al. Chronic myeloid leukemia: the paradigm of targeting oncogenic tyrosine kinase signaling and counteracting resistance for succesful cancer therapy. Mol Cancer 2018; 17: 49.
[2] Hochhaus A, Souselle S, Rosti G, et al. Chronic myeloid leukemia ESMO Clinical Practice Guidelines for diagnosis, treatment and follow‑up. Ann Oncol 2017; 28(Suppl 4): iv41–iv51.
[3] Schoepfer J, Jahnke W, Berellini G, et al. Discovery of asciminib (ABL001), an allosteric inhibitor of the tyrosine kinase activity of BCR‑ABL1. J Med Chem 2018; 61: 8120–8135.
Kompletní ZASTŘENO Asciminib najdete na https://www.remedia.cz/specialy/zaostreno-asciminib/